 |
Задачи для самостоятельного решения
|
|
|
|
1. Напишите электронные формулы для следующих элементов: 6C, 12Mg, 16S, 21Sc.
2. Элементы имеют следующие электронные формулы:
а) 1s2 2s2 2p4.
б) 1s2 2s2 2p6 3s2 3p1.
в) 1s2 2s2 2p6 3s2 3p6 3d6 4s2.
Какие это элементы? Напишите их латинские символы и названия на латинском и русском языках.
3. Элемент имеет внешний электронный уровень такого строения:...3p3. Что это за элемент?
4. Напишите электронную формулу для элемента с зарядом ядра Z = 12.
5. Какие из перечисленных атомов и ионов имеют электронные конфигурации, одинаковые с атомом 18Ar: Ca2+, Cl-, K, Na+, S2-, As3-, Al3+?
1. Какие из перечисленных подуровней не существуют: 2s, 4f, 2p, 3d, 1p, 2d, 1s, 3f?
2. Сколько электронов и протонов содержит молекула аммиака NH3?
3. Даны элементы с зарядами ядер Z = 3 и Z = 19. Который из них лучший донор электронов?
4. Перечисленные элементы разделите на доноры и акцепторы электронов. Сколько электронов нужно отдать или принять каждому из них, чтобы приобрести электронную оболочку благородного газа неона? Напишите символы соответствующих ионов этих элементов: O, Na, Al, Mg, F.
5. Атом превращается в ион, если принимает или отдает электроны с внешней оболочки. Напишите электронные формулы элементов с зарядами ядер Z = 3 и Z = 9. Руководствуясь правилом октета, ответьте на вопрос: какой из этих элементов склонен образовывать отрицательно заряженные, а какой - положительно заряженные ионы?
6. Даны элементы с зарядами ядер Z = 7 и Z = 15. Который из них лучший акцептор электронов?
7. Напишите электронную формулу элемента с зарядом ядра Z = 24. Нарисуйте орбитальную диаграмму последней (внешней) электронной оболочки.
8. Даны два элемента - с зарядами ядер Z = 17 и Z = 18. Один из них - ядовитый газ с резким запахом. Другой - не ядовит, лишен запаха, не поддерживает дыхания. Напишите электронные формулы обоих элементов. Какой из них ядовит?
|
|
|
9. Нарисуйте орбитальную диаграмму для углерода (заряд ядра Z = 6). Сколько неспаренных электронов на внешней электронной оболочке углерода?
10. Сокращенная электронная формула элемента изображена в виде:...5p3. Какой это элемент? Напишите полную электронную формулу и набор квантовых чисел для “последнего” электрона на внешнем электронном уровне.
11. Сокращенная электронная формула элемента изображена в виде:...3d8. Какой это элемент? Напишите полную электронную формулу и набор квантовых чисел для 8-го электрона на d-подуровне.
12. Напишите полную электронную формулу и нарисуйте орбитальную диаграмму для элемента 19K. Запишите набор квантовых чисел для последнего (наиболее далекого от ядра) электрона этого элемента.
13. В каком элементе при его образовании из субатомных частиц последним свое место в электронной оболочке займет электрон с таким набором квантовых чисел: n = 3, l = 2, m = 1, s = 1/2? Напишите полную электронную формулу для этого элемента.
14. Для какого элемента “последним” в электронной оболочке будет электрон с таким набором квантовых чисел: n = 4, l = 1, m = 1, s = 1/2? Напишите полную электронную формулу для этого элемента. Сколько у него неспаренных электронов?
15. Для какого элемента “последним” в электронной оболочке будет электрон с таким набором квантовых чисел: n = 2, l = 1, m = 0, s = 1/2? Напишите полную электронную формулу. Почему этот элемент не может быть благородным? Какой подуровень не заполнен по сравнению с ближайшим благородным элементом? Какой благородный элемент ближайший по электронному строению?
16. Запишите основной терм ионов с электронными конфигурациями  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  . Определить мультиплетность и полную степень вырождения основных термов.
. Определить мультиплетность и полную степень вырождения основных термов.
17. Для ионов с электронными конфигурациями  ,
,  ,
,  ,
,  ,
,  ,
, 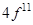 укажите полное число микросостояний.
укажите полное число микросостояний.
|
|
|
18. Укажите какой орбитальный и какой спиновый моменты соответствуют термам:  .
.
19. Постройте диаграмму молекулярных орбиталей молекулы водорода: (а) однократно ионизированной; (б) находящейся в возбужденном состоянии.
20. Постройте диаграмму молекулярных орбиталей молекулы СО.
|
|
|


