 |
Количественный анализ индивидуальных и смешанных растворов моногидрохлорида лизина и глицина спектрофотометрическим методом
|
|
|
|
Для количественного определения моногидрохлорида лизина и глицина в исследуемых растворах использовали спектрофотометрический метод (см. методику).
Предположив, что цвиттерионы глицина не сорбируется на катионите, считаем, что концентрация глицина в элюате соответствует концентрации глицина в исходной разделяемой смеси, которая составила 1,6×10-3моль/л. По градуировочному графику (рис. 3) с учетом закона аддитивности оптических плотностей (1) была определена концентрация моногидрохлорида лизина в элюате, которая составила 8,6×10-6моль/л.


|
 K LysHCl = C
K LysHCl = C
ysHCl CGlyGly
ysHCl Gly
(6, 7)


|
 выходе из колонки.
выходе из колонки.
KLysHCl QLysHCl

 LysHCl LysHCl
LysHCl LysHCl
Gly Gly LysHCl LysHCl
(8, 9)
 где aLysHCl– коэффициент разделения исследуемых аминокислот; RLysHCl – степень извлечения лизина из фазы раствора; QLysHCl, QLysHCl − количество моногидрохлорида
где aLysHCl– коэффициент разделения исследуемых аминокислот; RLysHCl – степень извлечения лизина из фазы раствора; QLysHCl, QLysHCl − количество моногидрохлорида
лизина в растворе и в фазе ионита соответственно, моль. Для расчета количества моногидрохлорида лизина в растворе и в фазе ионита находили QLysHCl в исходном растворе и в элюате, собранном после разделения.
Таблица 4. Результаты расчета параметров разделения исследуемых аминокислот
|
|
|
| KLysHCl | KGly | aLysHCl/Gly | KLysHCl× KGly | RLysHCl, % |
| 26,30 | 0,05 | 1,31 |
Из данных табл. 4 можно сделать вывод, что разделение моногидрохлорида лизина и глицина на катионите КУ-2-8 прошло практически полностью.
 Количественный анализ индивидуальных и смешанных растворов моногидрохлорида лизина и глицина методом доннановского потенциала
Количественный анализ индивидуальных и смешанных растворов моногидрохлорида лизина и глицина методом доннановского потенциала
В качестве точного и экспрессного метода для количественного определения лизина использовали разработанный нами потенциометрический сенсор для определения лизина в водных растворах [21] на основе перфторированной сульфокатионитовой мембраны МФ-4СК. Откликом сенсора является доннановский потенциал на индивидуальной границе исследуемый раствор/ мембрана в лизиновой форме. Рабочий диапазон рН анализируемых растворов составил 5-7.
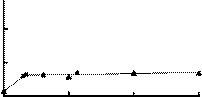
Для определения селективности сенсора к катионам лизина в водных растворах глицина и хлорида аммония использовали метод смешанных растворов [22]. На рисунке 4 представлены зависимости доннановского потенциала от концентрации мешающего компонента в смешанных растворах моногидрохлорида лизина и глицина.
-∆f, мВ

 1
1
110,0
80,0 2
50,0 -lgСGly 0,0 1,0 2,0 3,0
Рис.4. Зависимости доннановского потенциала в системах LysHCl+Gly / МФ-4СК от концентрации глицина при концентрациях моногидрохлорида лизина
СLysHCl, моль/л: 1 – 0,001; 2 – 0,010.
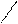 Значения константы селективности KLysH + рассчитывали как отношение Gly ±
Значения константы селективности KLysH + рассчитывали как отношение Gly ±
концентраций определяемого и мешающего которых наблюдается заметное отклонение значения.
компонентов в точках, начиная с отклика сенсора от постоянного
KLysH +
Х
CLysH +
 CХ
CХ
(10)
Аналогичным способом были определены константы селективности (10) сенсора к катионам лизина в присутствии хлорида аммония.
|
|
|
 Средние значения концентрационных констант селективности KLysH + для Х
Средние значения концентрационных констант селективности KLysH + для Х
исследуемых растворов, представлены в табл.5.
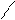 Таблица 5. Средние концентрационные константы селективности KLysH + в Х
Таблица 5. Средние концентрационные константы селективности KLysH + в Х
исследуемых растворах
| Исследуемый водный раствор | KLysH + Х |
| LysHCl+Gly | 0,015 ± 0,004 |
| LysHCl+NH4Cl | 0,030 ± 0,005 |
 Для определения моногидрохлорида лизина в индивидуальных и смешанных растворах использовали метод калибровочного графика. Зависимость доннановского потенциала на границе раствор/ мембрана МФ-4СК от концентрации LysHCl в индивидуальном растворе (рис. 5) определяется уравнением (11) с достоверностью аппроксимации 0,99.
Для определения моногидрохлорида лизина в индивидуальных и смешанных растворах использовали метод калибровочного графика. Зависимость доннановского потенциала на границе раствор/ мембрана МФ-4СК от концентрации LysHCl в индивидуальном растворе (рис. 5) определяется уравнением (11) с достоверностью аппроксимации 0,99.
∆f = −32,5+50,6×lg CLysHCl (11)
−∆fD, мВ

 125,0
125,0
100,0
75,0
50,0
25,0 −lgСLysHCl0,0
0,8 1,8 2,8
Рис.5. Калибровочная зависимость доннановского потенциала от концентрации LysHCl в индивидуальных растворах
Количество моногидрохлорида лизина в исходном разделяемом растворе, определенное с помощью разработанного метода составило (1,64±0,09)×10-6моль. Для разделения исходный раствор пропускали через колонку, заполненную сульфокатионитом КУ-2-8 в Na+-форме, в которой проходила сорбция катионов лизина. Десорбция ионов лизина из фазы сорбента проводилась 10% раствором аммиака. В состав элюата входили ионы Lys-, NH4+, OH-. Для создания нейтральной среды полученный элюат подкисляли концентрированной соляной кислотой. Количество вещества моногидрохлорида лизина в элюате определенное с помощью разработанного потенциометрического метода, составило (1,55±0,08)×10-6 моль. Погрешность определения моногидрохлорида лизина не превышала 5 %.
Заключение
Исследованы условия разделения лизина и глицина с использованием катионита КУ-2-8. Разделение основано на различных значениях pI АК: для лизина pI составляет 9,59, а для глицина – 5,97. Процесс разделения проводился в диапазоне рН от 5 до 7, когда в разделяемом растворе лизин находится в основном в форме однозарядных катионов, а глицин – цвиттерионов. Разделение протекает по реакции ионного обмена между ионами Lys+фазы раствора и ионами Na+фазы сорбента, цвиттерионы глицина не сорбируются и выходят из колонки с элюатом. Элюирование катионов лизина из фазы ионообменника проводили 5% раствором аммиака. Десорбция лизина основана на реакции протонирования/ депротонирования.
|
|
|
Спектрофотометрическим и ТСХ методами были исследованы смешанные и индивидуальные растворы глицина и моногидрохлорида лизина, а так же раствор, полученный после разделения глицина и моногидрохлорида лизина. Методом ТСХ
 было показано, что разделение произошло полностью. Рассчитаны такие количественные характеристики разделения, как коэффициенты распределения глицина и моногидрохлорида лизина, которые составили 26,3 и 0,05 соответственно; коэффициент разделения моногидрохлорида лизина и глицина, с использованием катионита КУ-2-8 в Na+форме, – 526; и степень извлечения моногидрохлорида лизина из раствора – 99%.
было показано, что разделение произошло полностью. Рассчитаны такие количественные характеристики разделения, как коэффициенты распределения глицина и моногидрохлорида лизина, которые составили 26,3 и 0,05 соответственно; коэффициент разделения моногидрохлорида лизина и глицина, с использованием катионита КУ-2-8 в Na+форме, – 526; и степень извлечения моногидрохлорида лизина из раствора – 99%.
Для определения лизина в аналите и элюате использовали разработанный нами потенциометрический сенсор на основе перфторированной сульфокатионитовой мембраны МФ-4СК, откликом которого является доннановский потенциал. Определены средние концентрационные константы селективности сенсора к катионам лизина в присутствии аминокислоты глицин и хлорида аммония, которые не превышали 0,035. Относительная погрешность определения моногидрохлорида лизина в исследуемых растворах составила 2-5 %.
Литература:
Определение лизина после разделения смешанных растворов лизина и глицина с использованием катионита КУ-2-8
Агупова М.В., Бобрешова О.В., Бобринская Г.А., Якунина Т.В.
|
|
|


