 |
Распространенность и значение в природе
|
|
|
|
Конденсированные системы гетероциклов. Пурин, ароматичность. Гидрокси- и аминопроизводные пурина: гипоксантин, ксантин, мочевая кислота, аденин, гуанин. Лактим-лактамная таутомерия. Кислотные свойства мочевой кислоты, ее соли (ураты). Метилированные ксантины: кофеин, теофиллин, теобромин. Качественные реакции метилированных ксантинов
Конденсированные системы гетероциклов:
Гетероциклические соединения с орто -конденсированными и орто- и пери -конденсированными кольцами называют по тем же правилам, что и конденсированные углеводороды (правило А—21). Компоненты называют по правилам А—21, В—1 и В—2. Основным компонентом должен быть гетероцикл. Если есть возможность выбора, основной компонент выбирают в следующем порядке:
(а) Азотсодержащий компонент.
Пример:

(b) Компонент, содержащий гетероатом (кроме азота), расположенный в табл. I как можно выше. Пример:

(с) Компонент, содержащий наибольшее число колец. Пример:

(d) Компонент, содержащий самое большое из возможных кольцо. Пример:

(е) Компонент, содержащий наибольшее число любых гетероатомов. Пример:

(f) Компонент с наиболее разнообразными гетероатомами. Примеры:

(g) Компонент, содержащий наибольшее число гетероатомов, перечисленных в табл. I первыми. Пример:

(h) Если есть возможность выбора между компонентами одинаковой величины, содержащими одинаковое число одинаковых гетероатомов, то в качестве основного следует принять компонент, в котором, если рассматривать его независимо, гетероатомы имеют наиболее низкие номера.
Примерш

Если общим для конденсированных колец является гетероатом, названия компонентов выбирают так, чтобы они оба отвечали системам с гетероатомом.
|
|
|
Пример:

Могут быть использованы следующие префиксы, выражающие наличие конденсированной системы; фуро-, имидазо-, изохино-, пиридо-, пиримидо-, хино- и тиено-.
Примеры:
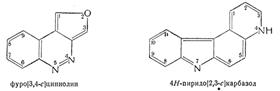
Полностью конденсированные гетероциклические системы располагают инумеруют в соответствии с принципами правила А—22. Если есть возможность выбора, систему следует ориентировать следующим образом:
(а) Гетероатомы должны получить наименьшие номера,
Примеры:

(b) Гетероатомы должны получить наименьшие номера в соответствии с табл. I.
Пример:

(с) Углеродные атомы, общие для двух или более колец, должны следовать за атомами с возможно более низкими номерами (см. правила А—22.2 и А—22.3). Гетероатом, общий для двух колец, нумеруется в соответствии с правилом В—3.4 (е).
Примеры:

В сложном названии с префиксом, показывающим сращение колец (т. е. когда требуется более одной пары скобок), точки сращения обозначают цифрами со штрихами и без штрихов, при этом цифры без штрихов даются кольцу, непосредственно присоединенному к основному компоненту.
Примеры:

(d) Насыщенные атомы (несущие «лишний» водород) должны получить по возможности низкие номера:

(е) Кольца нумеруются так же, как в углеводородах, но номерами обозначают все гетероатомы, в том числе и общие для двух или более колец. Внутренние гетероатомы нумеруют последними по кратчайшему расстоянию от предыдущего атома с самым большим номером.
Пурин, ароматичность:
Пурин — простейший представитель имидазо[4,5-d]пиримидинов. Бесцветные кристаллы, хорошо растворимые в воде, горячем этаноле и бензоле, плохо растворимые в диэтиловом эфире, ацетоне и хлороформе.
Реакционная способность [править]
Пурин проявляет амфотерные свойства (рКа 2,39 и 9,93), образуя соли с сильными минеральными кислотами и металлами (замещается водород имидазольного цикла).
|
|
|
Для пурина характерна прототропная таутомерия по имидазольному атому водорода, в водных растворах в таутомерном равновесии присутствует смесь 7H- и 9H-таутомеров:

Ацилирование и алкилирование пурина идет по имидазольным атомам азота. Так, при ацилировании уксусным ангидридом образуется смесь 7- и 9-ацетилпуринов, при алкилировании метилйодидом серебряной соли пурина либо диметилсульфатом в щелочных условиях образуется 9-метилпурин, действие избытка йодистого метила в диметилформамиде ведет к кватернизации с образованием йодида 7,9-диметилпуриния.
Пурин — электрондефицитная гетероциклическая система, поэтому реакции электрофильного замещения для него нехарактерны. При действии пероксида водорода, подобно пиридину, образует N-оксиды (смесь 1- и 3-оксидов при действии H2O2 в уксусном ангидриде).
При сплавлении с серой при 245 °С тионируется по имидазольному циклу с образованием 8-меркаптопурина.
Синтез
Впервые пурин был синтезирован Эмилем Фишером из мочевой кислоты 8 замещением кислорода на хлор действием пентахлорида фосфора и дальнейшим восстановлением образовавшегося 2,6,8-трихлорпурина 10: 
Благодаря доступности мочевой кислоты метод Фишера сохранил некоторое значение и по настоящее время, восстановление 2,6,8-трихлорпурина проводится цинковой пылью.
Лабораторный метод синтеза пурина — циклизация 4,5-диаминопиримидина действием муравьиной кислоты или формамида (синтез Траубе).
Биологическое значение
Производные пурина играют важную роль в химии природных соединений (пуриновые основания ДНК и РНК; кофермент NAD; алкалоиды, кофеин, теофиллин и теобромин; токсины,сакситоксин и родственные соединения; мочевая кислота) и, благодаря этому, в фармацевтике.

Гидрокси- и аминопроизводные пурина: гипоксантин, ксантин, мочевая кислота, аденин, гуанин.
Ксантин:
КСАНТИН (2,6-пуриндион, ф-ла I), мол. м. 152,12; бесцв. кристаллы, при нагр. разлагаются без плавления (с возгонкой); рК 0,8 (N-3), 7,4 (N-7), 11,1 (N-1); в УФ спектре lмaкc (в нм) 267 (рН 2), 241 и 278 (рН 10); lge соотв. 4.01, 3,95 и 3.97. Легко раств. в формамиде, горячем глицерине, разб. к-тах ищелочах, плохо - в воде, этаноле, эфире. Существует в таутомерном равновесии с гидроксиформой II (равновесие сдвинуто влево):

С минер, к-тами ксантин образует легко гидролизующиеся соли (т-ра плавления перхлората 262-264 °С), с аммиачным р-ром AgNO3 - нерастворимую серебряную соль. Ксантин устойчив к действию горячих водных р-ров к-т и щелочей. При взаимод. с НСl при 200 oС разлагается на СО2, NH3, глицин и муравьиную к-ту. При окислении с помощью КМnО4 или КСlО3 в присут. НCl образует аллоксан (качеств. определение ксантина), при восстановлении с помощью Zn в НСl или амальгамой Na-6-дезоксиксантин; под действием P2SS в пиридине превращ. в 6-тиоксантин, с РОСl3 в присут. Н2О образует 2,6-дихлорксантин. Электроф. замещение происходит в положение 8, напр. галогенирование приводит к 8-галогенксантину, действие солей диазония в щелочной среде - к 8-азопроизводному, к-рое далее м. б. восстановлено до 8-аминоксантина или гидролизовано до мочевой к-ты. В щелочной среде ксантин легко алкилируется сначала в положение 3, затем в положения 7 и 1 (в порядке уменьшения кислотности групп NH). Так, под действием димстилсульфата в зависимости от рН реакц. среды ксантин превращ. в 3,7-диметил-ксантин (теобромин), 1,3-диметилксантин (теофиллин) или 1,3,7-триметилксантин (кофеин). В нейтральной или слабокислой среде ксантин алкилируется диметилсульфатомпо атомам N имидазольного кольца с образованием бетаиновой формы пуринового основания:

Ксантин - пуриновое основание, входящее в состав нуклеиновых к-т в качестве минорного основания. В своб. состоянии в небольших кол-вах содержится в растениях, крови, тканях и выделениях животных (в т.ч. в моче человека). Получают ксантин из мочевины и этилового эфираизонитрозо-цианоуксусной к-ты или из 4,5-дикарбамоилимидазола пол действием щелочного р-ра КВrО:

Ксантин также м.б. получен кипячением мочевой к-ты с формамидом, гидролитич. дезаминированием гуанидина, гидролизом нуклеиновых к-т, выделяемых из дрожжей, окислением гипоксантина в присут. фермента ксантинокси-дазы. Последняя окисляет ксантин в мочевую к-ту - конечный продукт пуринового обмена в организме человека. На этой р-ции основано количеств. определение ксантина в биол. материале. Ксантин также количественно определяют в виде серебряной соли. Применяют ксантин для полусинтетич. получения пуриновых алкалоидов, гл. обр. теобромина икофеина. Ксантин обладает сильным диуретич. действием.
|
|
|
|
|
|
Гипоксантин:
Гипоксантин (англ. hypoxanthine) — природное производное азотистого основания пурина. Иногда встречается в составе нуклеиновых кислот, где присутствует в антикодоне тРНК в форме нуклеозида инозина. Имеет таутомер, носящий название 6-оксопурин.[1+
] 
Реакции
Гипоксантин образуется восстановлением ксантина ферментом ксантин оксидоредуктазой.
Гипоксантин-гуанин фосфорибозилтрансфераза превращает гипоксантин в IMP.[2]
Гипоксантин также является продуктом спонтанного дезаминирования аденина, ввиду того, что гипоксантин похож по структуре на гуанин, такое дезаминирование может привести к ошибке в транскрипции или репликации.
Мочевая кислота:
Мочевая кислота — бесцветные кристаллы, плохо растворимы в воде, этаноле, диэтиловом эфире, растворимы в растворах щелочей, горячей серной кислоте и глицерине.
Мочевая кислота была открыта Карлом Шееле (1776) в составе мочевых камней и названа им каменной кислотой — acide lithique, затем она была найдена им в моче. Название мочевой кислоты дано Фуркруа, её элементарный состав установлен Либихом.

Свойства
Является двухосновной кислотой (pK1 = 5.75, pK2 = 10.3), образует кислые и средние соли — ураты.
В водных растворах мочевая кислота существует в двух формах: лактамной (7,9-дигидро-1H-пурин-2,6,8(3H)-трион) и лактимной (2,6,8-тригидроксипурин) с преобладанием лактамной:



Легко алкилируется сначала по положению N-9, затем по N-3 и N-1, под действием POCl3 образует 2,6,8-трихлорпурин.
Азотной кислотой мочевая кислота окисляется до аллоксана, под действием перманганата калия в нейтральной и щелочной среде либо перекиси водорода из мочевой кислоты образуются сначала аллантоин, затем гидантоин и парабановая кислота.
Получение
Мочевую кислоту выделяют из гуано, где её содержится до 25%.
Метод синтеза заключается в конденсации мочевины с цианоуксусным эфиром и дальнейшей изомеризации продукта в урамил (аминобарбитуровую кислоту), дальнейшей конденсации урамила с изоцианатами, изотиоцианатами или цианатом калия.
Аденин:
Аденин — азотистое основание, аминопроизводное пурина (6-аминопурин). Образует две водородных связи с урацилом и тимином(комплементарность).

Физические свойства
Аденин — бесцветные кристаллы, которые плавятся при температуре 360—365 °C. Обладает характерным максимумом поглощения (λмакс) при 266 ммк (pH 7) с коэффициентом молярной экстинкции (εмакс) 13500.
|
|
|
Химические свойства
Химическая формула С5H5N5, молекулярный вес 135,14 г/моль. Аденин проявляет основные свойства (pKa1=4,15; pKa2=9,8). При взаимодействии с азотной кислотой, аденин теряет аминогруппу, превращаясь в гипоксантин (6-оксипурин). В водных растворах кристаллизуется в кристаллогидрат с тремя молекулами воды.
Растворимость
Хорошо растворим в воде, особенно горячей, с понижением температуры воды, растворимость аденина в ней падает. Плохо растворим вспирте, в хлороформе, эфире, а также в кислотах и щелочах — не растворим.
Распространенность и значение в природе
Аденин входит в состав многих жизненно важных для живых организмов соединений, таких как: аденозин, аденозинфосфотазы, аденозинфосфорные кислоты, нуклеиновые кислоты, адениновые нуклеотиды и др. В виде этих соединений аденин широко распространен в живой природе.
Гуанин:
Гуани́н (Гуа, Gua) — азотистое основание, аминопроизводное пурина (2-амино-6-оксопурин), является составной частью нуклеиновых кислот. В ДНК, при репликации и транскрипции образует три водородных связи с цитозином (Cyt) (комплементарность). Впервые выделен из гуано.

Физические свойства
Бесцветный, аморфный кристаллический порошок. Температура плавления 365 °C. Раствор гуанина в HCl флуоресцирует. В щелочных и кислых средах имеет по два максимума абсорбции (λмакс) в ультрафиолетовом спектре: при 275 и 248 нм (pH 2) и 246 и 273 нм (pH 11).
Химические свойства
Химическая формула — C5H5N5O, молекулярная масса — 151,15 г/моль. Проявляет основные свойства, pKa1= 3,3; pKa2= 9,2; pKa3=12,3. Реагирует с кислотами и щелочами с образованием солей.
При действии на гуанин HNO2 (азотистой кислоты) образуется ксантин.
Растворимость
Хорошо растворим в кислотах и щелочах, плохо растворим в эфире, спирте, аммиачных и нейтральных растворах, нерастворим в воде.
Качественные реакции
Для определения гуанина его осаждают метафосфорной и пикриновой кислотами, с диазосульфокислотой в растворе Na2CO3 дает красное окрашивание.
|
|
|


