 |
Глава 3. Патология анаболизма гемоглобина
|
|
|
|
Государственное образовательное учреждение
Высшего профессионального обучения
Читинская государственная медицинская академия
Л.П. Никитина, З.Ц. Ринчинов
БИОХИМИЯ ЭРИТРОЦИТОВ
Учебное пособие для студентов медицинского вуза
Чита – 2006
ОГЛАВЛЕНИЕ
Список сокращений……………………………………………………………..3
ГЛАВА 1. Биохимия плазмы крови…………………………………………....5
ГЛАВА 2. Биохимия эритроцитов….………………………………………......7
2.1. Строение мембран эритроцитов; особенности метаболизма………7
2.2. Обмен порфиринов……………………………………………………9
2.2.1. Синтез гема…………………………………………………….10
2.3. Строение гемоглобина………………………………………………12
2.4. Формы гемоглобина………………………………………………....14
2.5. Свойства гемоглобина……………………………………………….15
2.6. Метаболизм железа…………………………………………………..17
ГЛАВА 3. Патология анаболизма гемоглобина……………………………….18
3.1. Болезни синтеза гемоглобина……………………………………….18
3.2. Дисгемоглобинемии………………………………………………….23
3.3. Нарушения транспорта гемоглобина в плазме крови……………...24
ГЛАВА 4. Распад эритроцитов………………………………………………….25
4.1. Метаболизм билирубина у здорового человека…………………….27
4.2. Патология обмена жёлчных пигментов……………………………..31
4.2.1. Виды желтух……………………………………………………..31
4.2.1.1. Гемолитическая желтуха……………………………………31
4.2.1.2. Паренхиматозная желтуха………………………………….36
4.2.1.3. Механическая желтуха……………………………………...38
Вопросы для самопроверки……………………………………………………...41
Список литературы…………………………………………………………….....44
|
|
|
СПИСОК СОКРАЩЕНИЙ
АлАТ – аланин-аминотрансфераза
АО – антиоксидант
АОЗ – антиоксидантная защита
АРЗ – антирадикальная защита
АсАТ – аспартат-аминотрансфераза
АТФ – аденозинтрифосфат
ГАГ – глюкозаминогликан
ГАМК – гамма-аминомасляная кислота
ГА-3-ф – глицероальдегид 3 фосфат
ГГТП – гамма-глутаминилтранспептидаза
ГПО – глутатионпероксидаза
ГР – глутатионредуктаза
Г-6-ФДГ – глюкозо-6-фосфатдегидрогеназа
ДГАФ – дигидроксиацетонфосфат
ДГ – дегидрогеназа
Ко А – коэнзим ацилирования
КОС – кислотно-основное состояние
НАД+ - никотинамидадениндинуклеотид (окисленный)
НАДН – никотинамидадениндинуклеотид (восстановленный)
НАД+Ф – никотинамидадениндинуклеотид фосфат (окисленный)
НАДФН – никотинамидадениндинуклеотид фосфат (восстановленный)
ПНЖК – полиненасыщенные жирные кислоты
ПОЛ – перекисное окисление липидов
РЭС – ретикуло-эндотелиальная система
СОД – супероксиддисмутаза
УДФГК – уридиндифосфоглюкуроновая кислота
Ф – фосфат
ЩФ – щелочная фосфатаза
ЭТЦ – электронно-транспортная цепь
G-SH – глутатион восстановленный
G-S-S-G - глутатион окисленный
Hb – гемоглобин
ГЛАВА 1. БИОХИМИЯ ПЛАЗМЫ КРОВИ
Кровь (по мнению древних, река жизни) – жидкая соединительная ткань, состоящая из суспензии клеток в концентрированном растворе белков, образующая волокнистую структуру при свертывании.
Среди основных функций этой ткани можно выделить:
дыхательную, которую выполняют клетки эритроидного ряда, захватывая в легких кислород и перенося его к тканям, а в обратном направлении – углекислый газ;
питательную - с помощью плазмы осуществляется доставка к клеткам многочисленных необходимых соединений: витаминов, различных ионов, углеводов, аминокислот, высших жирных кислот и их производных;
терморегуляторную – плазма крови обладает высокой удельной теплоемкостью и одновременно хорошей теплопроводностью, что увеличивает потери тепла при испарении воды с поверхности кожи;
|
|
|
защитную – а) элементы свёртывающей системы крови защищают от неадекватных кровопотерь; б) групповая специфика крови; в) обеспечивает иммунитет: неспецифический - c помощью фагоцитоза (нейтрофилов, моноцитов), специфический - за счёт гамма-глобулинов и других иммунных белков (гуморальный) и Т-лимфоцитов (клеточный);
регуляторную – плазмой крови к клеткам-мишеням транспортируются различные биологически активные вещества – гормоны, витамины;
выделительную – продукты метаболизма клеток током крови доставляются к соответствующим системам;
поддержание критериев гомеостаза – онкотического давления за счет белков, кислотно-основного состояния (КОС) с помощью буферных систем (бикарбонатов, фосфатов, протеинов).
Особая роль в плазме крови принадлежит белкам (табл. 1), среди которых выделяют альбумины, глобулины, фибриноген.
Около половины объёма крови занимают форменные элементы, основными из которых являются эритроциты (99%). В их общем пуле на долю молодых приходится 5%, зрелых – 85%, стареющих – 10%.
Эритроцит совсем смешон –
Всех органоидов лишён.
Навеки быть ему судьбина
Контейнером гемоглобина.
Однако назначение красных кровяных телец совсем не сводится к этой шутливой формулировке. За счет их карбоангидразы осуществляется взаимодействие диоксида углерода с водой – и транспорт углекислоты. Очень велика роль ионообмена между эритроцитами и плазмой (обмена протонов на катионы натрия) в регуляции КОС и электролитного баланса организма. Огромна ёмкость гемоглобина как буферной системы. Красные кровяные тельца служат адсорбентами для иммунных комплексов, физиологически предохраняют сосудистую стенку от развития иммунных васкулитов.
Таблица 1
Функции белков плазмы
| Функция | Пример |
| Транспортная | Тироксинсвязывающий глобулин Транскортин Сексстероидсвязывающий белок Витамин Д-связывающий глобулин Гаптоглобин (транспорт гемоглобина) Гемопексин (транспорт гема) Аполипопротеины (транспорт холестерина, триацилглицеролов) Трансферрин (транспорт железа) Церулоплазмин (транспорт меди) |
| Гуморальный иммунитет | Иммуноглобулины |
| Поддержание онкотического давления | Все белки, особенно альбумины |
| Ферменты | Ренин, факторы свёртывания крови, белки комплемента |
| Ингибиторы протеаз | Альфа-1-антитрипсин |
| Буферность | Все белки |
ГЛАВА 2. БИОХИМИЯ ЭРИТРОЦИТОВ
|
|
|
СТРОЕНИЕ МЕМБРАН ЭРИТРОЦИТОВ. ОСОБЕННОСТИ
МЕТАБОЛИЗМА
Зрелые красные кровяные тельца обладают двояковогнутой формой и большой способностью к деформации, благодаря чему эффективно обеспечивают процессы диффузии газов и могут проходить через капилляры, диаметр которых в 3-4 раза меньше самих эритроцитов. Подобное свойство обусловлено особенностями в структуре мембран этих форменных элементов.
Принципы строения цитолеммы эритроцитов классические: основу составляет билипидный слой, в который встроены различные протеины. Наружная часть липидов представлена холинсодержащими соединениями (фосфатидилхолином, сфингомиелином), внутренняя поверхность обогащена фосфатидилсерином, фосфатидилэтаноламином, более четверти объёма приходится на холестерин. К цитозолю обращена плотная анастомозирующая белковая сеть, состоящая из спектринов, анкиринов, тропомиозинов, которые связываясь с интегральными гликопротеидами (гликофоринами) создают определённую жёсткость мембраны, определяют форму эритроцита (двояковогнутый диск). От степени фосфорилирования спектринов зависит эластичность сети, способность к упругой деформации. Гликофорины, пронизывая липидный слой, с помощью гидрофобных взаимодействий с фосфолипидами прочно фиксируются; их углеводные компоненты (олигосахариды, их производные, сиаловые кислоты), располагаясь на поверхности мембраны эритроцита, служат групповыми веществами крови: для О(Н) антигена детерминанта фукоза, для А-антигена - N-ацетилгалактоз-амин, для В – галактоза. Углеводные остатки гликофоринов являются также носителями антигенов групп крови MN-типа и ряда других иммунологических детерминант, служат рецепторами для вирусов гриппа и т.д.
|
|
|
Несмотря на отсутствие ядра и других органоидов, красные кровяные тельца весьма метаболически активные образования, обладающие спонтанной энергопродукцией на уровне 80 пДж на клетку. Энергетика эритроцита основана на анаэробном гликолизе (рис. 1). Глюкоза быстро проникает в клетку, независимо от присутствия инсулина.

Рис.1. Схема гликолиза и антирадикальной защиты в эритроците.
В пути Эмбдена-Мейергофа глюкоза распадается до лактата с образованием АТФ путём субстратного фосфорилирования. Следует заметить, что кроме энергетической функции, метаболиты гликолиза используются в следующих процессах. Восстановительные потенциалы генерируются в виде НАДН, который при необходимости используется метгемоглобин-редуктазой для восстановления железа в метгемоглобине. В отличие от других тканей в эритроцитах в качестве метаболита образуется много 2,3 - дифосфоглицерата (2,3-ДФГК) (в 1000 раз больше), который служит важным модулятором сродства гемоглобина к кислороду.
Некоторые морфобиохимические особенности красных кровяных телец предопределяют необходимость в высокой антиоксидантной активности. Во-первых, это высокие концентрации О2, что увеличивает вероятность образования его активных форм. Во-вторых, большое содержание ионов переходного металла – железа, что может способствовать его использованию в качестве донора электронов (рис.1). И, наконец, для обеспечения упругой деформации в липидном бислое мембран содержится больше ПНЖК – субстратов ПОЛ, чем в цитолемме других клеток. Для контроля интенсивности свободнорадикальных процессов, в цитоплазме эритроцитов активно работает антирадикальная защита.
Если нарушаются условия диссоциации оксигемоглобина (в кармане глобина, где расположен гем, оказываются ионы, молекулы воды), то в этом случае происходит отрыв электрона от двухвалентного железа гема с образованием метгемоглобина и супероксидного анион-радикала. Первое соединение восстанавливается с помощью метгемоглобинредуктазы, а радикал кислорода преобразуется под влиянием супероксиддисмутазы (СОД) в пероксид водорода, который также токсичен для клеток. Поэтому он восстанавливается с первоначально помощью каталазы, позднее глутатионпероксидазы (ГПО) (рис.1) и восстановленного глутатиона. Чтобы поддержать пул последнего, работает глутатионредуктаза (ГР), которая восстанавливает окисленную форму пептида, применяя в качестве восстановителя НАДФН. Необходимую концентрацию этого варианта кофермента получают путем окисления глюкозо-6-фосфата соответствующей дегидрогеназой. В мембранах эритроцитов продуктами свободнорадикальных процессов могут быть липопероксиды (ROOH), которые своевременно удаляются восстановленным глутатионом с участием ГПО:
|
|
|
|  |
ОБМЕН ПОРФИРИНОВ
Порфирины широко распространены в природе. Они обнаружены в нефти, сланцах, глубинных минеральных водах, метеоритах, в образцах лунного грунта. Порфирины входят в состав хлорофилла растений, которые с его помощью улавливают солнечную энергию и осуществляют фотосинтез. В животном мире эти вещества участвуют в образовании гема, который служит простетической группой таких белков, как гемоглобин, миоглобин, каталаза, пероксидазы, цитохромы, триптофан-2,3-диоксигеназа и др.
Основой молекулярной структуры порфиринов является кольцо порфина, которое состоит из 4-х пирролов, соединённых друг с другом метиновыми мостиками (=СН –). При восстановлении последних нарушается целостность сопряжённой системы, соединения становятся бесцветными, преобразуясь в порфириногены. Только они в организме подвергаются обменным превращениям. Порфирины же, лишенные дополнительных атомов водорода, метаболически инертны и выделяются из организма с мочой, желчью и калом.
Хотя способностью синтезировать порфирины обладает каждая клетка (кроме эритроцитов), их наибольшее количество образуется у человека в эритробластах костного мозга и гепатоцитах печени. В костном мозге порфирины, формируя комплексы с ионами железа (гем), утилизируются для образования гемоглобина. Синтезированные в печени порфирины включаются в цитохромы, в первую очередь, в Р450, а также в каталазы, пероксидазы и другие ферменты.
СИНТЕЗ ГЕМА
Исходными метаболитами синтеза гема, который катализирует сложная ферментативная система, служат сукцинил-КоА и глицин (по 8 молекул каждого) (Рис.2). Сукцинил-КоА является продуктом не только ЦТК, но и образуется при распаде треонина, метионина, тимина, высших жирных кислот с нечетным числом атомов углерода.
В ходе альдольной конденсации этих соединений (1) в митохондриях образуется 5-аминолевулиновая кислота(АЛК). Скорость этого процесса контролируется ключевым ферментом – 5-аминолевулинатсинтазой, кофактором которой является пиридоксаль-фосфат. Активность энзима индуцируется сниженным количеством гема.
|

Рис.2. Система ферментов и основные этапы биосинтеза гема.
На втором этапе из молекул АЛК, вышедших в цитоплазму, под влиянием специфической дегидратазы (2) синтезируются 4 молекулы порфобилиногена (ПБГ). В дальнейшем из них формируется тетрапиррольная молекула уропорфириногена (УП-гена). Данный этап катализируется двумя энзимами: ПБГ–дезаминазой и уропорфириноген-косинтетазой (3). В этих условиях обычно образуется УП-ген III. При отсутствии косинтетазы или снижении её активности в значительных количествах получается изомер УП-ген I, который ограничен в своих дальнейших преобразованиях и, как побочный метаболит, выделяется из организма. В норме синтез изомеров 1 типа минимален, однако при некоторых патологических состояниях и генетических нарушениях эти вещества могут накапливаться (4).
Дальнейшие превращения УП-гена III, молекула которого содержит 8 карбоксильных групп, протекают под контролем УП-гендекарбоксилазы (4), осуществляющей последовательное декарбоксилирование соединения до копропорфириногена III (КП-ген). Затем, после возвращения в митохондрии, это соединение подвергается действию системы энзимов: КП-ген- и протопорфириноген-оксидаз (5,6). Под влиянием первого фермента происходит окислительное декарбоксилирование КП-гена III до протопорфириногена IХ (5), окисление которого катализируется вторым энзимом (6). В клетках костного мозга за сутки синтезируется до 30 мг этого соединения, которое комплексируясь с ионами двухвалентного железа (ферроионами), образует гем. Этот этап катализируется феррохелатазой (гемсинтетазой) (7). В дальнейшем, как отмечено выше, гем включается в различные белки – гемопротеиды.
Скорость синтеза гема регулируется следующими факторами:
а) активность АЛК-синтазы лимитирует этот процесс;
б) генез АЛК-синтазы определяется количеством железа;
в) уровень же последнего в клетке зависит от работы рецептора трансферрина.
СТРОЕНИЕ ГЕМОГЛОБИНА
В разные периоды жизни зародыша и ребёнка активно работают различные гены, ответственные за синтез нескольких полипептидных цепей глобина. Выделяют 6 субъединиц: α, β, γ, δ, ε, ζ. Первая и последняя из них включают по 141, а остальные по 146 аминокислотных остатков. Друг от друга они отличаются не только количеством мономеров, но и их составом. Однако принцип образования вторичной структуры у всех цепей однотипен: они все сильно (до 75% длины) спирализованы за счёт водородных связей. Альфа-цепи включают 7, а бета, гамма, дельта – 8 спирализованных фрагментов, чередующихся с аморфными участками. Компактная укладка в пространстве подобного образования приводит к возникновению третичной структуры; причем при этом создаётся карман, куда и вкладывается гем. Возникший комплекс сохраняется с помощью приблизительно 60 гидрофобных взаимодействий между белком и простетической группой. Естественно, что в образовании углубления принимают активное участие гидрофобные аминокислоты (фенилаланин, валин, лейцин). Подобная глобула объединяется с 3 сходными субъединицами, используя для этого бисульфидные мостики и ковалентные взаимодействия (четвертичная структура). Получается белок, составленный из 4 полипептидных цепей (гетерогенный тетрамер), имеющий форму тетраэдра.
В зависимости от характера включённых протомеров различают следующие виды нормальных гемоглобинов (Hb). В первые 20 суток существования эмбриона в ретикулоцитах образуется Hb P (Primitive) в виде двух вариантов: Hb Gower 1, состоящего из дзета- и эпсилон-цепей, соединенных попарно, и Hb Gower 2, в котором дзета-последовательности уже заменены на альфа. Переключение генеза одного вида цепей на другой осуществляется медленно: вначале появляются отдельные клетки, продуцирующие иной вариант. Они дают стимул клонам новых клеток, синтезирующих другой вид полипептида. Позднее эти клетки начинают преобладать и постепенно вытесняют старые.
На 8-й неделе жизни зародыша включается синтез гемоглобина F = α2 γ2 , по мере же приближения акта родов появляются ретикулоциты, содержащие Hb A = α2β2 . На его долю у здорового взрослого человека приходится 96 – 98% от общей массы этого белка. Кроме того, в отдельных эритроцитах присутствуют гемоглобины Hb A2 = α2δ2 (1,5 – 3%) и фетальный (обычно не больше 1%). Однако в некоторых регионах, в том числе и у аборигенов Забайкалья концентрация последнего вида повышается до 4% (в норме).
ФОРМЫ ГЕМОГЛОБИНА
Описаны следующие формы данного гемопротеида.
а) Дезоксигемоглобин – свободная от газов форма протеина.
б) Оксигемоглобин – продукт включения кислорода в молекулу белка:
|
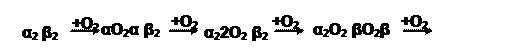
Интересно, что первоначальное связывание кислорода с одной субъединицей ускоряет присоединение последующих молекул (положительный кооперативный эффект). Одна молекула Hb способна удерживать 4 молекулы газа.
Структуры дезокси- и оксиHb несколько отличны. При отсутствии кислорода ферроион в гемоглобине имеет координационное число 5, связан c 4 атомами азота протопорфирина и с третичным атомом азота имидазольного кольца остатка гистидина белковой субъединицы. Шестое координационное место в оксигемоглобине способен занять только молекулярный кислород. Образованию этой связи благоприятствует высокая электронно-донорная способность порфириновой сопряженной системы и имидазола. Структура белка в Hb такова, что она экранирует подход к атому Fe (II) всех других молекул, имеющихся в крови, и своевременно регулирует его донорно-акцепторные свойства.
в) Исключение составляют токсиканты – яды крови, к которым относят и монооксид углерода. Проникая с атмосферным воздухом в лёгкие, СО быстро преодолевает альвеолярно-капиллярную мембрану, растворяется в плазме крови, диффундирует в эритроциты и вступает во взаимодействие с дезоки- и окси-Hb:
|

|
|
|

Образовавшийся карбоксигемоглобин неспособен присоединять к себе кислород, а угарного газа может связывать 4 молекулы.
г) Важным производным Hb является метгемоглобин, в молекуле которого атом железа находится в степени окисления 3+ (в виде ферри-иона). Такая форма гемопротеида образуется при действии на него различных окислителей (оксидов азота, нитробензола, нитроглицерина, хлоратов, метиленового синего и др.), в результате в крови уменьшается количество функционально важного оксиHb, что нарушает доставку кислорода к тканям, вызывая в них развитие гипоксии.
д) Особенности строения концевых аминокислот в цепях глобина позволяют им реагировать с моносахаридами, в первую очередь, с глюкозой. В настоящее время выделяют несколько подвидов Hb A (от 0 до 1c), в которых к валину бета-цепей прикреплены олигосахариды. Особенно легко реагирует последний подвид гемопротеида. У образовавшегося при этом без участия фермента гликозилированного гемоглобина меняется его сродство к кислороду. Это объясняется тем, что присоединившаяся к белку глюкоза занимает место 2,3-ДФГК, что тормозит подкисление среды и тем самым противодействует диссоциации оксигемоглобина. В норме на долю подобной формы Hb приходится не более 5% от его общего количества. При сахарном диабете его концентрация возрастает в 2-3 раза, что благоприятствует возникновению тканевой гипоксии.
СВОЙСТВА ГЕМОГЛОБИНА
Все известные гемопротеиды (см. выше) имеют сходство в строении не только простетической группы, но и апопротеина. У них общий способ укладки полипептидной цепи вокруг гема плюс одинаковые аминокислоты в отдельных участках (инвариантность) разных нитей. В первую очередь, это касается гистидина, глицина (с помощью последнего обеспечивается тесный контакт между спиралями). Определённая общность в строении обусловливает и сходство в функционировании – взаимодействии с газами, в основном с кислородом.
Главное свойство гемоглобина - способность обратимо связывать в лёгких (до 94%) и эффективно отдавать в тканях кислород. На 1г Hb связывается 1,34 мл О2. Сродство гемоглобина к этому газу меньше, чем у других гемопротеидов. Но поистине уникальным для того белка является сочетание прочности связывания кислорода при высоких его парциальных напряжениях и лёгкости диссоциации этой связи в области пониженных давлений. Кроме того скорость распада оксигемоглобина зависит от температуры, pH среды. При накоплении углекислоты, лактата и других кислых продуктов происходит более быстрая отдача кислорода (эффект Бора). Также действует и лихорадка. При алкалозе, гипотермии следует обратное смещение, улучшаются условия насыщения Hb кислородом в лёгких, но полнота отдачи газа в тканях уменьшается. Подобное явление наблюдается при гипервентиляции, замерзании и т.д.
Попадая в условия острой гипоксии, эритроциты активируют гликолиз, что сопровождается увеличением содержания 2,3-ДФГК, которая снижает сродство гемопротеида к кислороду, активирует дезоксигенацию крови в тканях, что носит приспособительный характер. При уменьшении уровня дифосфоглицерата противоположный эффект делает насыщение гемоглобина кислородом в лёгких более активным. Молекула ДФГК, присоединяясь к дезоксиHb в его центральной полости и образуя солевой мостик между двумя бета-цепями, оказывает весьма сильное влияние на сродство белка к кислороду. В физиологических условиях это свойство определяется величинами парциального давления газа в лёгких. При нахождении в высокогорных районах концентрация дифосфоглицерата в эритроцитах возрастает, а сродство гемоглобина к О2 снижается.
Интересно, что фетальный гемоглобин с ДФГК не взаимодействует, сохраняя поэтому повышенное сродство к кислороду и артериальной, и венозной крови.
МЕТАБОЛИЗМ ЖЕЛЕЗА
Большая часть пула железа в организме локализуется в гемопротеидах, в первую очередь в гемоглобине. Поэтому необходимо кратко остановиться на судьбе ионов этого металла в организме. Железо, находясь в пищевых продуктах, может иметь различные формы: восстановленную и окисленную. Наиболее хорошо всасывается последняя в составе гемина из животных продуктов. Отсюда диеты, богатые мясом, сводят вероятность экзогенного железодефицита к минимуму. В растительных, особенно, зерновых продуктах, до 60% ионов переходного металла находится в трудноусвояемой форме, связанной с фитиновой кислотой. Следует заметить, что биодоступность железа невелика: всасывается в кишечнике не более 10% содержащегося в пище, в основном из продуктов животного происхождения. Особую роль при этом играют нормальная секреция соляной кислоты, протеаз, характер питания (способствуют усвоению сукцинат, аскорбиновая кислота), биогенные эффекторы (эритропоэтин из почек стимулирует абсорбцию железа).
В энтероцитах ферроионы связываются с апоферритином с образованием ферритина (Fe2+). Попавшие по vena porta в печень ионы металла включаются в гликопротеид трансферрин, с помощью которого транспортируются к органам и тканям. После взаимодействия со специфическим рецептором ретикулоцита железо высвобождается из трансферрина и попадает в клетку. Иногда этот процесс осуществляется путём пиноцитоза. В эритроидных клетках железо делится между митохондриями, где включается в гем, и белком ферритином, а в миелоидных – его существенная часть попадает в защитный белок – лактоферрин. Если происходит внутрисосудистый гемолиз, то выделившийся при этом гем связывается с гемопексином (это необходимо вследствие прооксидантных свойств данного порфина) и в таком виде транспортируется в печень, где распадается. После чего ионы железа или вновь используются, или откладываются, или выводятся.
Основным депо этого металла служит ферритин, который накапливается в селезёнке, печени, костном мозге, в меньшей степени – в мышечной ткани (одна молекула белка способна удерживать до 4500 атомов Fe2+). Избыточное количество железа может аккумулироваться в печени и других органах в составе гранул гемосидерина – комплекса белков, полисахаридов, включающих до 3% кристаллов металла. Катаболическая фаза обмена ионов железа заключается в их выведении, в основном в составе желчи через желудочно-кишечный тракт (за сутки в среднем взрослый человек теряет его до 1,5 мг).
Нормой для здорового взрослого человека считается содержание железа в крови 12 – 30 мкмоль/л.
ГЛАВА 3. ПАТОЛОГИЯ АНАБОЛИЗМА ГЕМОГЛОБИНА
Так как на долю гемоглобина приходится около 30% массы эритроцита, то естественно, что повреждения в гемопротеиде сказываются на продолжительности жизни и функционировании красных кровяных телец. Отсюда выделяют следующие альтерации эритроцитов:
1) нарушения в синтезе Hb, разделённые на
а) сдвиги в метаболизме железа,
б) изменения в синтезе гема,
в) последствия мутаций в генах, ответственных за образование глобина;
2) дисгемоглобинемии – изменения в балансе различных форм гемопротеидов;
3) повреждения транспорта плазменного гемоглобина.
|
|
|


