 |
Ось гипоталамус-гипофиз-гонады. Мужские половые гормоны. Применение анаболиков в медицине.
|
|
|
|
Гонадотропные гормоны гипофиза, стимулирующие синтез и секрецию половых гормонов Фолликулостимулирующий гормон (ФСГ) и лютеинизирующий гормон (ЛГ) - гонадотропные гормоны гипофиза. Представляют собой гликопротеины с молекулярной массой около 30 кД, состоящие из α- и β-субъединиц. α-Субъединицы содержат 92 аминокислоты и две боковые углеводные цепи и идентичны α-субъединице тиреотропина, β-Субъединицы индивидуальны для каждого гормона.
Регуляция секреции ФСГ и ЛГ. Образование и освобождение обоих гормонов стимулируется гипоталамическим декапеп-тидом - гонадотропин-рилизинг-гормоном, секреция которого происходит эпизодически, что в основном и определяет импульсный характер секреции ЛГ и ФСГ.
У мужчин тестостерон и эстроген, образованный в клетках Лейдига и в процессе метаболизма тестостерона, блокируют по механизму обратной связи синтез и секрецию гонадолиберина и гонадотропных гормонов гипофиза. Кроме этого, клетками гранулёзы фолликулов и клетками Сертоли вырабатывается белок ингибин, который тормозит гипофизарную секрецию ФСГ.
Гонадотропные гормоны ЛГ и ФСГ связываются с рецепторами на мембранах своих клеток-мишеней в яичках, в результате чего происходит активация аденилатциклазной системы. Образующийся цАМФ активирует протеинкиназу, которая фосфорилирует белки, опосредующие эффекты ЛГ и ФСГ. У мужчин ЛГ стимулирует синтез тестостерона интерстициальными клетками Лейдига. ФСГ действуя на клетки Сертоли, запускает процесс сперматогенеза.
Мужские половые гормоны вырабатываются в основном в мужских половых железах - в интерстициальных клетках Лейдига семенников (95%). Небольшое количество андрогенов образуется в коре надпочечников.
|
|
|
Синтез андрогенов Путь биосинтеза андрогенов в яичках и коре надпочечников одинаков. Предшественником андрогенов, как и других стероидных гормонов, служит холестерол, который либо поступает из плазмы в составе ЛПНП, либо синтезируется в самих железах из ацетил-КоА. Отщепление боковой цепи холестерола и образование прегненолона -скорость-лимитирующая реакция. Однако, в отличие от аналогичной реакции, протекающей в надпочечниках, эта стадия стимулируется ЛГ (а не АКТГ). ЛГ, связываясь с рецептором плазматической мембраны клеток Лейдига, активирует аденилатциклазу, увеличивая тем самым внутриклеточную концентрацию цАМФ, что в конечном итоге вызывает активацию фермента, который расщепляет боковую цепь холестерола.
 Тестостерон. Превращение прегненолона в тестостерон катализируется пятью микросо-мальными ферментами и может протекать двумя путями: через образование дегидроэпиандростерона или через образование прогестерона (что, по-видимому, преобладает в семенниках человека).
Тестостерон. Превращение прегненолона в тестостерон катализируется пятью микросо-мальными ферментами и может протекать двумя путями: через образование дегидроэпиандростерона или через образование прогестерона (что, по-видимому, преобладает в семенниках человека).
Суточная секреция тестостерона у мужчин составляет в норме примерно 5 мг и сохраняется на протяжении всей жизни организма. Гормон циркулирует в крови в связанном с белками плазмы состоянии: альбумином (40%) и специфически связывающим половые гормоны р-глобулином (называемым секс-гормонсвязывающим глобулином, СГСГ). Лишь 2% от общего количества гормона в крови транспортируется в свободном виде, и именно такие молекулы проявляют биологическую активность. Дигидротестостерон. В семенных канальцах, предстательной железе, коже, наружных половых органах тестостерон служит предшественником более активного адцрогена - дигидротестостерона (рис. 11-41, 11-42). Это превращение, в котором участвует примерно 4% тестостерона, происходит в результате восстановления двойной связи кольца А и 3-кетогруппы при участии цитоплазматического фермента - NADPH-зависимой 5α-редуктазы. Семенники человека секретируют в сутки до 50-100 мкг дигидротестостерона. Однако большее количество гормона - следствие периферических превращений, и суммарная сугочная секреция дигидротестостерона составляет 400 мкг, что почти в 10 раз меньше уровня секреции тестостерона.
|
|
|
В некоторых периферических тканях небольшое количество тестостерона превращается в эстрадиол. В качестве побочных продуктов клетки Лейдига также постоянно секретируют эстрадиол и прогестерон, хотя роль этих гормонов в развитии и поддержании функций размножения и формирования полового поведения у мужчин до настоящего времени не выяснена.
Регуляция синтеза и секреции андрогенов. В препубертатный период секреция андрогенов подавляет по механизму отрицательной обратной связи секрецию гонадотропина до начала пубертатного периода, когда гипофизарные клетки становятся менее чувствительными к ингибирующему действию циркулирующих в крови андрогенов. Эта потеря чувствительности приводит к циклически импульсному освобождению ЛГ и ФСГ. ЛГ, связьюаясь с рецепторами клеток Лейдига, стимулирует образование тестостерона интерстициальными клетками Лейдига, а ФСГ, связываясь с рецепторами клеток Сертоли в семенниках, стимулирует сперматогенез. Тестостерон замыкает отрицательную обратную связь на уровне гипофиза и гипоталамуса, уменьшая частоту секреторных импульсов ЛГ. Торможение секреции ФСГ аденогипофизом происходит под действием белка ингибина, вырабатываемого клетками Сертоли. ФСГ стимулирует синтез этого белка, который по механизму отрицательной обратной связи тормозит дальнейшую секрецию ФСГ.
Мишени для андрогенов. К мишеням тестостерона относят эмбриональные вольфовы структуры, сперматогонии, мышцы, кости, почки, мозг. Подобно другим стероидным гормонам, андрогены образуют внутри клетки комплекс с рецептором, который связывается с определённым участком хроматина, активируя специфические гены, белковые продукты которых опосредуют биологические эффекты андрогенов. Эффекты андрогенов. Физиологическое действие андрогенов различно в разные периоды жизни организма. У эмбриона под действием андрогенов из вольфова протока образуются придаток яичка (эпидидимис), семявыносящий проток и семенной пузырёк. У плода мужского пола происходит маскулинизация мозга. Поскольку андрогены в организме обладают мощным анаболическим действием и стимулируют клеточное деление, повышенный уровень андрогенов в препубертатный период приводит к скачкообразному увеличению линейных размеров тела, увеличению скелетных мышц, росту костей, но одновременно способствуют и остановке роста, так как стимулируют сращение эпифизов длинных костей с их стволами. Андрогены вызывают изменение структуры кожи и волос, снижение тембра голоса вследствие утолщения голосовых связок и увеличения объёма гортани, стимулируют секрецию сальных желёз.
|
|
|
В медицине анаболики применяют в тех случаях, когда пациенту требуется восстановление после серьезных затяжных заболеваний, например, онкологии.
В спорте же основная роль стероидов направлена на получение высоких результатов, которых невозможно добиться без медикаментозного вмешательства, дозы анаболиков при этом в несколько раз выше доз, используемых при лечении больных.
Пути передачи гормонального сигнала: рецепторный и пострецепторный. Мессенджеры второго порядка ц-АМФ, ц-ГМФ, инозитол-3-фосфат, диацилглицерол, кальций-кальмодулин. NО – как модулятор образования вторичных мессенджеров.
По механизму действия гормоны можно разделить на 2 группы. К первой группе относят гормоны, взаимодействующие с мембранными рецепторами (пептидные гормоны, адреналин, а также гормоны местного действия - цитокины, эйкозаноиды). Вторая группа включает гормоны, взаимодействующие с внутриклеточными рецепторами. Связывание гормона (первичного посредника) с рецептором приводит к изменению кон-формации рецептора. Это изменение улавливается другими макромолекулами, т.е. связывание гормона с рецептором приводит к сопряжению одних молекул с другими (трансдукция сигнала). Таким образом, генерируется сигнал, который регулирует клеточный ответ путём изменения активности или количества ферментов и других белков. В зависимости от способа передачи гормонального сигнала в клетках меняется скорость реакций метаболизма: 1. в результате изменения активности ферментов; 2 в результате изменения количества ферментов
|
|
|
1.Передача гормональных сигналов через мембранные рецепторы. Гормоны (первичные посредники), связываясь с рецепторами на поверхности клеточной мембраны, образуют комплекс гормон-рецептор, который трансформирует сигнал первичного посредника в изменение концентрации особых молекул внутри клетки - вторичных посредников. Вторичными посредниками могут быть следующие молекулы: цАМФ, цГМФ, ИФ3 (инозитолфосфат), ДАГ (диацилглицерол), Са2+, NO.
Гормоны, взаимодействие которых с рецептором клетки-мишени приводит к образованию цАМФ, действуют через трёхкомпонентную систему, которая включает белок-рецептор, G-белок и фермент аденилатциклазу. Образующийся под действием аденилатциклазы цАМФ активирует протеинкиназу А, фосфорилируюшую ферменты и другие белки (см. раздел 5). Известно более 200 различных G-белков, в структуре которых обнаружены 3 субъединицы α, β и γ (см. раздел 5). В отсутствие гормона α-субъединица G-белка связана с ГДФ. Образование комплекса гормонрецептора приводит к конформационным изменениям α-субъединицы, замене ГДФ на ГТФ и отщеплению димера βγ от α-ГТФ. В случае рецепторов, сопряжённых с Gs-белком, субъединица αs-ГТФ активирует аденилатциклазу.
В случае рецепторов, сопряжённых с Giбелком, субъединица αi-ГТФ ингибирует аденилатциклазу. Другая система, генерирующая цГМФ как вторичный посредник, сопряжена с гуанилатциклазой. Цитоплазматический домен такого типа рецепторов обладает активностью гуанилатциклазы, которая катализирует реакцию образования цГМФ из ГТФ> (подобно аденилатциклазе). Молекулы цГМФ могут активировать ионные каналы либо активировать цГМФ-за-висимую протеинкиназу G, участвующую в фосфорилировании других белков в клетке. Например, фосфодиэстерааа, которая гидролизует цАМФ до АМФ, активируется в результате фосфорилирования цГМФ-зависимой протеинкиназой. Некоторые гормоны (например, вазопрессин или адреналин), образуя комплекс с соответствующими рецепторами (рецептор V1 для вазопрессина и αi-рецептор для адреналина), через активацию соответствующих G-белков активируют фосфолипазу С, в результате чего в клетке появляются вторичные посредники ИФ3, ДАГ. Молекула ИФ3 стимулирует высвобождение Са2+ из ЭР. Кальций связывается с белком кальмодулином. Этот комплекс активирует Са2+-кальмодулинзависимую протеинкиназу. Ионы кальция и ДАГ участвуют в активации протеинкиназы С
|
|
|
Сигнальной молекулой в клетке может служить также оксид азота NO, образующийся в организме из аргинина при участии фермента NO-синтазы, присутствующего в нервной ткани, эндотелии сосудов, тромбоцитах и других тканях. Молекула NO может быстро диффундировать через мембрану эндотелиальныхклеток, где она синтезируется, в соседние клетки. В клетках-мишенях, например, эндотелиальных клетках NO взаимодействует с входящим в активный центр гуанилатциклазы ионом железа, способствуя тем самым быстрому образованию цГМФ. Увеличение концентрации цГМФ в клетках гладких мышц вызывает активацию киназ, что в конечном итоге приводит к расслаблению ГМК сосудов и последующему их расширению. Механизм действия оксида азота объясняет использование нитроглицерина в качестве лекарственного препарата для снятия острых болей в сердце, поскольку нитроглицерин - источник образующихся молекул NO, которые и вызывают расслабление кровеносных сосудов и увеличение притока крови в миокард.
2. Передача сигналов через внутриклеточные рецепторы. Стероидные и тиреоидные гормоны связываются с рецепторами внутри клетки и регулируют скорость транскрипции специфических генов. В отсутствие гормона внутриклеточные рецепторы связаны обычно с другими белками в цитозоле или ядре. Рецепторы тиреоидных гормонов всегда связаны с ДНК. В отсутствие гормонов соответствующие рецепторы ингибируют экспрессию генов. Напротив, взаимодействие с гормоном превращает их в активаторы транскрипции.
3.Передача сигналов через рецепторы,сопряжённые с ионными каналами. Рецепторы, сопряжённые с ионными каналами, являются интегральными мембранными белками, состоящими из нескольких субъединиц. Они действуют одновременно как ионные каналы и как рецепторы, которые способны специфически связывать с внешней стороны эффектор, изменяющий их ионную проводимость. Эффекторами такого типа могут быть гормоны и нейромедиаторы.
82. Гормоновитамин А, структура, суточная потребность проявления авитаминоза и гипервитаминоза, биологические функции.
Ретинол. Структура. жирорастворимые витамины; циклический,ненасыщенный,одноатомный спирт.Сод-ся в животных продуктах: печень крупного рогатого скота,яичном желтке,молочных продуктах,рыбьем жире. Суточная потребность 1-2 мг; Участвует в акте зрения регулирует рост и дифференцировку клеток. Авитаминоз: куриная слепота, кератоз эпителиальных клеток, ксерофтальмия. гиперавитаминоз - встречается как в острой, так и в хронической формах. Острая интоксикация витамином А возникает в том случае, когда в рационе питания содержится большое количество печени морских животных, рыб и моллю-сков. Некоторые из указанных продуктов являются высокоактивными концентратами витамина А.Симптомы острого гипервитаминоза А: жесточайшие головные боли, рвота, брадикардия, нарушение зрения, кожные высыпания, напоминающие сыпь при скарлатине; через 6—7 ч начинается крупнопластинчатое шелушение, поднимается температура, появляются вялость, апатия, у детей повышается внутричерепное давление (грибовидное выпячивание родничка, гидроцефалия), поднадкостничные гематомы, особенно в области эпифизов. Резко снижается количество фибриногена. Симптомы острой интоксикации витамином А проходят через неделю. Биологич.роль. Оказывает многообразное влияние на жизнедеятельность организма. Играет важную роль в окислительно-восстановительных процессах (вследствие большого количества ненасыщенных связей), участвует в синтезе мукополисахаридов, белков, липидов. Ретинолу принадлежит важная роль в поддержании нормального состояния кожи и эпителия слизистых оболочек, обеспечении нормальной дифференциации эпителиальной ткани, в процессах фоторецепции (способствует адаптации человека к темноте). Ретинол участвует в минеральном обмене, процессах образования холестерина, усиливает выработку липазы и трипсина, усиливает миелопоэз, процессы клеточного деления. Местное действие опосредовано наличием на поверхности клеток эпителия специфических ретинолсвязывающих рецепторов. Тормозит процессы кератинизации, усиливает пролиферацию эпителиоцитов, омолаживает клеточные популяции и уменьшает количество клеток, которые идут по пути терминальной дифференцировки.




83. Гомоновитамин Д, его роль в регуляции обмена кальция и фосфатов. Суточная потребность. Авитаминоз
Д, его проявления. Понятие о гипервитаминозе Д
Витамин D (кальциферол) - жирорастворимый витамин, антирахитический фактор.. В коже содержится неактивный
предшественник витамина (вещество, превращающееся в организме в активный витамин), на который и действуют ультрафиолетовые лучи солнечного света.Сегодня витамином D называют два витамина - D 2 и D 3 - эргокальциферол и холекальциферол - это кристаллы без цвета и запаха, устойчивые в воздействию высоких температур. Эти витамины являются жирорастворимыми, т.е. растворяются в жирах и органических соединениях и нерастворимы в воде. Биологическая роль витамина D. Витамин D способствует правильному росту костей, предохраняет детей от развития рахита, ускоряет процессы заживления костной ткани при ее повреждениях..Витамин D является главным звеном гормональной регуляции обмена кальция и фосфора: Увеличивает проницаемость плазматической мембраны энтероцитов для кальция и активный транспорт его в митохондрии. Индуцирует синтез белка-переносчика для выкачивания кальция из энтероцитов в кровь. Стимулирует абсорбцию фосфора в кишечнике, отложение солей кальция во вновь сформированном остеоидном матриксе. Способствует дифференцировке моноцитов и макрофагов в остеокласты.Снижает синтез остеобластами коллагена I типа, способствуя резорбции избытка неминерализованного остеоида. Усиливает реабсорбцию кальция в дистальных извитых канальцах почек. Рекомендуемое ежедневное потребление этого витамина для детей до пяти лет составляет 10 мкг, а для детей после пяти лет - 2,5 мкг. Потребность в витамине D взрослых составляет 2,5 мкг/сут. При авитаминозе D понижается всасывание кальция и освобождение его из кости, что ведет к стимуляции выработки паратгормона паращитовидными железами. Развивается вторичный гиперпаратиреоз, который способствует вымыванию кальция из костей и потере фосфата с мочой. Клиническим проявлением этих процессов является рахит.При неправильном применении препаратов витамина D может развиться гипервитаминоз, при котором происходит усиленная мобилизация кальция из костной ткани и метастатическая кальцификация органов и тканей (почек, сердца, кровеносных сосудов, печени, легких) с нарушением их функции. У маленьких детей избыток витамина D может вызвать синдром, относимый врачами к типу "провала процветания", который включает слабый рост и плохое развитие, маленькое увеличение веса, раздражительность и плохой аппетит.Ранними признаками передозировки витамина являются тошнота, головная боль, потеря аппетита и массы тела, полиурия, жажда, полидипсия, запоры, гипертензия, мышечная ригидность. Смертельные исходы обусловлены почечной недостаточностью, сдавлением мозга, ацидозом и гиперкальциемическитми аритмиями. Следствием длительной передозировки витамина D в рационе является гиперкальциемия (высокое содержание кальция в сыворотке). Симптомы гиперкальциемии могут варьировать от раздражительности до спазмов мышц и сильной судорожной активности. Долговременная гиперкальциемия приводит к кальцификации тканей (откладывания кальция в тканях почек, легких, артериях). 
Ось гипоталамус-гипофиз-кора надпочечников. Гормоны коры надпочечников: биосинтез и катаболизм. Регуляция секреции, механизм действия, влияние на обмен веществ. Применение глюкокортикоидов в медицине. Изменения метаболизма при гипо- и гиперфункции коры надпочечников. Синдром Иценко-Кушинга.
Ось гипоталамус - гипофиз - надпочечники формирует реакцию на стресс. Центральная часть головного мозга выпускает соединение кортикотропином,Затем кортикотропин поступает в гипофиз, где вызывает выпуск гормона, адренокортикотропина. Данный гормон поступает в кровоток и заставляет кору надпочечника выпускать гормоны стресса, особенно кортизол, который является гормоном кортикостероидом. Кортизол увеличивает приток веществ, которые необходимы, чтобы отреагировать на стрессВ коре надпочечников синтезируется более 40 различных стероидов, различающихся по структуре и биологической активности. Кортикостероиды в зависимости от их преобладающего действия делят на 3 основные класса: глюкокортикоиды, минералокортикоиды и андрогены.
Глюкокортикоиды, играют важную роль в адаптации к стрессу. Они оказывают разнообразные эффекты, но наиболее важный - стимуляция глюконеогенеза (кортизол). Минералокортикоиды, С21-стероиды, необходимы для поддержания уровня Na+ и К+- альдостерон. Андрогены. В коре надпочечников образуются предшественники андрогенов, из которых наиболее активный - дегидроэпиандростерон (ДЭА) и слабый - андростендион. Самый мощный андроген надпочечников тестостерон синтезируется в надпочечниках в небольшом количестве. Эти стероиды превращаются в более активные андрогены вне надпочечников.
Тестостерон в незначительных количествах может превращаться в надпочечниках в эстрадиол. Но в норме продукция этих гормонов надпочечниками не играет существенной роли.
СИНТЕЗ: Общим предшественником кортикостероидов служит холестерол. В митохондриях холестерол превращается в прегненолон при участии гидроксилазы, относящейся к группе цитохромов Р450. Цитохром Р450, отщепляющий боковую цепь, локализован во внутренней мембране митохондрий.
Дальнейшее превращение прегненолона происходит под действием различных гидроксилаз с участием молекулярного кислорода и NADPH, а также дегидрогеназ, изомераз и лиаз. В коре надпочечников различают 3 типа клеток, образующих 3 слоя, или зоны: клубочковую, пучковую и сетчатую. ферменты, необходимые для синтеза альдостерона, присутствуют только в клетках клубочковой зоны, а ферменты синтеза глюкокортикоидов и андрогенов локализованы в пучковой и сетчатой зонах Катаболизм гормонов коры надпочечников происходит в печени. Здесь протекают реакции гидроксилирования, окисления и восстановления гормонов. Продукты катаболизма кортикостеровдов (кроме кортикостерона и альдостерона) выводятся с мочой в форме 17-кетостероидов, образующихся в результате отщепления боковой цепи
Эффекты: Кортизол стимулирует образование глюкозы в печени, усиливая глюконеогенез и одновременно увеличивая скорость освобождения аминокислот, индуцирует синтез ферментов катаболизма аминокислот (аланинаминотрансферазы, трипто-фанпирролазы и тирозинаминотрансферазы и ключевого фермента глюконеогенеза - фосфо-енолпируваткарбоксикиназы). Избыточное количество кортизола стимулирует липолиз в конечностях и липогенез в других частях тела (лицо и туловище). Влияние глюкокортикоидов на обмен белков и нуклеиновых кислот проявляется двояко: в печени кортизол в основном оказывает анаболический эффект (стимулирует синтез белков и нуклеиновых кислот). В мышцах, лимфоидной и жировой ткани, коже и костях кортизол тормозит синтез белков, РНК и ДНК и стимулирует распад РНК и белков. При высокой концентрации глюкокортикоиды подавляют иммунные реакции, вызывая гибель лимфоцитов и инволюцию лимфоидной ткани; подавляют воспалительную реакциюВысокая концентрация глюкокортикоидов вызывает торможение роста и деления фибро-бластов, а также синтез коллагена и фибронектина. Для гиперсекреции глюкокортикоидов типичны истончение кожи, плохое заживление ран, мышечная слабость и атрофия мышц. Глюкокортикоиды участвуют в физиологическом ответе на стресс, связанный с травмой, инфекцией или хирургическим вмешательством. Минералокортикоиды стимулируют реабсорбцию Na+ в дистальных извитых канальцах и собирательных трубочках почек. Кроме того, они способствуют секреции К+, NH4+ в почках, а также в других эпителиальных тканях. Заболевания коры надпочечников могут проявиться симптомами как гипо-, так и гиперпродукции гормонов. Большинство клинических проявлений надпочечниковой недостаточности обусловлено дефицитом глюкокортикоидов и минералокортикоидов. Острая надпочечниковая недостаточность - проявляется сосудистым коллапсом, резкой адинамией, потерей сознания. Такое состояние возникает вследствие нарушения обмена электролитов, которое приводит к потере ионов Na+ и Сl- с мочой, обезвоживанию за счёт потери внеклеточной жидкости, повышению уровня К+ в сыворотке крови, в межклеточной жидкости и клетках, в результате чего может нарушаться сократительная способность миокарда. Изменение углеводного обмена проявляется в снижении уровня сахара в крови, уменьшении запаса гликогена в печени и скелетных мышцах. Первичная недостаточность надпочечников (болезнь Аддисона) развивается в результате поражения коры надпочечников туберкулёзным или аутоиммунным процессом. Основные клинические проявления выражаются в снижении массы тела, общей слабости, снижении аппетита, тошноте, рвоте, снижении АД и типичной для первичной надпочечниковой недостаточности гиперпигментацйи кожи ("бронзовая болезнь"). Причина гиперпигментации - повышение продукции ПОМК - предшественника АКТГ и меланоцитстимулирующего гормона.Вторичная недостаточность надпочечников может развиться при дефиците АКТГ, что, в свою очередь, может быть следствием опухоли или инфекционного поражения гипофиза.
Гиперпродукция глюкокортикоидов (гиперкортипизм) Причина: может быть следствием повышения уровня АКТГ при опухолях гипофиза
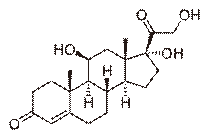
(болезньИценко-Кушинга) и опухолях других клеток (бронхов, тимуса, поджелудочной железы), вырабатывающих кортикотропинподобные вещества, или избыточного синтеза кортизола при гормонально-активных опухолях коры надпочечников (синдром Иценко-Кушинга). Основные проявления: гипергликемия и снижение толерантности к глюкозе, обусловленные стимуляцией глюконеогенеза («стероидный диабет»), усиление катаболизма белков, уменьшение мышечной массы, истончение кожи, остеопороз, инволюция лимфоидной ткани. Характерно своеобразное перераспределение отложений жира («лунообразное лицо», выступающий живот). Гипернатриемия, гипертензия, гипокалиемия обусловлены некоторой минералокортикоидной активностью кортизола, которая проявляется при его избытке. (На картинке кортизол)

Применение глюкокортикоидов в медицине. наиболее широкое распространение они получили в терапевтической клинике, причем назначаются на длительное время (иногда годами). Это способствовало формированию контингента стероидозависимых больных. Этот контингент состоит в основном из больных ревматического круга заболеваний (ревматоидный артрит, системная красная волчанка, склеродермия и др.); хроническими заболеваниями легких (бронхиальная астма); аутоиммунными заболеваниями системы крови (тромбоцитопения, гипо- и апластическая анемия); хроническими заболеваниями почек и печени; группа больных с патологией кожи и др. У больных с перечисленными выше заболеваниями понижена общая сопротивляемость, реактивность организма, имеется склонность к осложнениям со стороны желудочно-кишечного тракта (стероидные язвы, кровотечения), сердечно-сосудистой системы (артериальная гипертония), эндокринного аппарата (стероидный диабет, атрофия надпочечников), нервной системы (эйфория, психозы и др.), водно-болевого обмена (задержка жидкости и натрия в организме). Глюкокортикоиды обладают выраженным катаболическим действием, подавляют иммунитет и способствуют возникновению различных осложнений, особенно приострых инфекциях, травмах, во время и после оперативных вмешательств и т. д. У лиц, получавших в прошлом длительное время глюкокортикоиды или принимающих их в настоящее время, наблюдается нарушение заживления раны, послеоперационный период протекает, обычно вяло, длится дольше.
|
|
|


