 |
Классификация О.А. Алекина
|
|
|
|
Классификация О.А. Алекина (рисунок 8) сочетает принцип деления подземных вод по преобладающим ионам и по соотношению между ними. По преобладающему аниону О.А. Алекиным /4/ выделяются три класса вод: гидрокарбонатная, сульфатная и хлоридная. По ведущему катиону различают группы кальциевых, магниевых и натриевых вод. Соотношение ионов позволяет установить различные типы вод. При выделении которых содержание ионов выражается в молярной форме (r)
1 тип r  > r Ca2+ + r Mg2+ (гидрокарбонатный натриевый),
> r Ca2+ + r Mg2+ (гидрокарбонатный натриевый),
2 тип r  < r Ca2+ + r Mg2+ (сульфатный натриевый),
< r Ca2+ + r Mg2+ (сульфатный натриевый),
3 тип r  +
+ 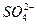 < r Ca2+ + r Mg2+ или r Сl- >r Na+
< r Ca2+ + r Mg2+ или r Сl- >r Na+
4 тип r  +
+ 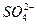 =0
=0
3 тип подразделяется: 3а rCl- < r Na++ r Mg2+ (хлормагниевый),
3б rCl- < r Na++ r Mg2+(хлоркальциевый).

Рисунок 8 Классификация природных вод по О.А. Алекину
Типы гидрокарбонатных: Ca - I,II,III; Mg – I,II,III; Na – I,II,III
Типы сульфатных: Ca - IV,II,III; Mg – IV,II,III; Na – I,II,III
Типы хлоридных: Ca - IV,II,III; Mg – IV,II,III; Na – I,II,III
Эти гидрохимические оценки можно записать и в более сжатой форме. Если классы вод обозначить условными индексами (С-гидрокарбонатные воды, S-сульфатные, Cl-хлоридные), а типы римскими выделить символами ведущих катионов (Ca,Mg, Na), а типы римскими цифрами (I-IV), то химическая характеристика вод указанного состава запишется так:  .
.
Эту краткую форму записи следует использовать, указывая класс воды по Алекину в таблице результатов химических анализов природных вод (таблица 5).
Формула М.Г. Курлова
При массовых определениях химического состава природных вод возникает необходимость обобщения, полученных результатов и изображения анализов воды в виде кратких формул, допускающих обзор и интерпретацию аналитического материала. Формула Курлова представляет собой псевдо-дробь, в числителе которой в порядке убывающего содержания записываются анионы, а в знаменателе катионы, выраженные в процентах (дробные величины процентов округляются до целых чисел). Слева от полученной «простой дроби» указывается содержание растворенных газов в мг/ дм3 и величина минерализации воды в г/ дм3, справа от нее температура воды и дебит скважины в м3 /сутки. Образец записи результатов анализа в виде формулы Курлова приводится ниже
|
|
|
 .
.
Наименование водам дается по преобладающим (свыше 20% моль) анионам и катионам в порядке их возрастания (приведенный анализ читается – вода сульфатно-хлоридно-карбонатная, магниево-кальциевая).
Пересчет из ионной формы в солевую
Пересчет из ионной формы в солевую производится по правилу фрезенуса в соответствии с растворимостью солей. В первую очередь комбинируются малорастворимые, а затем более растворимые. Общая схема связывания следующая. Ионы Ca2+ связываются последовательно с 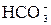 ,
,  , CI в зависимости от его содержания в процентах. В такой же последовательности связываются ионы Mg2+ и Na+. Пересчет в солевую форму имеет важное значение при оценке питьевых, лечебных, технических и др. качеств воды, т.к. полезно принять во внимание не только абсолютное содержание ионов но и предполагаемые ассоциации анионов с катионами (соли).
, CI в зависимости от его содержания в процентах. В такой же последовательности связываются ионы Mg2+ и Na+. Пересчет в солевую форму имеет важное значение при оценке питьевых, лечебных, технических и др. качеств воды, т.к. полезно принять во внимание не только абсолютное содержание ионов но и предполагаемые ассоциации анионов с катионами (соли).
Графические методы изображения результатов анализов воды
Для обобщения аналитического материала и его большей наглядности используются различные типы графиков:
1 Графики, изображающие результаты большего числа анализов (треугольники анионо-катионного состава и квадрат Н.И. Толстихина).
2 Графики, отражающие химический состав отдельных проб воды (колонки-диаграммы, циклограммы Н.И. Толстихина).
3 Графики, характеризующие изменение химического состава вод в определённом направлении (гидрохимический профиль А.А. Бродского).
|
|
|
|
|
|


