 |
Технологическая схема умягчения воды из подземного источника.
|
|
|
|
Состав сооружений технологической схемы реагентного умягчения зависит от того, какие сопутствующие процессы водоподготовки необходимо реализовать параллельно с умягчением. Как правило, если умягчается вода поверхностных источников водоснабжения параллельно требуется ее осветление и обесцвечивание, в то время, как для воды из подземных источников водоснабжения или для воды, забираемой из хозяйственно-питьевого водопровода осветление и обесцвечивание не требуется. Поэтому различают технологические схемы реагентного умягчения воды поверхностных источников и воды подземных источников.
В таких технологических схемах основным сооружением, в котором реализуется процесс реагентного умягчения является вихревой реактор. Кроме того, схема включает напорный осветлительный фильтр и блок реагентного хозяйства. Сам вихревой реактор представляет собой напорный аппарат конусной формы, загружаемый контактной массой (мелкозернистый кварцевый песок или мраморная крошка крупностью d=0,25 мм или каменно-угольной пылью). Объем загрузки составляет 1 кг на 1 м3 объема вихревого реактора. Исходная концентрация магния в воде не более 15 мг/л. Вода подается в нижнюю часть реактора. В самом реакторе высокие скорости подъема воды и поэтому вода приобретает вихреобразное движение.

1 – вихревой реактор; 2 – напорный фильтр; 3 – РЧВ; 4 – насос, подающий промывную воду; 5 – насос подачи воды в систему технического водоснабжения.
Сами взвешенные частицы контактной массы являются центрами кристаллизации. На этих взвешенных частицах образуется осадок СаСО3. Он как бы обволакивает частицы контактной массы. Зерна контактной массы увеличивается в массе и объеме и при размере 1,5-2 мм перестают поддерживаться во взвешенном состоянии. В этом случае контактную массу выпускают и загружают новую (в среднем через 3-4 дня). В виде осадка СаСО3↓ удаляется кальциевая жесткость. Этот осадок, почти чистый карбонат кальция с влажностью 10%. Он используется как сырье для получения извести. А осадок Mg(ОН)2↓, в виде которого удаляется магниевая жесткость, не способен кристаллизоваться и задерживаться в загрузке напорного фильтра.
|
|
|
Регламент проектирования вихревого реактора:
1)скорость входа 0,8-1 мм/с;
2)скорость выхода из него 4-6 мм/с;
3) продолжительность пребывания воды в нем 15-20 мин.
Область применения различных методов умягчения.
| Наименование метода | Характеристика процесса | Назначение метода | Условия эффективного применения | |||
| Мутность исходной воды, мг/л | Жесткость исходной воды, мг-экв/л | Остаточная жесткость, мг-экв/л | Температура воды, °С | |||
| Термический | Воду нагревают до температуры более 100°С, при этом удаляется карбонатная и некарбонатная жесткости | Устранение Жк и Жнк из исходной воды, используемой для питания котлов низкого и среднего давления | До 50 | Жк с преобладанием Са(НСО3)2; Жнк в виде гипса(любое значение) | Жк до 0,035 Жнк в виде СаSO4 до 0,7 | До 270 |
| Реагентный | В воду добавляют реагенты, которые связывают Са2+ и Мg2+ в малорастворимые соединения | Неглубокое умягчение при одновременном осветлении воды от взвешенных веществ | До 500 | Жобщ до 5-30 | Жобщ до 0,7 | До 90 |
| Ионный обмен | Умягчаемая вода пропускается через катионитовый фильтр (набухший катионит в форме Н-kat, Na-kat, NH4-kat. | Глубокое умягчение воды, содержащей небольшое количество взвешенных веществ | Не более 5-8 | Жобщ до 15 | Жобщ 0,1-0,2 – при одноступенчатой схеме; Жобщ 0,01-0,05 при двухступенчатой схеме | До 30, если загрузка глауконит, До 60, если сульфоуголь |
| Электролиз | Исходная вода фильтруется через полупроницаемые мембраны | Глубокое умягчение воды | До 2 | Жобщ до 10 | Жобщ -0,01 и ниже | До 60 |
9. Основы процесса умягчения ионным обменом
|
|
|
Сущность ионного обмена основана на способности некоторых, практически не растворимых в воде веществ, называемых катионитами, обменивать содержащиеся в них активные группы катионов на катионы (Ca2+) и (Mg2+) при фильтровании умягчаемой воды через слой загрузки катионита. В процессе умягчения катионированием, активная группа, содержащаяся в катионите путём проведения регенерации катионита может представлять Na-катиониты или H-катиониты.
Раствор, который используется для регенерации Na- катионита: NaCl, а при Н-катионировании, регенерационным раствором является H2SO4.
Химизм процесса Na-катионирования:
2Na [  ]+
]+  (1)
(1)
2Na [  ]+
]+  (2)
(2)
2Na [  ]+
]+ 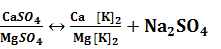 (3)
(3)
Процесс Водород-катионирования:
H [  ]+
]+  (4)
(4)
2H [  ]+
]+  (5)
(5)
H [  ]+
]+  (6)
(6)
При фильтровании воды через Na-кат в процессе снижения жёсткости (удаляется  ) повышается щёлочность фильтрата эквивалентно карбонатной жёсткости (уравнение 1).
) повышается щёлочность фильтрата эквивалентно карбонатной жёсткости (уравнение 1).
При фильтровании воды через Н-кат повышается кислотность фильтрата эквивалентно некарбонатной жёсткости и одновременно вода насыщается свободной углекислотой СО2 (уравнения 4,5,6).
10. Катиониты и их свойства.
Катионообменные материалы могут быть органического или минерального происхождения, естественного или искусственного происхождения. В основном в практике водоподготовки применяют катиониты органического и искусственного происхождения, такие как: сульфоуголь (чёрные зёрна неправильной формы d 0,25-0,7мм, сорт СК-1); катионит КУ-2 (зёрна желтоватого цвета, получают из стирола, бензола, d 0,3-1,5 мм); Анберлайт-50; Зеролит 325, Пьюрлайт –с100,-с100Е,с145;
Качества катионитов характеризуются физическими свойствами (фракционный состав, механическая прочность, химическая стойкость, термическая стойкость и обменная способность)
Характеризуются катиониты полной и рабочей обменной способностью.
Полная обменная способность катионита [Е полн.]-это количество грамм-эквив.  и
и  , кот.Может содержать 1 м3 катионита, находящегося в рабочем состоянии до того момента, когда жёсткость фильтрата сравняется с жёсткостью исходной воды.
, кот.Может содержать 1 м3 катионита, находящегося в рабочем состоянии до того момента, когда жёсткость фильтрата сравняется с жёсткостью исходной воды.
Рабочая обменная способность [Е раб.]-это количество грамм-экв.  и
и  , кот. Задерживает 1м3 катионита до момента проскока в фильтрат некоторой жёсткости, превышающей норму.
, кот. Задерживает 1м3 катионита до момента проскока в фильтрат некоторой жёсткости, превышающей норму.
|
|
|
Ераб<Е полн.
Отношение обменной способности ко всему объёму катионита, загруженного в фильтр, называют ёмкостью поглощения катионита.
Существуют сильнокислотные катиониты, способные к обмену катионов в нейтральной, кислой, и щелочной средах. Существуют слабокислотные катиониты, способные к обмену катионитов при рН>7. (При рН<7 обменная способность слабокислотных катионитов очень мала.)
Катиониты характеризуются активной группой или типом матрицы, насыпной массой продукта, размером зёрен и полной обменной ёмкостью.
|
|
|


