 |
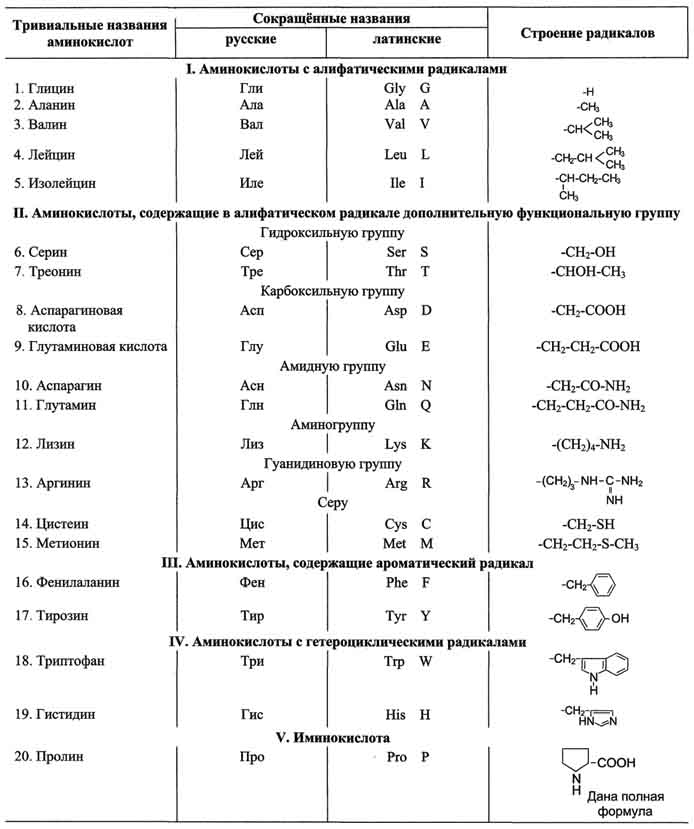
Таблица 1. Классификация основных аминокислот белков по их химическому строению
|
|
|
|
Таблица 1. Классификация основных аминокислот белков по их химическому строению
Денатурация. Синтезированная молекула белка, складываясь, приобретает свойственную ей конфигурацию. Эта конфигурация, однако, может разрушиться при нагревании, при изменении рН, под действием органических растворителей и даже при простом взбалтывании раствора до появления на его поверхности пузырьков. Измененный таким образом белок называют денатурированным; он утрачивает свою биологическую активность и обычно становится нерастворимым. Хорошо знакомые всем примеры денатурированного белка – вареные яйца или взбитые сливки. Небольшие белки, содержащие всего лишь около сотни аминокислот, способны ренатурировать, т. е. вновь приобретать исходную конфигурацию. Но большинство белков превращается при этом просто в массу спутанных полипептидных цепей и прежнюю конфигурацию не восстанавливает.
Качественные реакции на аминокислоты и белок:
1) Все аминокислоты окисляются нингидрином с образованием продуктов, окрашенных в сине-фиолетовый цвет. Иминокислота пролин дает с нингидрином желтое окрашивание.
2) При нагревании ароматических аминокислот с концентрированной азотной кислотой происходит нитрование бензольного кольца и образуются соединения, окрашенные в желтый цвет. Эта реакция называется ксантопротеиновой.
3) При добавлении к раствору белка растворов едкого натра и сульфата меди (II) появляется розово-фиолетовое окрашивание за счет образования комплексных соединений меди (II) с пептидными связями. Эта реакция называется биуретовой.
4) При нагревании серусодержащих аминокислот с уксусно-кислым свинцом в щелочной среде образуется осадок черного цвета. Эта реакция называется цистеиновой.
|
|
|
Задачи для самостоятельного решения
1. Напишите все возможные уравнения реакций, протекающих по карбоксильной группе молекулы фенилаланина.
2. Напишите все возможные уравнения реакций, протекающих по аминогруппе
молекулы аланина.
3. При гидролизе трипептида были получены аминокислоты: глицин, серин, цистеин. Какое строение мог иметь исходный трипептид? Напишите все возможные структурные формулы.
4. С какими из перечисленных ниже реагентов глицин реагирует по аминогруппе: NaOH, HCl, CH3COOH, CH3CH2NH2, CaO, HNO2, Na2CO3, CO2, CH3CH2I, CH4. Напишите уравнения реакций.
5. Напишите структурные формулы аминокислот лейцина и валина. Назовите их по международной номенклатуре ИЮПАК.
6. Каков заряд аминокислоты серина, помещенной в буферный раствор, содержащий 10 мл 0, 1 М раствора уксусной кислоты и 100 мл 0, 1 М раствора ацетата натрия, рК (CH3COOH) = 4, 76.
7. Чему равен рН буферного раствора, содержащего в 1 л 0, 1 моль NH4OH и 0, 01 моль NH4Cl, pK (NH4OH) = 4, 75. Какой заряд имеет аминокислота треонин в полученном растворе?
8. Напишите декарбоксилирование, окислительное дезаминирование, трансаминирование аминокислоты гистидин и образование трипептида: гистидилаланилсерин.
9. Определите характер среды в растворах различных аминокислот: лейцина, лизина, аспарагиновой кислоты и их заряд при изменении рН.
10. К каким электродам и в каком порядке будут двигаться при электрофорезе следующие аминокислоты: аланин (рI = 6, 02); аспарагиновая кислота (рI = 2, 98); аргинин (рI = 10, 05), если электрофорез проводится в буферном растворе при рН = 8, 6?
Тестовые задания
Выберите один правильный ответ
1. Незаменимые аминокислоты:
1) не могут заменяться на аминокислоты, вводимые в организм с пищей
2) не могут синтезироваться в организме из других веществ
|
|
|
3) входят преимущественно в состав растительных белков
4) входят в состав нуклеиновых кислот
2. Аминокислота, относящаяся к моноаминомонокарбоновой:
1) глутаминовая 3) серин
2) лизин 4) аспарагиновая
3. Аминокислота, относящаяся к моноаминодикарбоновой:
1) валин 3) фенилаланин
2) цистеин 4) аспарагиновая
4. Раствор лизина может иметь значение рН:
1) 3 2) 5 3) 7 4) 8
5. Вещество, добавление которого вызывает обратимое осаждение белков:
1) нитрат свинца 3) хлорид калия
2) азотная кислота 4) хлорид ртути
6. Аланин может вступать во взаимодействие с:
1) этаном 3) водородом
2) гидроксидом калия 4) хлоридом калия
7. Ксантопротеиновая реакция является качественной на:
1) пептидные связи
2) остатки аминокислот, содержащих бензольное кольцо
3) остатки аминокислот, содержащих серу
4) остатки аминокислот, содержащих гидроксогруппу
8. Цистеиновая реакция дает окрашивание:
1) желтое 3) черное
2) фиолетовое 4) малиновое
9. Оптических изомеров не имеет:
1) фенилаланин 3) аланин
2) глицин 4) валин
10. Аминоуксусная кислота реагирует с каждым из двух веществ:
1) HCl, KOH 3) C2H5OH, KCl
2) NaCl, NH3 4) CO2, HNO3
|
|
|


