 |
Физико-химические свойства этилового спирта
|
|
|
|
Этиловый спирт – бесцветная прозрачная жидкость; молярная масса С2Н5ОН 46 г/моль; температура плавления –114,14°С; температура кипения 78,3°С; критическое давление 6,395 МПа; температура вспышки 13°С; температура самовоспламенения 404°С; плотность 0,7893 г/см3; смешивается с водой в любых соотношениях.
Расчет термодинамических величин
2.1. Реакция горения этилового спирта в воздухе:
С n Н m O r + 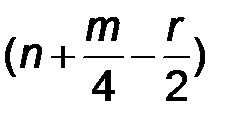 ×(O2 + 3,75 N2)
×(O2 + 3,75 N2) 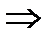
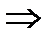 n CO2(г) +
n CO2(г) +  H2O(ж) +
H2O(ж) +  ×3,75 N2.
×3,75 N2.
Для этилового спирта С2Н5ОН: n =2, m =6, r =1:
C2H5OH(Ж) + 3 (O2 + 3,75N2)(г) 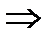 2 CO2(г) + 3H2O(ж) + 11,25 N2.
2 CO2(г) + 3H2O(ж) + 11,25 N2.
2.2. Табличное значение стандартной энтальпии сгорания этилового спирта  =−1366,91 кДж/моль.
=−1366,91 кДж/моль.
Следовательно, высшая энтальпия сгорания топлива 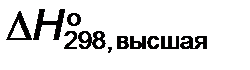 равна:
равна:
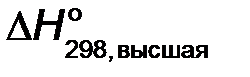
 −1366,91 кДж/моль С2Н5ОН.
−1366,91 кДж/моль С2Н5ОН.
2.3. Высшая теплота сгорания топлива QВ:
Qв 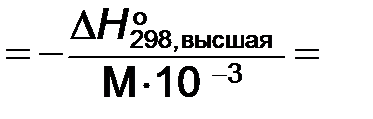
 29715кДж/кг С2Н5ОН≈
29715кДж/кг С2Н5ОН≈
≈29,72 МДж/кг С2Н5ОН.
2.4. Низшая энтальпия сгорания топлива  рассчитывается по уравнению реакции:
рассчитывается по уравнению реакции:
С n Н m O r + 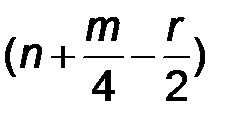 ×(O2+3,75 N2)
×(O2+3,75 N2) 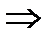
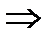 n CO2(г) +
n CO2(г) + 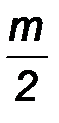 H2O(г)+
H2O(г)+  ×3,75 N2.
×3,75 N2.
Для этилового спирта
C2H5OH(Ж) + 3 (O2 + 3,75N2)(г) 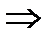 2 CO2(г) + 3H2O(г) + 11,25 N2.
2 CO2(г) + 3H2O(г) + 11,25 N2.
Низшая энтальпия сгорания  отличается от высшей на энтальпию конденсации водяного пара
отличается от высшей на энтальпию конденсации водяного пара 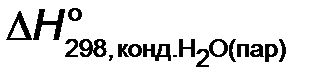 =−44,01 кДж/моль. Из уравнения реакции горения этилового спирта видно, что образуются три моля воды. Поэтому
=−44,01 кДж/моль. Из уравнения реакции горения этилового спирта видно, что образуются три моля воды. Поэтому
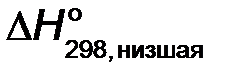
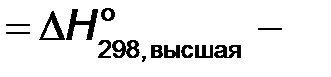
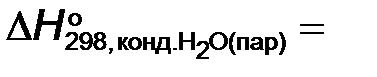 −1366,91+3·44,01=
−1366,91+3·44,01=
=−1234,88 кДж/моль.
2.5. Низшая теплота сгорания топлива QН:
QН  26845 кДж/кг С2Н5ОН ≈
26845 кДж/кг С2Н5ОН ≈
≈ 26,85 МДж/кг С2Н5ОН.
2.6. Теоретически необходимое количество воздуха для полного сгорания 1 кг топлива:
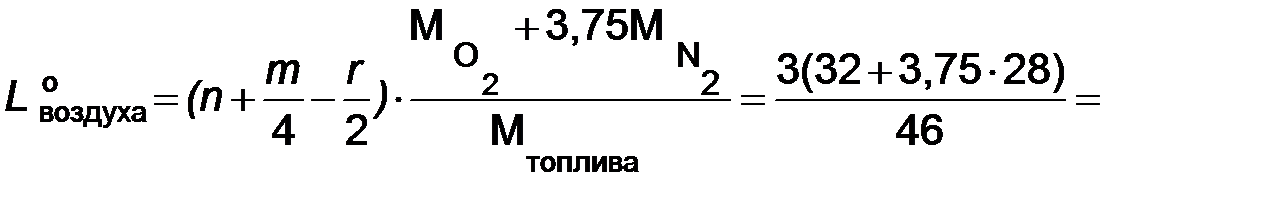
= 8,9 кг воздуха/кг топлива.
2.7. Количество топливовоздушной смеси:
М1 = 1топлива +  (О2 + 3,75N2)=1топлива+3(1+3,75)=15,25 моль.
(О2 + 3,75N2)=1топлива+3(1+3,75)=15,25 моль.
2.8. Низшая теплота сгорания топливовоздушной смеси q н, она же калорийность стехиометрической смеси топлива с воздухом:
 кДж/м3.
кДж/м3.
Таблица 6
Сравнительные характеристики (QН, 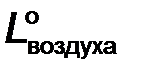 , q н)
, q н)
Этилового спирта и бензина
|
|
|
| Характеристики | Бензин | Этиловый спирт | |
| Справочные данные | Расчет | ||
| Низшая теплотворная способность, QН (МДж/кг) | 43,3 – 44,0 | 25,0 – 26,8 | 26,85 |
| Низшая теплота сгорания топливовоздушной смеси, q н (кДж/м3) | 3439 − 3910 | ||
Стехиометрическая потребность воздуха в процессе сгорания, 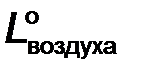 (кг воздуха / кг топлива) (кг воздуха / кг топлива)
| 14,9 | 9,0 | 8,9 |
Выводы
Из приведенных данных (табл. 6) следует, что этиловый спирт и бензин имеют близкую по значению теплотворную способность стехиометрической смеси.
Для этилового спирта характерна меньшая теплотворная способность единицы массы топлива и требуется меньшее стехиометрическое количество воздуха, необходимое для сгорания спирта, что обусловлено меньшим содержанием углерода и большим содержанием кислорода в спирте.
Анализ физико-химических свойств этилового спирта и термодинамических расчетов в сравнении со свойствами бензина показывает возможность его использования в качестве топлива для двигателей с искровым зажиганием.
Проблемой, ограничивающей применение этилового спирта в качестве топлива, являются большие затраты энергии на производство спирта по сравнению с энергией, получаемой в процессе его сгорания.
Кроме того, коррозионная активность спиртов, а также их активность по отношению к ряду пластмасс требует пересмотра материалов топливной системы.
Этиловый спирт применяется в настоящее время для питания автомобилей в виде смеси (90% бензина + 10% С2Н5ОН – газойль).
ПРИЛОЖЕНИЕ
Таблица 1
Варианты заданий для выполнения курсовой работы
| № варианта | Вещество, агрегатное состояние | № варианта | Вещество, агрегатное состояние |
| С2Н2 (г) (ацетилен) | н-С6Н14(ж) (н-гексан) | ||
| С2Н4(г) (этилен) | н-С7Н16(ж) (н-гептан) | ||
| С2Н6(г) (этан) | н-С8Н18 (ж) (н-октан) | ||
| С3Н4 (г) (пропадиен) | н-С9Н20 (ж) (н-нонан) | ||
| С3Н6(г) (пропилен) | н-С10Н22(ж) (н-декан) | ||
| С3Н8(г) (пропан) | СН3ОН(ж) (метиловый спирт) | ||
| С3Н6(г) (циклопропан) | С3Н5ОН (ж) (аллиловый спирт) | ||
| н-С4Н8(г) (н-бутилен) | С3Н7ОН (ж) (н-пропиловый спирт) | ||
| изо-С4Н8(г) (изобутилен) | С3Н7ОН (ж) (изопропиловый спирт) | ||
| н-С4Н10(г) (н-бутан) | С4Н8О2 (ж) (этилацетат) | ||
| изо-С4Н10(г) (изобутан) | С4Н9ОН (ж) (н-бутиловый спирт) | ||
| С5Н10(ж) (циклопентан) | С4Н9ОН (ж) (изобутиловый спирт) | ||
| н-С5Н12(г) (н-пентан) | С4Н10О (ж) (диэтиловый эфир) | ||
| изо-С5Н12(г) (изопентан) | С6Н5СН2ОН (ж) (бензиловый спирт) | ||
| С6Н10(ж) (циклогексен) | С6Н11ОН (ж) (циклогексанол) | ||
| С6Н12(ж) (циклогексан) | С8Н17ОН(ж) (октиловый спирт) |
Таблица 2
|
|
|
Значения стандартных энтальпий сгорания
| Вещество | Агрегатное состояние |  Но298,сгор.,
кДж/моль Но298,сгор.,
кДж/моль
|
| Углеводороды | ||
| СН4 (метан) | газ | -890,31 |
| С2Н2 (ацетилен) | газ | -1299,63 |
| С2Н4 (этилен) | газ | -1410,97 |
| С2Н6 (этан) | газ | -1559,88 |
| С3Н4 (пропадиен) | газ | -1946,00 |
| С3Н6 (пропилен) | газ | -2051,00 |
| С3Н8 (пропан) | газ | -2220,03 |
| С3Н6 (циклопропан) | газ | -2078,60 |
| н-С4Н8 (н-бутилен) | газ | -2717,30 |
| изо-С4Н8 (изобутилен) | газ | -2700,50 |
| н-С4Н10 (н-бутан) | газ | -2878,83 |
| изо-С4Н10 (изобутан) | газ | -2871,69 |
| С5Н10 (циклопентан) | жидкость | -3278,60 |
| н-С5Н12 (н-пентан) | газ | -3536,15 |
| изо-С5Н12 (изопентан) | газ | -3528,11 |
| С6Н10 (циклогексен) | жидкость | -3731,70 |
| С6Н12 (циклогексан) | жидкость | -3919,91 |
| н-С6Н14 (н-гексан) | жидкость | -4163,12 |
| н-С7Н16 (н-гептан) | жидкость | -4811,12 |
| н-С8Н18 (н-октан) | жидкость | -5450,50 |
| н-С9Н20 (н-нонан) | жидкость | -6124,50 |
| н-С10Н22 (н-декан) | жидкость | -6737,10 |
| Кислородосодержащие соединения | ||
| СН3ОН (метиловый спирт) | жидкость | -715,00 |
| С2Н5ОН (этиловый спирт) | жидкость | -1366,91 |
| С3Н5ОН (аллиловый спирт) | жидкость | -1851,00 |
| С3Н7ОН (н-пропиловый спирт) | жидкость | -2010,40 |
| С3Н7ОН (изопропиловый спирт) | жидкость | -2003,80 |
| С4Н8О2 (этилацетат) | жидкость | -2254,21 |
| С4Н9ОН (н-бутиловый спирт) | жидкость | -2671,90 |
| С4Н9ОН (изобутиловый спирт) | жидкость | -2633,00 |
| С4Н10О (диэтиловый эфир) | жидкость | -2730,90 |
| С6Н5СН2ОН (бензиловый спирт) | жидкость | -3741,70 |
| С6Н11ОН (циклогексанол) | жидкость | -3726,70 |
| С8Н17ОН (октиловый спирт) | жидкость | -5280,20 |
ОГЛАВЛЕНИЕ
| 1. Введение | |
| 2. Методика расчета термодинамических характеристик | |
| 3. Методика выполнения курсовой работы(примеры) ПРИЛОЖЕНИЕ | |
|
|
|
|
|
|


