 |
Физико-химические свойства пластовых вод
|
|
|
|
Плотность пластовых вод сильно зависит от минерализации, т.е. содержания растворённых солей. В среднем плотность пластовой воды составляет 1010-1210 кг/м3.
Тепловое расширение воды характеризуется коэффициентом теплового расширения:
 . (3.29)
. (3.29)
Из формулы следует, что коэффициент теплового расширения воды (Е) характеризует изменение единицы объёма воды при изменении её температуры на 1°С. По экспериментальным данным в пластовых условиях он колеблется в пределах (18-90)×10-5 1/°С. С увеличением температуры коэффициент теплового расширения возрастает, с ростом пластового давления – уменьшается.
Коэффициент сжимаемости воды характеризует изменение единицы объёма воды при изменении давления на единицу:
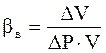 . (3.30)
. (3.30)
Коэффициент сжимаемости воды изменяется в пластовых условиях в пределах 3,7×10-10 – 5,0×10-10 Па-1. При наличии растворённого газа он увеличивается, и приближённо может рассчитываться по формуле:
bвг = bв (1+0,05×S), (3.31)
где S – количество газа, растворённого в воде, м3/м3.
Объёмный коэффициент пластовой воды характеризует отношение удельного объёма воды в пластовых условиях к удельному объёму воды в стандартных условиях:
 . (3.32)
. (3.32)
Увеличение пластового давления способствует уменьшению объёмного коэффициента, а рост температуры – увеличению. Объёмный коэффициент изменяется в пределах 0,99-1,06.
Вязкость воды в пластовых условиях зависит, в основном, от температуры и минерализации. От давления вязкость зависит слабо. Наибольшую вязкость имеют хлоркальциевые воды (в 1,5-2 раза больше чистой воды).
Минерализация воды – содержание растворённых солей в г/л. По степени минерализации пластовые воды делятся на четыре типа:
|
|
|
рассолы (Q>50 г/л);
солёные (10<Q<50 г/л);
солоноватые (1<Q<10 г/л);
пресные (Q£1 г/л).
Минерализация пластовой воды растёт с глубиной залегания пластов.
По типу растворённых в воде солей различают хлоркальциевые (хлоркальциево-магниевые) и гидрокарбонатные (гидрокарбонатно-натриевые, щелочные) пластовые воды. Тип пластовой воды определяется соотношением ионов растворённых солей:
анионов: OH–; Cl–; SO42–; CO32–; HCO3–;
катионов: H+; K+; Na+; NH4+; Mg2+; Ca2+; Fe3+;
ионов микроэлементов: I–; Br–;
коллоидных частиц SiO2; Fe2O3; Al2O3;
нафтеновых кислот и их солей.
Состав воды определяет её жёсткость. Жёсткостью называется суммарное содержание растворённых солей кальция, магния, железа.
Жёсткость подразделяется на временную (карбонатную) и постоянную (некарбонатную).
Временная жёсткость или карбонатная (Жк) обусловлена содержанием в воде гидрокарбонатов двухвалентных металлов (кальция, магния, железа).
Постоянная жёсткость или некарбонатная (Жнк) обусловлена наличием в воде сульфатов и хлоридов двухвалентных металлов (кальция, магния, железа).
Общая жёсткость воды определяется как сумма карбонатной и некарбонатной:
Жо = Жк + Жнк (3.33)
Жёсткость воды оценивается содержанием в ней солей в миллиграмм-эквивалентах на литр  .
.
Жк, Жнк оценивают как сумму жесткостей всех i-ых ионов (∑gi):
 , (3.34)
, (3.34)
где mvi – концентрация i-го иона в воде (мг/л);
эi – эквивалент i-го иона.
 , (3.35)
, (3.35)
где Мi – молекулярная масса иона;
n – валентность иона.
Жо = Sgi (3.36)
Тип природной воды характеризуется в зависимости от содержания двухвалентных катионов:
очень мягкая вода – до 1,5 мг-экв./л;
мягкая вода – 1,5-3,0 мг-экв./л;
умеренно жёсткая вода – 3,0-6,0 мг-экв./л;
жёсткая вода – более 6 мг-экв./л.
Временную (карбонатную) жёсткость можно устранить термическим методом (длительным кипячением) или химическим методом – добавлением гидроксида кальция Са(ОН)2.
В обоих случаях выпадает в осадок карбонат кальция СаСО3.
|
|
|
Постоянную жёсткость устраняют химическим способом с помощью добавления соды или щёлочи.
Содержание водородных ионов в воде определяется параметром рН:  , где Сн+ – концентрация ионов водорода. В зависимости от рН различают следующие типы воды:
, где Сн+ – концентрация ионов водорода. В зависимости от рН различают следующие типы воды:
нейтральная (рН=7);
щелочная (pH>7);
кислая (pH<7).
Вода, находясь в контакте с нефтью, частично в ней растворяется. Коэффициент растворимости нефти в воде зависит от наличия в воде полярных составляющих. Чем легче нефть, тем меньше в ней растворено воды. Нефти парафинового основания содержат мало воды. С ростом в нефти содержания ароматических углеводородов и гетероатомных соединений, растворимость воды в нефти растёт.
За счёт растворения воды в нефти происходят изменения в зоне водонефтяного контакта. Чёткой границы вода-нефть не существует. За счёт растворения воды образуется т.н. "переходная зона", величина которой зависит от полярности нефти.
|
|
|


