 |
Окислительно-восстановительные процессы
|
|
|
|
Химические реакции можно подразделить на два типа: реакции, протекающие без изменения степени окисления атомов, входящих в состав реагентов (например, реакции обмена, происходящие в растворах, некоторые реакции соединения и разложения), и реакции, при которых изменяется степень окисления одного или нескольких элементов.
Реакции, относящиеся ко второму типу, называются окислительно-восстановительными.
Окислительно-восстановительные реакции:
· это такие реакции, которые протекают с переходом электронов от одних атомов (восстановителя) к другим (окислителю).
или
· это реакции, протекающие с изменением степени окисления атомов реагирующих веществ.
Окислительно-восстановительными реакциями являются большинство лабораторных, промышленных и природных процессов.
Степень окисления – условный заряд, который приписывают данному химическому элементу в соединении исходя из предположения о полном смещении электронной плотности от менее электроотрицательного к более электроотрицательному элементу.
Например, 
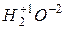 ,
, 
 ,
,  .
.
Степень окисления изменяется либо в результате полного перехода электронов от одного участника процесса к другому, либо за счет перераспределения электронной плотности между атомами реагентов.
При протекании окислительно-восстановительных реакциях происходит процесс окисления и процесс восстановления.
В качестве окислителей и восстановителей могут выступать как простые и сложные вещества, так и ионы, содержащие в своем составе элементы, изменяющие степень окисления в процессе реакции.
Проявление окислительно-восстановительных свойств атомов различных элементов зависит:
1) от положения элемента в периодической системе:
|
|
|
а) металлы в свободном состоянии могут быть только восстановителями (наиболее активные восстановители – щелочные и щелочноземельные металлы);
б) неметаллы (исключая фтор) в свободном состоянии способны проявлять как окислительные, так и восстановительные свойства;
2) от степени окисления элемента в веществе:
| Степень окисления элемента в соединении | пример | Проявляемые окислительно-восстановительные свойства |
| максимальная | 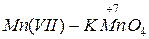


| участвует только в процессе восстановления, является только окислителем |
| минимальная | 

| участвует в процессе окисления, является только восстановителем |
| промежуточная |  , , 
| участвует в процессе окисления и восстановления, проявляет окислительно-восстановительную двойственность |
Классификация окислительно-восстановительных реакций.
1. Межмолекулярные окислительно-восстановительные реакции – реакции, в которых окислитель и восстановитель входят в состав разных веществ.
Например,

| окислитель | 
| процесс восстановления | ||
| восстановитель | 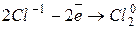
| процесс окисления |
2. Внутримолекулярные окислительно-восстановительные реакции – реакции, в которых окислитель и восстановитель (атомы разных элементов) находятся в составе одного вещества.
Например,

| окислитель | 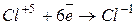
| процесс восстановления | ||
| восстановитель | 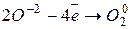
| процесс окисления |
3. Диспропорционирование (самоокисление – самовосстановление ) – реакции, в которых окислителем восстановителем является один и тот же элемент, в одной той же степени окисления.
Например,
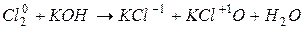
| окислитель | 
| процесс восстановления | ||
| восстановитель | 
| процесс окисления |
4. Конпропорционирование – реакции, в которых окислителем и восстановителем является один и тот же элемент в разных степенях окисления.
|
|
|
Например,

| окислитель | 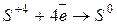
| процесс восстановления | ||
| восстановитель | 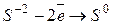
| процесс окисления |
|
|
|


