 |
Гидрометаллургия. Гидрометаллургические процессы.
|
|
|
|
Гидрометаллургия – обработка руд различными растворами.
Гидрометаллургические процессы:
· Восстановление металла из растворов солей более активным металлом.
Медная руда (перевод в раствор):
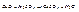 ,
,
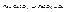 , Fe – более активный металл.
, Fe – более активный металл.
· Гидроэлектрометаллургический – оксиды или металлы переводят в раствор (кислота или щёлочь) и раствор подвергают электролизу.
Медная руда
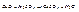 ,
,
Электролиз:
 ,
,  .
.
№20.
Комплексные соединения. Их строение, номенклатура и диссоциация в растворах.
Комплексные соединения – вещества, в узлах кристаллической решётки которых находятся сложные частицы, построенные за счёт координации одним атомом или ионов электронейтральных молекул или противоположно заряженных ионов способные к самостоятельному существованию в расплавленном или растворённом состоянии.
Строение комплексных соединений (теория Вернера)
1. Комплексообразователь (М) – катионы d -элементов (Ni, Cr и т.д.)
2. Комплексообразователь координирует вокруг себя некоторое число одинаковых или разных лигандов – L.
Лиганды:
· Анионы:
· Простые ( );
);
· Сложные (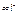 );
);
· Нейтральные молекулы:
· Органические ( );
);
· Неорганические ( ).
).
Число лигандов непосредственно соединённых с комплексообразователем называется координационным числом.
 , 2, 4, 6, 8 – чаще всего.
, 2, 4, 6, 8 – чаще всего.
Комплексообразователь с лигандами образуют внутреннюю сферу, и она заключается в квадратные скобки:  .
.
В зависимости от заряда центрального иона и лигандов комплексные соединения бывают либо катионными, либо анионными, либо нейтральными.
Комплексные соединения:
· Катионные 
· Анионные 
· нейтральные 
Номенклатура комплексные соединений.
Первым называется анион, затем в родительном падеже катион, притом цифры римские, а сами лиганды в порядке увеличения их сложности.
|
|
|
 – сульфат бромопентааммин кобальта (III)
– сульфат бромопентааммин кобальта (III)
 – тетрагидроксодиакваферрат натрия (III).
– тетрагидроксодиакваферрат натрия (III).
Устойчивостькомплексных соединений определяется константой нестойкости. По первой ступени комплексные соединения диссоциируют как сильные электролиты.
 .
.
Дальнейшая диссоциация происходит по типу диссоциации слабых электролитов
 ,
,
 – табличные данные.
– табличные данные.

 .
.
 .
.
Чем меньше  , тем устойчивее комплекс.
, тем устойчивее комплекс.
Константа устойчивости:

№21.
Жёсткость воды и способы её устранения.
Жёсткость воды обусловлена наличием солей Ca, Mg, Fe. Она выражается числом милиэквивалентов 

 в миллилитре воды.
в миллилитре воды.
1 милиэквивалент жёсткости отвечает содержанию:




 .
.
Вода:
· Жёсткая  ,
,
· Средняя  ,
,
· Мягкая 
 .
.
Жёсткость:
· Временная (карбонатная) 


· Постоянная (обусловленная наличием хлоридов и сульфатов Fe, Ca, Mg).
Временная жёсткость устраняется кипячением, добавлением соды или извести..
1.  ,
,
2. 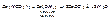 ,
,

3.  .
.
Постоянная жёсткость устраняется действием соды или  .
.
 ,
,
 .
.
Современный способ смягчения воды – применение синтетических ионообменных смол (иониты).
Иониты: катиониты и аниониты.
 .
.
Вода пропускается через слой ионита, связывается в соединения.
№22.
Синтетические полимеры.
Полимер – вещество с большой молекулярной массой, молекула которого состоит из большого числа (n) структурных звеньев (повторяющихся группировок, имеющих одинаковое строение).
n – степень полимеризации.
Структурное звено:  ,
,
Структурная формула:  ,
,
 – жидкость,
– жидкость,
 – пластичное твёрдое вещество,
– пластичное твёрдое вещество,
 – непластичное твёрдое вещество.
– непластичное твёрдое вещество.
Полимеры подразделяются:
– неорганические;
– органические;
– элементоорганические.
Органические полимеры: синтетические и природные.
|
|
|


