 |
Сорбция из водных растворов
|
|
|
|
СОДЕРЖАНИЕ
1. Введение
2. Адсорбционные методы
3. Сорбция из водных растворов
4. Изотермы адсорбции. Уравнение Лэнгмюра. Уравнение Фрейндлиха......
5. Расчет изотермы адсорбции молекулярно-растворенных органических веществ на активных углях без экспериментальных измерений
5.1 Аддитивность величин стандартного уменьшения свободной энергии адсорбции
5.2 Парциальная константа адсорбционного равновесия при адсорбции из водных растворов на пористых углеродных сорбентах
5.3 Коэффициент активности. Предельное значение коэффициента активности
5.4 Вычисление изотерм адсорбции органических веществ из водных растворов углеродными адсорбентами
6. Методы выбора и контроля адсорбентов для очистки воды
6.1. Влияние природы поверхности и пористости углеродных адсорбентов на молекулярную адсорбцию органических веществ из водных растворов
6.2. Влияние ионизации и ассоциации молекул в растворе на их адсорбцию
7. Кинетика и динамика сорбции из водных растворов
8. Активные угли и их регенерация
9. Использование дешевых сорбентов и отходов
Заключение
Практическая часть
Список используемой литературы
ВВЕДЕНИЕ
Объем потребляемой в мире воды достигает 4 трлн. м3 в год, а
преобразованию со стороны человека подвергается практически вся гидросфера. Химическая и нефтехимическая отрасли промышленности способствуют проникновению в водную среду веществ, обычно отсутствующих в ней, или превышению естественного уровня их концентрации, ухудшающей качество водной среды. [9]
За время существования человечества в природную среду было введено огромное количество органических веществ. Вредные химические элементы и вещества попадают в водоемы, ухудшая их санитарное состояние и вызывая необходимость специальной глубокой очистки воды перед использованием ее для хозяйственно-питьевых и некоторых промышленных целей. Многие органические примеси не извлекаются из воды механически, не нейтрализуются при биологической очистке, не удаляются такими традиционными методами водоочистки, как отстаивание, коагуляция и флотация. Это обуславливает введение в комплексную технологическую схему водоподготовки стадии адсорбционной доочистки. Как правило, эта стадия является заключительным этапом в технологическом процессе очистки воды. Адсорбционный метод является хорошо управляемым процессом. Он позволяет удалять загрязнения различного характера практически до любой остаточной концентрации независимо от их химической устойчивости. При этом отсутствуют вторичные загрязнения. Отсюда перспективной является тенденция развития фильтрующе-сорбирующих устройств, предназначенных для локальной доочистки питьевой воды, и этот вопрос является весьма актуальным.
|
|
|
АДСОРБЦИОННЫЕ МЕТОДЫ
Адсорбция – процесс концентрирования растворенного вещества (адсорбата) или растворителя (адсорбтива) из объема фаз на поверхности раздела между ними (на поверхности твердого тела (адсорбента) или жидкости). [3]
В зависимости от характера сорбционного взаимодействия адсорбата и адсорбента различают физическую адсорбцию, активированную адсорбцию и хемосорбцию.
Физическая адсорбция обусловлена силами межмолекулярного взаимодействия Ван-дер-Ваальса, не избирательна, полностью необратима, протекает с высокой скоростью и имеет сравнительно низкую теплоту адсорбции – от нескольких килоджоулей до нескольких десятков килоджоулей на моль адсорбата. Адсорбция протекает молекулярно, т.е. преимущественно адсорбируются соединения в недиссоциированном состоянии. Физическая адсорбция характерна для веществ, адсорбируемых из парогазовой фазы, а при адсорбции из растворов осложнена физико-химическим взаимодействием адсорбата, адсорбтива и адсорбента.
|
|
|
Активированная адсорбция обусловлена взаимодействием адсорбата и адсорбента с образованием поверхностного соединения особого рода, характерного тем, что молекулы адсорбента, вступившие во взаимодействие с молекулами адсорбата (адсорбтива), остаются в кристаллической решетке адсорбента. Активированная адсорбция избирательна, как правило, протекает медленно (с повышение температуры скорость адсорбции заметно возрастает), необратима и характеризуется высокой теплотой адсорбции – до нескольких сотен килоджоулей на моль адсорбата.
Хемосорбция – обычная химическая реакция, протекающая на поверхности адсорбента и сопровождающаяся выделением теплоты, эквивалентной теплоте химической реакции.
Использование комбинации нескольких адсорбентов разного типа позволяет осуществлять комплексную корректировку состава воды по всем необходимым в каждом конкретном случае показателям. Использование смесей адсорбентов определенного состава для подготовки питьевой воды не только высокоэффективно, но и чрезвычайно экономически выгодно. [4]
Сорбция из водных растворов
Материал, на поверхности пор которого происходит концентрирование поглощаемого вещества, называют адсорбентом, а само вещество — адсорбатом. Адсорбционные явления основаны на физическом и химическом взаимодействии адсорбата и адсорбента.
Силы молекулярного взаимодействия, в основном, дисперсионные, обуславливающие физическую адсорбцию, возникают при сближении молекул материала адсорбента и адсорбируемого вещества и проявляются в упорядочении движения частиц вследствие взаимного притяжения. Дисперсионные взаимодействия неспецифичны, присущи всем веществам и различаются в конкретных случаях лишь количественно. Потенциальная энергия взаимодействия двух атомов равна
 (1)
(1)
где r — расстояние между центрами атомов; b — эмпирическая константа; С n — константа поляризации.
Приведенное выражение показывает, что адсорбционные взаимодействия проявляются только на очень малых расстояниях. Теоретически, если взаимное притяжение атомов максимально на расстоянии r 0, то при  их взаимодействие ослабевает в 4 — 5 раз. И, наоборот, при
их взаимодействие ослабевает в 4 — 5 раз. И, наоборот, при  превалируют силы отталкивания. Иногда дисперсионные взаимодействия усиливаются водородными связями и электростатическими (индукционными или ориентационными) силами. Эти дополнительные взаимодействия специфичны для определенного вида адсорбируемых веществ или свойств поверхности адсорбента. Адсорбция – процесс самопроизвольный, протекающий с выделением некоторого количества теплоты,
превалируют силы отталкивания. Иногда дисперсионные взаимодействия усиливаются водородными связями и электростатическими (индукционными или ориентационными) силами. Эти дополнительные взаимодействия специфичны для определенного вида адсорбируемых веществ или свойств поверхности адсорбента. Адсорбция – процесс самопроизвольный, протекающий с выделением некоторого количества теплоты,
|
|
|
В отличие от физической адсорбции, носящей обратимый характер с сохранением индивидуальности адсорбата и адсорбента, хемосорбция — скорее химический процесс на границе раздела фаз. Этот процесс обычно необратимый и значительно более экзотермичный, чем физическая сорбция.
Сорбция из жидких растворов значительно сложнее, чем из парогазовой смеси, так как включает взаимодействия сорбента с сорбируемым веществом и с растворителем (водой); при этом также следует учитывать взаимодействие растворителя с сорбатом. Поэтому, несмотря на то, что сорбция из водных растворов исследуется и используется почти 200 лет, она изучена значительно менее сорбции из парогазовой фазы. В основном механизм сорбции из растворов в том или ином виде объясняют представлениями, выведенными для газовой фазы, лишь дополняя или ограничивая условиями, специфическими для жидкой фазы. Отличия в подходе к подобному переносу отражаются на виде и точности моделей и расчетов систем сорбционной очистки воды.
Теория полимолекулярной сорбции, в основе которой лежит представление о многослойной сорбции на поверхности макро- и мезопористого сорбента, была разработана Брунауэром, Эметом и Теллером. Однако в практике наибольшее распространение получили микропористые сорбенты, в чрезвычайно малом пространстве микропор которых послойной сорбции вещества на поверхности не происходит. При сорбции в микропорах происходит заполнение части или всего объема их сорбатом, который под действием взаимно усиливающихся и перекрывающихся адсорбционных полей, создаваемых противоположными стенками пор, находится в специфическом уплотненном состоянии. Теории объемного заполнения микропор, разработанная Дубининым и его школой, использует понятие о предельном объеме адсорбционного пространства микропористого сорбента W 0. Основное уравнение адсорбции паров и газов на микропористых сорбентах, известное как уравнение Дубинина – Радушкевича, имеет вид:
|
|
|
 (2)
(2)
При сорбции вещества из раствора оно занимает на поверхности или в объеме пор сорбента место, которое до этого занимали молекулы растворителя (воды), а не свободное пространство. Присутствие воды в порах приводит к некоторому выравниванию сорбционного потенциала. В объеме сорбируемой фазы концентрация вещества значительно выше, чем в растворе. При этом снижается поверхностное натяжение на границе раздела раствор – твердый сорбент.
Основы термодинамики адсорбции из растворов впервые сформулировал Гиббс более 100 лет назад. Им было введено понятия избыточной адсорбции  , т.е. избыточного содержания поглощаемого вещества в адсорбированной фазе по сравнению с его содержанием в растворе. Величина избыточной (гиббсовской) адсорбции легко определима по формуле
, т.е. избыточного содержания поглощаемого вещества в адсорбированной фазе по сравнению с его содержанием в растворе. Величина избыточной (гиббсовской) адсорбции легко определима по формуле
 (3)
(3)
где С0 и Ск – концентрация вещества в растворе до и после опыта; V – объем раствора; m – навеска сорбента.
Термодинамический подход к решению проблемы сорбции является наиболее общим и позволяет оценивать сорбируемость молекул по значению максимальной работы переноса вещества из раствора на поверхность сорбента. Поскольку при сорбции вещества из воды происходит уменьшение свободной энергии системы  , Когановский предложил использовать эту величину для прогнозирования эффективности извлечения растворенных соединений из воды. Константа равновесия при сорбции из разбавленных растворов
, Когановский предложил использовать эту величину для прогнозирования эффективности извлечения растворенных соединений из воды. Константа равновесия при сорбции из разбавленных растворов 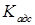 связана с
связана с  зависимостью вида
зависимостью вида  , из которой следует, что чем больше
, из которой следует, что чем больше  , тем лучше сорбируется вещество.
, тем лучше сорбируется вещество.
Идею о возможности применения теории объемного заполнения микропор для описания сорбции из жидкой фазы выдвинули Эльтеков и Стадник. Эта идея использует представления об отсутствии влияния физического состояния сорбата в объемной фазе на сорбционный потенциал в микропорах углей и отсутствии ассоциативных, ионных и водородных связей между молекулами сорбируемого вещества и воды, а также внутри сорбата. Эта теория применима для расчета сорбции из очень разбавленных растворов ограничено растворимых веществ: уравнение изотермы сорбции на микропористых АУ в данном случае принимает вид:
|
|
|
 (4)
(4)
Здесь W 0 – предельный объем микропор сорбента; Vm – мольный объем сорбата;  – структурно-энергетическая константа;
– структурно-энергетическая константа;  – растворимость соединения в воде при данной температуре;
– растворимость соединения в воде при данной температуре;  – равновесная концентрация в воде.
– равновесная концентрация в воде.
Обобщая данные о сорбируемости на АУ низкомолекулярных органических соединений, можно сделать вывод, что менее других сорбируются структурно простые вещества в ионной форме, лучше – в молекулярной. Сорбируемость органических веществ возрастает в ряду:
гликоли < спирты < кетоны < сложные эфиры < альдегиды <
< недиссоциированные кислоты < ароматические соединения.
Вода, сорбируясь на участках окисленной поверхности АУ, препятствует сорбции на них неполярных алифатических соединений. Сорбируемость органических веществ возрастает с увеличением длины углеродной цепи (если она не ограничена размером пор сорбента), причем для гомологов, согласно правилу Траубе, на величину, кратную изменению длины углеродной цепи.
Способность к сорбции возрастает с ростом молекулярной массы органических веществ, особенно выше 30 000. Аналогична и зависимость при росте мицеллярной массы коллоидов. Присутствие в воде неорганических солей, способствующих укрупнению ассоциатов молекул красителей и гуматов, приводит к их более полному сорбционному выделению.
Специфическими загрязнениями сточных вод заводов СК являются неокисляемые биохимическими путем лейканол и трилон Б. Первый обладает свойствами ПАВ и присутствует в воде в виде отдельных молекул и ассоциатов, что и определяет особенность сорбции его из воды, а именно: при 20–30ºС отдельные молекулы и ассоциаты малых размеров сорбируются на ГАУ, а крупные ассоциаты способны лишь к дальнейшему укрупнению и коагуляции. Поэтому сорбционная емкость ГАУ зависит от начальной концентрации лейканола в воде, так как пропорционально росту  увеличивается и доля крупных ассоциатов лейканола.
увеличивается и доля крупных ассоциатов лейканола.
Эффективность сорбции трилона Б на БАУ, ОУ, АГ-3, СКТ при  ммоль/дм3 почти одинакова. Сорбция трилона Б из воды – типичный случай полимолекулярного поглощения с преобладающим взаимодействием во втором и последующих слоях над взаимодействием в первом слое.
ммоль/дм3 почти одинакова. Сорбция трилона Б из воды – типичный случай полимолекулярного поглощения с преобладающим взаимодействием во втором и последующих слоях над взаимодействием в первом слое.
Применение угля СКТ более эффективно в области малых равновесных концентраций (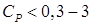 ммоль/дм3); при больших
ммоль/дм3); при больших  целесообразнее сорбция на АГ-3.
целесообразнее сорбция на АГ-3.
Такие биологические объекты, как бактерии и вирусы, несмотря на крупные размеры, хорошо сорбируются АУ. Изотерма сорбции E. Coli описывается уравнением Лэнгмюра, а вируса Polio – уравнением Фрейндлиха.
Влияние температуры на сорбцию из водных растворов далеко не однозначно. Дело в том, что при сорбции на микропористых сорбентах веществ, размеры молекул которых близки к эффективным размерам пор, проникновение этих молекул в поры зависит от их кинетической энергии. При достаточной энергии (температуре) молекулы сорбата проникают в окна пор и сорбируются; в противном случае происходит лишь незначительно поглощение на поверхности мезо- и макропор. Иными словами, сорбционная емкость повышается с ростом температуры; это явление получило название «активированной адсорбции». В то же время физическая сорбция, как любой экзотермический процесс, в целом ухудшается с ростом температуры. Поэтому суммарное внешне фиксируемое проявление этих двух явлений (активированной и физической адсорбции) может иметь экстремум при определенной температуре. Как показано в работах Дубинина, для газов и паров этот экстремум имеет вид острого пика.
При сорбции из водных растворов, а в особенности из таких многокомпонентных систем, как сточные воды, этот пик размыт. Например, при доочистке сточных вод максимальные значения сорбционной емкости достигались при 35 – 60ºС. Емкость угля при 0 – 10 и выше 75 – 80ºС была в 1,5 – 2 раза ниже. В других случаях оптимальная температура может быть иной. Есть данные о том, что с повышением температуры значительно улучшается кинетика адсорбции при доочистке высококонцентрированных вод, что связано с перестройкой молекул в растворах, разрушением ассоциатов воды и сорбируемого вещества, снижением вязкости раствора. Изменение сорбируемости различных веществ на АУ при нагревании неодинаково.
Многокомпонентность состава природных и сточных вод приводит к тому, что показатели сорбции малого (до 5%) или очень большого (более 95%) количества загрязнений от общего отличаются от средних. Обычно это выражается в завышенных показателях сорбции небольшой части хорошо сорбируемых примесей и, наоборот, в низких показателях при высокой степени очистки от плохо сорбируемых веществ. Последнее приводит к тому, что при сорбции в статических условиях при необходимости повысить эффект очистки воды до 92 – 95% дозу АУ следует резко увеличить. [5]
|
|
|


