 |
Химическая связь и некоторые представления о кинетике химических реакций.
|
|
|
|
При взаимодействии атомов между ними может возникнуть химическая связь, приводящая к образованию устойчивой многоатомной системы — молекулы, молекулярного иона, кристалла [5,10,14]. Условием образования химической связи является уменьшение потенциальной энергии взаимодействующих атомов. Возникновение химической связи обусловливается обменом электронами между взаимодействующими атомами. Прочность связи, устойчивость молекулы и многоатомных систем определяется энергией связи,выраженной в Дж/моль или эВ/молекула. Энергия связи — это энергия, необходимая для разъединения (атомизации) многоатомных систем на отдельные атомы или для отрыва одного атома от многоатомной системы. В рассматриваемых процессах ПХТ и ИХТ такими многоатомными системами являются: обрабатываемые материалы и многоатомные молекулы рабочего газа и продукты их разложения в электрическом разряде.
Типичной ковалентной связью обладают молекулы, состоящие из одноименных атомов. Из интересующих нас рабочих веществ, обладающих ковалентной связью атомов в молекулах, следует отметить: водород  , кислород
, кислород 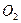 , азот
, азот  , фтор
, фтор  , хлор
, хлор  .
.
Если во взаимодействие вступают разнородные атомы, то при образовании молекулы возникают полярные ковалентные связи. Примером таких многоатомных молекул с полярными ковалентными связями является большинство молекул, используемых для осуществления процессов ПХТ и ИХТ: плавиковая кислота  , аммиак
, аммиак  , углекислый газ
, углекислый газ  , широко используемый в процессах ПХТ и ИХТ хладон-14
, широко используемый в процессах ПХТ и ИХТ хладон-14  .
.
Способность атома оттягивать на себя общую электронную пару характеризуется относительной электроотрицательностью [14]. Значение электроотрицательности элементов определяет прочность связи атомов в многоатомных молекулах. С увеличением разности электроотрицательностей связанных атомов происходит упрочение связи. Электроотрицательность имеет важное значение для оценки вероятности протекания реакций присоединения, имеющих широкое распространение в процессах ПХТ и ИХТ.
|
|
|
Ковалентная связь отличается относительно высокой прочностью, чем объясняется высокая стабильность и малая реакционная способность таких веществ, как фторуглероды, которые широко используются в процессах травления.
Актом химической реакции называется химическое превращение, происходящее за время, меньшее времени соударения атомов или молекул. Это время определяется относительной скоростью Движения взаимодействующих частиц. Химическая реакция —последовательность элементарных актов, в результате которых из суммы молекул одних веществ образуется сумма молекул других
Чтобы произошла реакция, т. е. образовались новые молекулы, сначала необходимо разорвать или ослабить связи между атомами в молекулах исходных веществ, для этого требуется затратить энергию, называемую энергией активации. Энергия активации химической реакции определяется как разность между средней энергией частиц составляющих молекул и средней энергией всех частиц — внутренней энергией молекулы.
При получаемых молекулой энергиях, больших энергии активации, происходит диссоциация молекулы. При диссоциации, многоатомных молекул в результате энергетического воздействия на них происходит образование радикалов — осколков молекул, имеющих неспаренные электроны. В процессах ПХТ и ИХТ энергетическое воздействие на газ осуществляется с помощью электрического разряда. Возникают валентно ненасыщенные частицы, проявляющие вследствие этого высокую химическую активность. С меньшей вероятностью происходит образование ионов. Такими радикалами, например, являются атомы водорода  , хлора
, хлора  , фтора
, фтора  , группы атомов
, группы атомов  ,
, 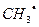 ,
,  . Число точек определяет число неспаренных электронов.
. Число точек определяет число неспаренных электронов.
|
|
|
Остатки углеводородов, образующиеся при отборе у молекул одного, двух или нескольких атомов водорода, образуют углеводородные радикалы, обозначаемые:  — одновалентный,
— одновалентный,  — двухвалентный,
— двухвалентный,  — трехвалентный радикалы, где R — остаток молекулы, которая может включать в свой состав тысячи атомов.
— трехвалентный радикалы, где R — остаток молекулы, которая может включать в свой состав тысячи атомов.
Таким образом, протекание химической реакции подразумевает на первом этапе образование реакционноспособных радикалов, которые затем вступают в новые химические связи, образуя новое вещество.
В процессах ПХТ и ИХТ процесс травления осуществляется в результате гетерогенных реакций на границе раздела двух фаз: плазма — поверхность твердого тела обрабатываемого материала. Кроме этого, происходят многочисленные гомогенные реакции в "плазме, приводящие к образованию и исчезновению реактивных частиц плазмы.
Химическая реакция характеризуется скоростью ее протекания, т. е. кинетикой развития. Факторами, определяющими значение скорости химической реакции, являются: природа реагирующих веществ, их концентрация, температура, присутствие катализатора. В процессах ПХТ к важным факторам, влияющим на скорость протекания реакции травления, относится энергетическая активация поверхности в результате ионной и электронной бомбардировок, ультрафиолетового излучения из плазмы. Скорость протекания гетерогенных реакций зависит также от скоростей подвода и отвода газа к поверхности травления.
Особенность гетерогенных реакций, в частности реакций ПХТ, состоит в том, что они связаны с переносом вещества. В ходе реакции можно выделить три стадии:
1. подвод реагирующего вещества к поверхности травления;
2. собственно химическая реакция на поверхности;
3. отвод продукта реакции от поверхности.
Для реакций с низкой энергией активации лимитирующей стадией, определяющей скорость протекания всей реакции, будет скорость переноса вещества (подвод и отвод). Если энергия, активации велика, то лимитирующей стадией гетерогенной реакции является собственно химическая реакция на поверхности.
|
|
|
В процессах ПХТ и ИХТ практически все происходящие реакции носят цепной характер. В цепных реакциях протекание каждого элементарного акта реакции связано с успешным ходом предыдущего акта и, в свою очередь, обусловливает возможность протекания последующего. Они протекают с участием активных центров на обрабатываемой поверхности, в качестве которых выступают возбужденные атомы и молекулы, радикалы в плазме, дефекты, создаваемые ионной бомбардировкой на поверхности обрабатываемого материала.
Особенностью плазмо- и ионно-химических процессов обработки материалов является использование холодной плазмы, являющейся неравновесной термодинамической системой. Неравновесность системы определяется повышенной энергией всех или части частиц плазмы. Энергия частиц существенно завышена по сравнению с уровнем, необходимым для эффективного протекания химических реакций. В результате этого возможно одновременное протекание сразу нескольких реакций по различным направлениям с образованием различных продуктов.
Процессы ПХТ и ИХТ многоплановы. Эта многоплановость связана с необходимостью учитывать многочисленные газофазные реакции, обеспечивающие создание в электрическом разряде реактивной плазмы необходимого состава, рассматривать многочисленные гетерогенные реакции на поверхности, осуществляемые реактивными частицами плазмы. Происходящие химические реакции вызываются или сопровождаются различного рода энергетическими воздействиями на реагирующие вещества.
В процессах ПХТ и ИХТ нельзя, как в обычных химических процессах (равновесных), отделить кинетику химических реакций от кинетики физического взаимодействия реактивных частиц плазмы с обрабатываемым материалом. При ионно-химической обработке следует принимать во внимание, что кинетика физического взаимодействия предворяет и во многом определяет кинетику последующего химического взаимодействия.
Скорость химической реакции возбужденных частиц, ионов и радикалов с материалом, как правило, значительно превышает скорость образования этих частиц. Поэтому суммарная скорость химических превращений в процессах ПХТ и ИХТ определяется скоростями образования и расходования этих частиц, т. е. скоростями возбуждения, диссоциации и ионизации. Лимитирующей стадией гетерогенной реакции ПХТ и ИХТ является, в большинстве случаев, стадия переноса.
|
|
|
|
|
|


