 |
Спайностью называется способность кристаллов раскалываться по плоскостям, параллельным действительным граням под действием механических сил.
|
|
|
|
Глава 3. Зависимость физических свойств твердых веществ от строения кристаллов
Физические свойства кристаллов определяются в первую очередь природой химических элементов, входящих в их состав, то есть определяющую роль играет тип химической связи. Также проявление тех или иных физических свойств связано с геометрическим характером структуры, с взаимным расположением атомов в кристаллической структуре веществ, а также с несовершенствами структур реальных кристаллов, отражающих условия их образования. В зависимости от колебаний химического состава физические свойства одного и того же вещества могут варьировать в более или менее широких пределах.
Самой характерной особенностью физических свойств кристаллов является их симметрия и анизотропия. Вследствие периодичности и симметрии внутреннего строения кристаллов в них обнаруживается ряд свойств, невозможных в изотропных телах. Анизотропные физические свойства кристаллов чрезвычайно чувствительны к внешним воздействиям. Поэтому, подбирая и комбинируя те или иные воздействия, можно создавать кристаллы с уникальными, необычными свойствами, которые используются в источниках, приемниках, преобразователях и усилителях различных видов энергии.
Проявление ряда физических свойств, таких как масса, плотность, теплоемкость, температура плавления и др., зависит от межатомных расстояний в структурах кристаллов. В этом случае кристалл можно рассматривать как дискретную среду. Однако в отношении целого ряда макроскопических свойств, таких как тепло- и электропроводность, оптические и другие свойства, можно отвлечься от дискретного строения и рассматривать кристаллическое вещество как сплошную однородную анизотропную среду, и оперировать расстояниями и объемами, значительно превышающими параметры, а, следовательно, и объем элементарных ячеек кристаллических структур. Поэтому с некоторой степенью приближения можно считать, что, поскольку свойства кристалла одинаковы во всем его объеме, во всех его точках, кристалл как однородная среда характеризуется неизменностью физического свойства по отношению к трансляциям. Но поскольку проявление многих физических свойств зависит от направления в кристалле, то кристалл можно считать сплошной анизотропной средой.
|
|
|
Для описания физических свойств кристаллов используют скалярные, векторные и тензорные величины, поэтому и свойства кристаллов подразделяются на скалярныевекторныеи тензорные свойства.
Плотность кристаллов
Плотность вещества (r) – фундаментальное физическое свойства, которое определяется как отношение массы вещества к его объему:, выражается в г/см3 (или в кг/м3).
Зависит плотность от типа кристаллической структуры вещества, его химического состава, коэффициента упаковки атомов, валентностей и радиусов слагающих его частиц.
Изменяется плотность с изменением температуры и давления, так как эти факторы вызывают расширение или сжатие вещества.
С увеличение коэффициента упаковки кристаллической структуры возрастает плотность вещества. Например, при полиморфном переходе углерода графита в алмаз – с изменением координационного числа атомов углерода с 3 до 4 соответственно повышается и плотность от 2,2 до 3,5 г/см3.
Плотность реальных кристаллов обычно меньше, чем расчетная плотность (идеальных кристаллов) из-за присутствия дефектов в их структурах. Плотность алмаза, например, колеблется в пределах 2,7-3,7 г/см3. Таким образом, по уменьшению реальной плотности кристаллов можно судить о степени их дефектности.
|
|
|
Плотность меняется с изменением химического состава вещества при изоморфных замещениях при переходе от одного члена изоморфного ряда к другому.
Твердость и температура плавления кристаллов
Твердость и температура плавления характеризуют прочность кристалла: твердость – механическую, а температура плавления – термическую прочность.
Твердость – это степень сопротивления кристалла внешнему воздействию.
Для приближенного определения твердости пользуются методом, основанном на царапании одного кристалла другим. В 1824 году австрийский минералог Ф. Моос предложил 10-балльную шкалу твердости минералов, которая позволяет приближенно оценить их твердость.
Шкала твердости по Моосу
| Минерал | Относительная твердость по Моосу |
| Тальк Mg3[Si4O10](OH)2 | |
| Каменная соль NaCl | |
| Кальцит CaCO3 | |
| Флюорит CaF2 | |
| Апатит Ca5(PO4)3F | |
| Полевой шпат K[AlSi3O8] | |
| Кварц SiO2 | |
| Топаз Al2[SiO4](F,OH)2 | |
| Корунд Al2O3 | |
| Алмаз C |
Твердость зависит от химического состава кристалла и от его строения: типа структуры, коэффициента упаковки, заряда образующих кристалл ионов. Например, различная твердость двух полиморфных модификаций карбоната кальция – кальцита (3 по шкале Мооса) и арагонита (4 по шкале Мооса) – объясняется различной плотностью их структур: для структуры кальцита с КЧ (Са) = 6 плотность равна 2,72 г/см3, для структуры арагонита с КЧ (Са) = 9 – 2,94 г/см3. В ряду кристаллов с одинаковой структурой твердость возрастает с увеличением заряда и уменьшением размера катиона. Присутствие больших анионов (фторид-иона, гидроксила) или молекул воды понижает твердость. Например, для изоструктурных минералов гематита Fe2O3 и корунда Al2O3 значения твердости составляют 5-6 и 9 соответственно (r (Fe3+) = 0,78  ; r (Al3+) = 0,57
; r (Al3+) = 0,57  ).
).
Изменение температуры плавления кристаллов связаны с изменением их твердости, чем выше твердость, тем больше температура плавления. Увеличение межатомного расстояния при сохранении типа структуры у вещества с одинаковой валентностью атомов влечет за собой, как уменьшение твердости, так и понижение температуры плавления кристаллов (табл.).
| Соединение | Длина связи
M – O, 
| Твердость по школе Мооса | Температура плавления, °С |
| MgO | 2,10 | 6,5 | |
| CaO | 2,40 | 4,5 | |
| SrO | 2,57 | 3,5 | |
| BaO | 2,77 | 3,0 |
|
|
|
При уменьшении валентности катионов происходит те только увеличение твердости, но и температуры плавлении (табл., приведенные вещества имеют сходные межатомные расстояния и одинаковый структурный тип).
| Соединение | Длина связи
M – Э, 
| Твердость по школе Мооса | Температура плавления, °С |
| NaF | 2,31 | 3,5 | |
| MgO | 2,10 | 6,5 | |
| TiC | 2,23 | 8,0 |
Замена 8-электронного иона на 18-электронный практически не влияет на изменение твердости, но значительно уменьшает температуру плавления, например: температура плавления NaCl равна 840 °С, а AgCl – 455 °С (оба вещества кристаллизуются в структурном типе хлорида натрия).
Твердость кристалла также зависит от грани кристалла, например для граней топаза твердость 7,5 соответствует граням пинакоида, а твердость 8 – граням призмы.
Спайность кристаллов
Спайностью называется способность кристаллов раскалываться по плоскостям, параллельным действительным граням под действием механических сил.
В зависимости от легкости раскалывания различают:
· весьма совершенную спаянность;
· совершенную спаянность;
· несовершенную спаянность.
Кристаллы могут раскалываться как в одном, так и в нескольких направлениях.
Ретикулярная плотность
Ретикулярная плотность определяется густотой расположения узлов кристалла в узловой сетке, т. е. это плотность узловой сетки.
Спайность связана с особенностями строения кристаллов, их геометрически характером. Плоскости спайности проходят параллельно сеткам с наименьшей ретикулярной плотностью, и обычно перпендикулярны направлениям более слабых химических связей. Например, между слоями графита, пакетами слюд и др., то есть в гетеродесмических структурах спайность зависит от слабейшего типа связи. В координационных структурах плоскость спайности параллельна атомным сеткам с наименьшей ретикулярной плотностью, с учетом электростатического взаимодействия между атомными плоскостями.
|
|
|
Проиллюстрируем приведенные правила на примере проявления спайности в геометрически подобных структурах сфалерита ZnS и алмаза С (рис. 3.1.). Сравнение расстояний между атомными сетками (010), (110) и (111) показывает, что спайность должна проявляться по (111), поскольку:
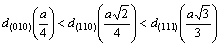 .
.

Рис. 3.1. Расположение атомных сеток в структуре сфалерита ZnS
Ожидаемая спайность реализуется только в структуре алмаза, где связь между атомами углерода одного типа – ковалентная неполярная. В структуре сфалерита на этом расстоянии располагаются слои разных атомов – цинка и серы. Силы связи между такими слоями большие, чем силы связи между слоями, находящимися ближе друг к другу, но на которых находятся одновременно оба типа атомов и которые являются более валентно насыщенными. Поэтому, несмотря на то, что d (110) < d (111), плоскость спайности в сфалерите параллельна (110).
|
|
|


