 |
Абсорбционная очистка газов от оксида углерода
|
|
|
|
В качестве абсорбента для поглощения СО применяют медноам- миачные растворы (МАР). В процессе абсорбции СО под высоким дав- лением поглощается в противоточном абсорбере раствором комплекс- ного медно-аммиачного соединения. Чаще других используются рас- творы формиата, карбоната или ацетата меди. Раствор имеет слабоще- лочной характер, вследствие чего одновременно поглощается и диок- сид углерода. Регенерацию проводят нагревом, под действием тепла комплекс разлагается и оксиды углерода полностью выделяются.
В абсорбере протекают следующие основные реакции: [Cu(NH3)2]+ + CO + NH3 = [Cu(NH3)3CO]+;
2NH4OH + CO2 = (NH4)2CO3 + H2O; (NH4)2CO3 + CO2 + H2O = 2NH4HCO3.
Ионы двухвалентной меди не могут связывать оксид углерода, но их присутствие (до 20 %) необходимо, т.к. они препятствуют выпаде- нию металлической меди:
2Cu+ ® Cu + Cu++.
Степень очистки зависит от парциального давления СО над реге- нерированным раствором и общего давления газа.
Чтобы улучшить условия очистки, абсорбцию проводят при вы- соком давлении - 32 МПа и низкой температуре - около 0 оС. Десорб- цию ведут при атмосферном давлении и температуре около 60 оС. Бо- лее высокие температуры приводят к интенсивному выделению ам- миака. Схема установки приведена на рис. 6.3.
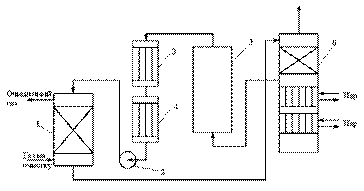
Рис. 6.3. Схема установки медно-аммиачной очистки газов
1 - абсорбер; 2 - насос; 3 - водяной холодильник; 4 – аммиачный холодильник
5 - емкость; 6 - десорбер
Газ из цеха компрессии под давлением 32 МПа поступает в скрубберы, орошаемые МАР.
Состав азотводородной смеси (%): Н2 70; N2 23-26; CO 3-5; СО2
1,5-2.
После очистки газ, содержащий не более 40 см3/м3 СО и до 150 см3/м3 СО2, подается в скрубберы, орошаемые аммиачной водой (на схеме не показан), где он освобождается от остальной СО2, и затем в цех синтеза NH3. Регенерацию МАР проводят путем снижения Р и на- гревания раствора в 6. В результате предварительного дросселирова- ния МАР до 0,8 МПа из него удаляются растворенные Н2 и N2. При дальнейшем дросселировании до 0,1 МПа и нагревании раствора до 45- 50 оС происходит разложение медноаммиачного комплекса и выделе- ние СО.
|
|
|
Для нагревания отработанного раствора до 60 оС служит отходя- щий регенерированный раствор, а для окончательного нагрева до 80 оС
- пар. Регенерированный раствор охлаждают последовательно посту- пающим отработанным раствором, оборотной водой в теплообменнике 3 и испаряющимся жидким NH3 в холодильнике 4, после чего регене-
рированный раствор при 10 оС направляют на абсорбцию. В случае не-
обходимости проводят окисление Cu+ продуванием воздуха через ре- генерированный раствор.
Для разложения углекислого аммония при атмосферном давлении раствор нагревают не выше 80 оС. Поскольку при более высокой тем- пературе медноаммиачный комплекс разлагается, для более полной ре- генерации вторую ее ступень проводят в вакууме.
Чтобы предупредить выделение металлической меди при регене- рации аммиачного раствора формиата или ацетата меди, к нему добав- ляют свежую муравьиную или уксусную кислоту.
Окончательную очистку водорода, идущего на синтез аммиака, от оксида углерода производят промывкой газа жидким азотом при тем- пературе порядка -190 оС под давлением 20-25 атм. Этот метод отно- сится к низкотемпературным процессам очистки газов и основан на физической абсорбции СО.
Процесс очистки состоит из трех стадий: предварительного охла- ждения и сушки исходных газов; глубокого охлаждения этих газов и частичной конденсации их компонентов; отмывки газов от оксида уг- лерода, метана и кислорода жидким азотом в промывной колонне. Хо- лод, необходимый для создания в установке низких температур, обес- печивается аммиачным холодильным циклом, а также рекуперацией холода обратных потоков азотноводородной фракции и азотного цикла высокого давления.
|
|
|
Характерным для этого процесса является отсутствие стадии де- сорбции поглощенной примеси из абсорбента: часть испарившегося азота примешивается к водороду и используется в ступени синтеза. Т.к. промывка ведется чистым абсорбентом, то может быть достигнута любая степень очистки.
Особенность процесса такова, что его можно рассматривать не как абсорбцию, а как ректификацию смеси N2 – СО в токе инертного газа - водорода.
Имеются данные о равновесии в тройной системе Н2-N2-CO, ана- лиз которых показывает, что Н2 практически не влияет на раствори- мость СО в жидком азоте. Поэтому расчет процесса можно проводить по данным для двойной смеси. Полученная по этим данным зависи- мость растворимости СО в жидком азоте от давления СО над раство- ром описывается законом Генри.
Минимальный расход азота для промывки 150 м3 газа, содержа- щего 6 % СО возможен при Р=2-2,6 МПа и равен 12-13 см3.
Температура оказывает очень большое влияние на расход жидко- го азота и на высоту колонны.
Расход азота, как и для других процессов физической абсорбции, практически не зависит от концентрации СО и уменьшается почти пропорционально увеличению общего давления.
|
|
|


