 |
Задача 29. Константа уравнения Штаудингера
|
|
|
|
Уравнение Штаудингера имеет вид:
[η]=KMα.
Отсюда: [η]=1,85∙10-5∙300000∙0,56 = 3,108 м3/кг.
Задача 30 Константа скорости реакции H2… при 714 К ровна 0,111 моль/с/л
По условию задачи константа скорости реакции имеет единицы измерения [концентрация-1× время-1]. Следовательно, реакция образования газообразного иодоводорода из простых веществ является реакцией второго порядка.
Кинетическое уравнение скорости реакции второго порядка имеет вид:
v = k × c(H2) × c(I2)
Исходя из уравнения реакции, определим количество каждого реагента, необходимое для образования 0,2 моль иодоводорода.
Рассчитаем количество исходных реагентов, оставшееся к моменту времени, когда в реакционной смеси образуется 0,2 моль НI.
n(Н2)вст=n(I2)вст=0,5× n (НI)обр=0,1 моль.
n(Н2)ост=n(I2)ост=2 – 0,1=1,9 моль.
с(Н2)=с(I2)= 1,9:2=0,95 моль/л
Рассчитаем скорость реакции:
v = 0,111 л/(моль·с)·0,952 моль2/л2 = 0,1 моль/(л·с)
Ответ: 0,1 моль/(л·с).
Задача 31 Напишите формулу мицеллы коллоидного раствора сульфата бария
на поверхности ядра будут адсорбироваться сульфат-анионы, образующие слой потенциалопределяющих ионов.
[(mBaSO4)nSO42-] - агрегат
Заряженная поверхность агрегата притягивает из раствора катионы натрия, которые образуют два слоя противоионов: адсорбционный, жестко связанный с поверхностью, и диффузионный, частицы которого могут обратимо переходить в раствор. Совокупность ядра и двух адсорбционных слоев называется гранулой, которая собственно и является коллоидной частицей.
{[(mBaSO4)nSO42-]2(n-x)Na+} - гранула
Гранула и диффузионный слой противоионов образуют мицеллу.
{[(mBaSO4)nSO42-]2(n-x)Na+}-2x2xNa+ - мицелла
Задача 32 Определите направления протекания реакции… при 298 К и….
ΔG0р-ции=RT(lnC(2HI)/(c(H2)×c(I2))-ln Kравн)- уравнение изотермы Вант - Гоффа;
|
|
|
ΔG0р-ции=8,31×298(ln 2/(0,01×0,01) – ln 2)=21091 Дж/моль=21,091 кДж/моль.
Ответ: ΔG0р-ции>0, поэтому реакция в прямом направлении не может идти самопроизвольно.
Задача 33 Определить молекулярную массу синтетического каучука
Уравнение Марка – Куна – Хаувинка имеет вид [η]=KMα.
Отсюда: 0,0215 = 1,85∙10-5∙М1,56.
М1,56=1162,2
1,56lgМ =lg1162,2
М = 91,2 г/моль
Ответ: М = 91,2 г/моль.
Задача 34 Для проведения исследований были взяты равные массы…
Период полураспада цезия 137 составляет 30 лет, а циркония 95 – 65 суток.
Закон радиоактивного распада:
m = m0∙2-t/T, где Т – период полураспада.
Определим время, за которое 99% циркония подвергнется распаду:
0,01 = 2-t/65
t = 432 суток = 1,18 лет.
Для цезия за это время останется: m/m0 = 2-1,18/30 = 0,97.
Таким образом, распадётся ок. 3%
Ответ: 97%
Для коагуляции 100мл золя гидроксида железа понадобилось добавить 10,5 МЛ 1н раствора КС l. Определите порог коагуляции золя хлоридом калия.


36.Разложение спазмолитина в растворе является реакцией первого порядка с энергией активации 75кДж/моль. Период полупревращения при 200С равен 103ч. Рассчитайте время, за которое разложится 25% спазмолитина при 370С.
Решение:
Т1=20+273=293 К; Т2=37+273=310 К.
Рассчитаем константу скорости k1 при Т1, воспользовавшись уравнением 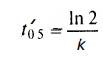 после преобразования относительно k:
после преобразования относительно k:

Для расчета константы скорости k2 при Т2 воспользуемся уравнением Аррениуса для двух температур 


37. Определите, к какому электроду должны перемещаться частицы золя, получаемого по реакции при небольшом избытке Н2 S.
2H 3 AsO 3 +3H 2 S=As 2 S 3 +6H 2 O
Решение:
Потенциал определяющими ионами в данном случая могут быть ионы S2-, так как в состав агрегата входят ионы серы. Состав адсорбционного слоя могут входить ионы К+. Ионы К+ образуют диффузный слой. Таким образом, схематическое строение мицеллы золя можно выразить следующей формулой:
|
|
|
{[(As2S3)m·n S 2-]· 2(n-x)Н+}-2х 2x Н+
Частица имеет отрицательный заряд, - следовательно, движение частиц золя направлено к аноду.
|
|
|


