 |
Основные тенденции в развитии потребления магния в мире.
|
|
|
|
Основные тенденции в развитии потребления магния в мире.
В последние годы за рубежом положение магния как одного из масштабных промышленных металлов упрочнилось: в 1980 году впервые в мирное время был превзойдён максимальный уровень производства магния военного 1943 года. Несмотря на отдельные спады, обусловленные общей неблагоприятной коньюктурой, потребление магния оставалось стабильным, хотя цены на него и выросли в 1, 9 раза.
Самым крупным производителем и потребителем первичного магния за рубежом остаются США, но их доля в мировом потреблении за 1975-85гг сократилось с 51, 7% до 41, 5%. Норвегия и США – крупнейшие экспортёры магния: по 36-45 тыс. тонн в год. США являются также крупнейшим производителем магния из вторичного сырья.
Второе место по объёма потребления магния занимает Западная Европа (30%). Потребление магния в Японии оценивается на уровне 20-25 тыс. тонн в год, из которых 69% расходуется в производстве алюминиевых сплавов и высокопрочного чугуна, на отливки из магниевых сплавов – 4, 9%.
Магний за рубежом используется во многих отраслях промышленности. Всё разнообразие направлений использования можно условно разделить на 3 группы:
1. Применение магния в производстве алюминиевых сплавов, в которых добавляют от 0, 5% до 10% магния. Алюминиевые сплавы, содержащие магний, отличаются высокой удельной прочностью, коррозийной стойкостью и хорошо обрабатываются резанием.
2. Приготовление сплавов конструкционного назначения на основе магния. Содержание магния в таких сплавах 90-98%. Деформируемые магниевые сплавы и литые заготовки из них находят применение в ряде отраслей промышленности, прежде всего в аэрокосмической промышленности, далее идут военная и автомобильная.
|
|
|
3. Использование магния в качестве химического реагента в чёрной и цветной металлургии для восстановления Be, Ti, U, Zr, Hf и др. металлов, в химии (в основном в реакции Гриньяра), также в качестве расходуемых анодов для катодной защиты от коррозии стальных конструкций, подземных трубопроводов и резервуаров. Магний в этих процессах полностью расходуется. Лом и отходы не образуются, в отличии от первых двух групп, где он может повторно использоваться в виде вторичных сплавов.
В условиях дефицита магния также актуальной является задача более рационального использования имеющихся ресурсов металла, сокращение потерь его на всех этапах переработки и использования. Например, более эффективно может быть использован вторичный магниевый сплав типа МА9С6 для легирования алюминиевых сплавов взамен первичного металла. Предпочтительнее выглядит и прямое использование отходов из магниевых сплавов в виде брикетов стружки взамен чушкового металла, например, для десульфурации или модифицирования чугуна, производстве модификаторов типа железо-кремний-магний.
Использование магния в аппаратах космической и авиационной техники, автомобилестроении, различных агрегатах и ответственных приборах предъявляя особые требования к технологии производства литья из магниевых сплавов. Потребность народного хозяйства в магнии и магниевых сплавах значительно превышает возможность их производства. Это ставит перед металлургами, технологами и разработчиками новые проблемы повышения качества литья, использования лома и стружки, создание безотходных и малоотходных технологий производства. Обостряются вопросы экологии.
9. ЖЕСТКОСТЬ ВОДЫ
Природная вода, проходя через известковые горные породы и почвы, обогащается солями кальция и магния и становится жёсткой. В жёсткой воде при стирке белья увеличивается расход мыла, а ткань, впитывая соли, становится жёлтой и быстро ветшает. Нерастворимые соли кальция и магния осаждаются на внутренних стенках паровых котлов и трубопроводов. В жёсткой воде хуже и дольше варятся овощи.
|
|
|
Различают временную и постоянную жёсткость воды. При наличии временной жёсткости воды нагрев её приводит к выпадению осадков карбонатов CaCO3 и MgCO3. Временная жёсткость вызвана присутствием в воде гидрокарбонатов Mg(HCO3)2. Такая жёсткость устраняется кипячением воды:

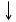 Mg(HCO3)2 = MgCO3 + H2O + CO2
Mg(HCO3)2 = MgCO3 + H2O + CO2
Постоянная жёсткость обусловлена другими солями кальция и магния, она не устраняется кипячением воды. Осадки малорастворимых и практически нерастворимых солей (CaSo4, CaSiO3, MgSiO3)могут выпадать вследствие следующих причин:
1. Повышение концентрации солей при выпаривании воды;
2. Понижение растворимости солей при нагревании (если соль обладает отрицательным температурным коэффициентом).
Для умягчения воды из неё необходимо удалить все соли кальция и магния, как Mg(HCO3)2, так и MgSO4, MgCl2 и др. Это достигается обработкой природной воды различными осадителями:
1. Действие известковой воды
 |

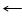 Mg(HCO3)2 + Ca(OH)2 CaMg(CO3)2 + 2H2O,
Mg(HCO3)2 + Ca(OH)2 CaMg(CO3)2 + 2H2O,


 Ca(HCO3)2 + Ca(OH)2 2CaCO3 + 2H2O;
Ca(HCO3)2 + Ca(OH)2 2CaCO3 + 2H2O;
2. Действие соды
 |
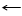
 MgSO4 + Na2CO3 MgCO3 + Na2SO4,
MgSO4 + Na2CO3 MgCO3 + Na2SO4,
 |

 3CaCl2 + 2Na3PO4 Ca3(PO4)2 + 6NaCl.
3CaCl2 + 2Na3PO4 Ca3(PO4)2 + 6NaCl.
Отметим, что один из указанных выше осадков, а именно карбонат магния – кальция CaMg(CO3)2, отвечает по составу природному веществу – минералу доломиту, также широко распространённому, как и кальцит. Он является важнейшим природным источником магния наравне с карналлитом KMgCl3*6H2O.
В химической лаборатории и в промышленности используется полностью обессоленная вода (для питья непригодна). Для этого природную воду подвергают перегонке (дистилляции). Такая дистиллированная вода является мягкой, подобно дождевой воде.
С практической точки зрения (например при эксплуатации паросиловых установок) существенна именно форма образующихся осадков. Накипи отлагаются на поверхностях нагрева, снижая экономичность установки и могут привести к перегреву стенки (поверхности нагрева). Шламы – рыхлые осадки – выпадают в объёме воды и не опасны, поскольку могут быть удалены. Поэтому все методы борьбы с жёсткостью воды направлены либо на очистку воды от ионов солей жёсткости, либо на искусственное осаждение солей жёсткости в форме шламов.
|
|
|
|
|
|


