 |
1.3.2 Катализаторы переэтерификации жиров
|
|
|
|
1. 3. 2 Катализаторы переэтерификации жиров
Перемещение жирных кислот из одной молекулы в другую или из одного положения в другое происходит в присутствии катализаторов.
Наибольшее распространение получили щелочные катализаторы: натрий, калий и некоторые соединения этих металлов. В заводской практике чаще всего используют соединения натрия.
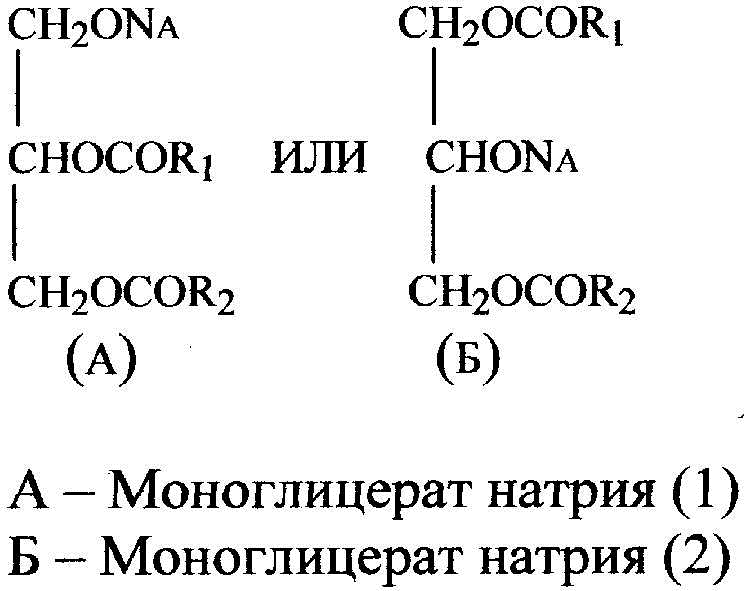
Установлено, что в результате воздействия натриевого катализатора на молекулу глицерида сначала образуется моноглицерат натрия с различным положением его в молекуле:

Глицерат натрия является истинным катализатором переэтерификации. Ниже приводится одно из уравнений, по которому протекает реакция переэтерификации.
Как видно из уравнения, в результате реакции натрий и радикалы кислот поменялись местами. Образовались новые триглицерид и моноглицерат натрия. Новый моноглицерат натрия снова вступает в реакцию с этим же или другими триглицеридами, и переэтерификация продолжается до тех пор, пока радикалы жирных кислот не распределятся в молекулах глицеридов более или менее равномерно [3].
1. 3. 3 Требования к основному сырью
Жиры и масла, используемые в процессе переэтерификации, должны отвечать следующим основным требованиям: влажность не более 0, 01 %; содержание свободных жирных кислот не более 0, 1 %; перекисное число не более 0, 05 % йода.
Переэтерификации подвергают главным образом смеси высокоплавких жиров (животные жиры, пальмовое масло, пальмовый стеарин, гидрированные жиры с температурой плавления не ниже 34 °С и т. п. ) с жидкими растительными маслами [4].
1. 3. 4 Процесс переэтерификации
Процесс переэтерификации может быть осуществлен несколькими способами, такими как щелочными, кислотными катализаторами, биокатализаторами, гетерогенными катализаторами и использование спирта в сверхкритическом состоянии. Общая реакция показана ниже
Растительное масло + метанол(этанол) → биодизель + глицерин
|
|
|
В щелочном процессе в качестве катализатора ) используется гидроксид натрия (NaOH) или гидроксид калия (КОН), а также метанол или этанол. Первоначально, в ходе процесса, формируется реакция катализатора с алкоголем, а затем смесь реагирует с любым растительным маслом, и формируются биодизель и глицерин. Глицерин более плотный оседает на дне, а биодизель всплывает. Этот процесс является наиболее эффективным и наименее агрессивный из всех процессов и скорость реакции достаточно высока даже при низкой температуре 60 ° C. Здесь возникает риск образования свободной кислоты или загрязнение воды и образование мыла, поэтому, трудный процесс разделения. (Ma и Ханна, 1999; Фукуда и др., 2001;. Барнвал и Шарма, 2005).
Второй традиционный способ производство биодизеля - это использование кислотного катализатора. Любая минеральная кислота может быть использована для ускорения процесса; наиболее часто используемые кислоты: серная кислота и сульфокислота. Хотя доходность высока, кислоты являются коррозийными и могут привести к повреждению оборудования и наблюдалась низкая скорость реакции. (Фридман и др.., 1984).
Недавно было установлено, что ферменты, такие как липаза могут быть использованы в качестве катализатора процесса переэтерификации путем иммобилизации их на подходящую поверхность. Преимущество иммобилизации является в том, что фермент можно повторно использовать без разделения. Кроме того, рабочая температура этого процесса является низкой (50 ° C) по сравнению с другими методами. К недостаткам можно отнести торможение реакции при использовании метанола, а также сюда следует отнести то, что фермент являются дорогим (Нельсон и др., 1996;.. Симада и др., 2002). Гетерогенные катализаторы такие как аморфный цирконий, титан, алюминий, калий, легированные цирконием также стали распространены в качестве катализатора переэтерификации растительных масел. Продолжаются исследования, чтобы решить проблемы, возникающие в этом процессе, такие как истощение катализатора и достижения более высокой конверсии (Фурута и соавт., 2006). [5]
|
|
|
Процесс переэтерификации может быть осуществлен даже без катализатора, но со значительным увеличением температуры. Доходность очень низкая при температурах ниже 350 ° C и, следовательно, стали необходимы более высокие температуры. Однако при температуре выше 400 ° C произошла термическая деструкция эфиров (Демирбас, 2006). Недавно было установлено, что спирт в сверхкритическом состоянии производит лучший выход и исследователи провели опыты этого процесса с помощью метанола в сверхкритическом состоянии. Эффективность процесса может быть увеличена с помощью оксида кальция в качестве катализатора (Демирбас, 2006). [5]
Из всех указанных выше методов для производства биодизеля, только щелочной процесс осуществляется в промышленных масштабах. Он является экономически выгодным и высокоэффективным. Но проблемы возникают в последующих операциях, включающих разделение катализатора и непрореагированного метанола из биодизеля. Удаление катализатора включает в себя множество осложнений и биодизель требует повторной очистки для достижения необходимого качества. На рис. 2 и 3 показаны стадии, необходимые для щелочных и ферментативных производств.
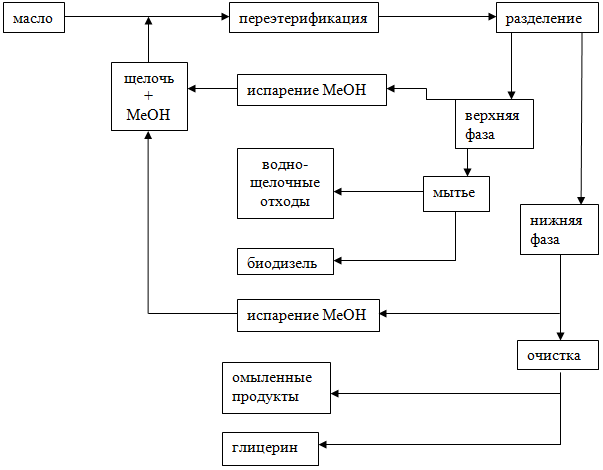
Рисунок 1 - Производство биодизельного топлива путем щелочного процесса

Рисунок 2 - Производство биодизельного топлива путем ферментативного процесса
Производство биодизеля с использованием биокатализатора устраняет недостатки щелочного процесса и делает чистый биодизель (Фукуда и соавт., 2001 ). Этот метод производства биодизеля был запатентован Хаасом (1997). Но этот процесс еще не был реализован в промышленном масштабе в связи с определенными ограничениями, такие как торможение реакции метанолом, истощение активности и высокая стоимость фермента. [1]
|
|
|


