 |
Химические свойства водорастворимых витаминов и их анализ
|
|
|
|
Витамины группы В1
Тиохромная проба
Препараты тиамина легко окисляются в щелочной среде, образуя тиохром, который в УФ-свете обладает характерной синей флюоресценцией, исчезающей при подкислении и вновь возникающей при подщелачивании. Эта реакция известна под названием тиохромной пробы и является специфической для препаратов группы тиамина:

|

|
Тиохромную пробу используют для качественного и количественного флуориметрического анализа витамина В1 в лекарственных препаратах, растительном сырье и пищевых продуктах.
Реакция с диазореактивом
Для проведения этой реакции обычно используют диазореактив, полученный из сульфаниловой кислоты.
Тиамин в нейтральной или слабощелочной среде реагирует с солями диазония с образованием окрашенных в красный цвет триазенов:

|

|
Реакция применяется для спектрофотометрического количественного анализа тиамина в растворах.
Витамины группы В2
Реакция восстановления
Рибофлавин, принимая два атома водорода, легко восстанавливается до лейкорибофлавина. При этом нарушается сопряженная система связей, что сопровождается исчезновением окраски. Лейкорибофлавин легко окисляется (в организме под действием НАД+) до рибофлавина. Благодаря этим химическим свойствам коферменты, образующиеся из рибофлавина – ФМН и ФАД, участвуют в окислительно-восстановительных процессах, происходящих в клетке:
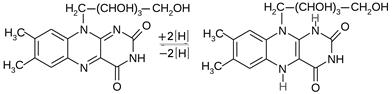
| |
| Рибофлавин (желтого цвета) | Лейкорибофлавин (бесцветный) |
Реакция с солями тяжёлых металлов
Рибофлавин проявляет очень слабые кислые свойства, но образует устойчивые окрашенные соли с ионами тяжелых металлов. При добавлении к водному раствору рибофлавина раствора нитрата серебра или ацетата ртути образуются окрашенные соединения розового или оранжевого цвета, соответственно:
|
|
|
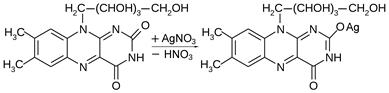
| |
| Рибофлавин (желтого цвета) | Серебряная соль рибофлавина (розового цвета) |
Реакции с солями серебра или ртути используются для качественного и количественного спектрофотометрического анализа рибофлавина.
Витамины группы В6
Реакция с хлоридом железа (III)
Все представители группы витаминов В6 проявляют свойства, характерные для фенолов, в частности они дают общую реакцию подлинности на фенолы с хлорным железом, легко вступают в реакции электрофильного замещения по свободному пара -положению к фенольному гидроксилу. При этом образуется комплексная соль фенолята железа красного цвета:
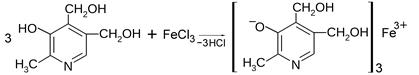
| |
| Пиридоксин | Комплексная соль фенолята железа красного цвета |
Реакция с диазореактивом
Также легко пиридоксин вступает в реакцию азосочетания с солями диазония с образованием окрашенных в красный цвет азокрасителей:
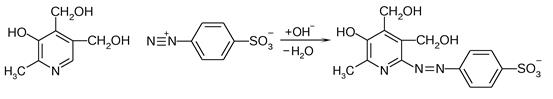
| |
| Пиридоксин | Окрашенное в красный цвет соединение |
Витамины группы РР
Никотиновая кислота проявляет выраженные и кислые, и оснóвные свойства; амид никотиновой кислоты обладает только оснóвными свойствами. Эти различия в свойствах также используются для отличия одного препарата от другого.
Реакция с солями тяжёлых металлов
Никотиновая кислота образует малорастворимые соли с ионами тяжелых металлов. Например, при реакции с сульфатом меди образуется осадок синего цвета:
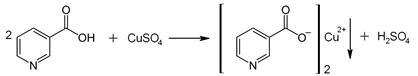
| |
| Пиридоксин | Осадок синего цвета |
В присутствии роданид-ионов образуется комплексная соль зеленого цвета:
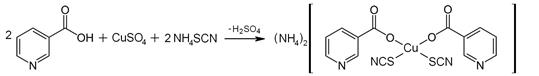
| |
| Пиридоксин | Комплексная соль зеленого цвета |
Витамин С
Аскорбиновая кислота является сильным восстановителем. Она окисляется ионами серебра и меди, йодом, красной кровяной солью, нитратами, кислородом и др. При окислении аскорбиновой кислоты образуется дегидроаскорбиновая кислота:
|
|
|

| |
| Аскорбиновая кислота | Дегидроаскорбиновая кислота |
|
|
|


