 |
δ3% Zr ↔ γ1%Zr + Ж8%Zr.
|
|
|
|
δ 3% Zr ↔ γ 1%Zr + Ж8%Zr.
При температуре 1582оC происходит перитектическое превращение по реакции
Ж13%Zr +(ZrFe2)27%Zr ↔ (ZrFe3)25%Zr,
где (ZrFe2) – фаза переменного состава на основе устойчивого химического соединения.
Температура δ ↔ γ полиморфного превращения – 1392 оС, растворимость циркония в γ -железе приближается к 0 при 900 оС. Температура плавления железа – 1538 оС, устойчивого химического соединения ZrFe2 – 1673 оС. 22. СИСТЕМА Sn – V (ат. %). При температуре 1500 оС происходит монотектическое превращение по реакции
Ж 18, 8% V ↔ (SnV3)25% Sn + Ж 4%V
При температуре 1600оC происходит перитектическое превращение по реакции
Ж 48% Sn +(V)16%Sn ↔ (SnV3)25% Sn
При температуре 756 оC в результате перитектического превращения образуется Sn3V2 по реакции
Ж 0, 1% V + (SnV3)25% Sn ↔ (Sn3V2)40% V
Температура плавления ванадия – 1910 оС. Растворимость олова в ванадии при 600 оС – 11%.
23. СИСТЕМА Hf – Th (ат. %). При температуре 1600оС происходит метатектическое превращение по реакции
(β -Hf)3% Th ↔ (α -Hf)1, 5%Th + Ж43% Th.
При температуре 1450 оC происходит эвтектическое превращение по реакции
Ж31, 6% Hf ↔ (α -Hf)1, 5%Th + (β -Th)17%Hf
При температуре 1295 оC происходит эвтектоидное превращение по реакции
(β -Th)11, 5%Hf ↔ (α -Hf)1, 5%Th + (α -Th)6%Hf
При температуре 1000оС растворимость тория в гафнии снижается до 0, 5 %, гафния в тории – до 4%. Температура плавления гафния – 2231 оС, тория – 1755 оС. Температура полиморфного превращения (β -Hf) ↔ (α -Hf) – 1740 оС, (β -Th) ↔ (α -Th) – 1360 oC.
24. СИСТЕМА Bi – S (ат. %). При температуре 727 оС происходит монотектическое превращение по реакции
Ж33%Bi ↔ Ж0, 5%Bi + (Bi2Sn3)40% Bi
При температуре 270 оC протекает вырожденное перитектическое превращение по реакции
|
|
|
Ж0, 1%Sn + (Bi2Sn3)40% Bi ↔ Bi
При температуре 115 оС в результате вырожденного эвтектического превращения образуются Bi2Sn3 и сера. Температура плавления висмута – 268 оС, серы – 115, 2 оС, устойчивого химического соединения Bi2Sn3 – 1118 оС
25. СИСТЕМА Cu – Se (ат. %) в области сплавов Cu2Se (36% Se) – Se. При температуре 523 оС происходит монотектическое превращение с образованием фазы переменного состава на основе химического соединения Cu2Se по реакции
Ж47%Сu ↔ Ж2%Cu + (Cu2Se)38% Se
При температуре 377 оС происходит перитектическое превращение по реакции
Ж1%Cu + (Cu2Se)37% Se ↔ (CuSe)50% Se
При температуре 332 оС происходит еще одно перитектическое превращение по реакции
Ж0, 5%Cu + (CuSe)50% Se ↔ (CuSe2)33% Se
При температуре 250 оC концентрация селена в фазе перерменного состава (Cu2Se) изменяется до 36, 5%, меди в жидкой фазе – 0, 03 %. Температура плавления устойчивого химического соединения Cu2Se – 1130 оС.
III. ПРИМЕРЫ ПОСТРОЕНИЯ И РАЗБОРА
ДИАГРАММ ДВУХКОМПОНЕНТНЫХ СИСТЕМ
3. 1. Пример построения диаграммы с нонвариантным эвтектическим превращением
Рассмотрим диаграмму системы Pb - Sb. При 250оС в сплаве с 17, 5% Sb протекает эвтектическое превращение с образованием твердого раствора α (6 ат. % Sb, остальное – Pb) и β (2 ат. % Pb, остальное – Sb). При 20 оС растворимость в обоих растворах практически равно нулю. Температура плавления свинца – 327 оС, сурьмы – 631 оС.
Для построения диаграммы по описанию выбираем масштаб по оси температур и концентраций (рис. 3. 1. ). Намечаем линию, соответствующую эвтектическому превращению (пунктирная линия) и точки (C, E и D), соответствующие равновесным фазам нонвариантного эвтектического превращения. Отмечаем температуры плавления компонентов и точки, соответствующие минимальной растворимости компонентов в α - и β -фазах при 20 оС.

Рис. 3. 1. Схема построения диаграммы равновесия системы Pb-Sb c эвтектическим превращением
|
|
|
Строим линию ликвидуса АЕВ соединяя плавной линией точки плавления свинца и сурьмы с точкой Е. Затем строим линию солидуса АСЕDВ, соединяя точки А и В (температуры плавления компонентов) с точками С и D, проведя через точки С, Е и D горизонтальную линию эвтектического превращения. Затем проводим линии сольвуса – линии ограниченной растворимости в твердом состоянии сурьмы в свинце ( Сс ) и свинца в сурьме( Dd ).
3. 2. Пример построения диаграммы с нонвариантным
перитектическим превращением
Построение диаграммы Cu – La в области сплавов LaCu5 - LaCu2 с нонвариантными перитектическим и эвтектическим превращениями. При 785 оС происходит перитектическое превращение по реакции (LaCu5)17% La + Ж ↔ (LaCu4) 20% La. При 723 оС происходит эвтектическое превращение по реакции Ж27% La ↔ LaCu4 + (LaCu4) 33% La.
Температуры плавления устойчивых химических соединений LaCu5 и LaCu2 соответственно равны 913 и 834 оС.
Построение начинаем с выбора масштаба осей температуры и концентрации (рис. 3. 2).
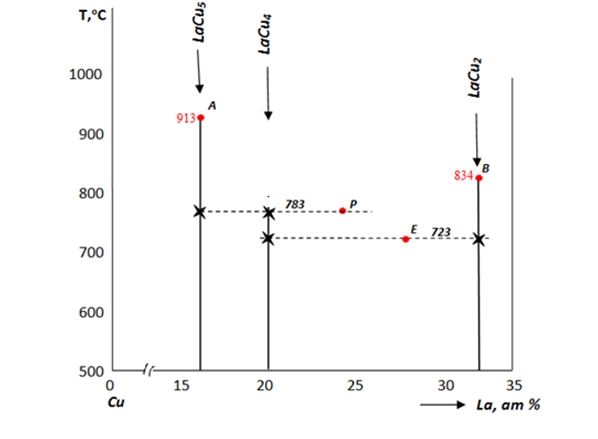
Рис. 3. 2. Схема построения диаграммы равновесия системы Cu-La с перитектическим и эвтектическим равновесием
Затем проводим вертикальные линии, соответствующие химическим соединениям LaCu5, LaCu4и LaCu2. Отмечаем температуры плавления устойчивых химических соединений и намечаем линии нонвариантных превращений. Отмечаем перитектическую ( Р ) и эвтектическую ( Е ) точки. Соединяем плавными линиями точки ликвидуса А, Р, Е, В. Проводим горизонтальные линии перитектического и эвтектического превращения и вертикальные лини, соответствующие химическим соединениям. Указываем фазовый состав во всех областях.
|
|
|


