 |
Применение соединений молибдена в фармации
|
|
|
|
Некоторые соединения молибдена применяются в анализе. Молибдат аммония (NH4)2MoO4 используется как аналитический реактив на фосфор: в присутствии концентрированной азотной кислоты, образуется желтый осадок аммониевой соли гетерополифосфорномолибденовой кислоты (NH4)3 [P(Mo12O40)]´6H2O.
Вопросы и задачи для самоподготовки:
1. В чем особенность строения валентного слоя электронов атомов хрома и молибдена?
2. Какие степени окисления возможны, а какие более устойчивы для хрома и молибдена?
3. Как изменяются кислотно-основные свойства в ряду гидроксидов хрома (II), (III), (VI)?
4. Объясните, почему в растворе, содержащем ион гексааквахрома (III) среда кислая? Что произойдет с этим ионом, если рН увеличить до12?
5. Что произойдет, если раствор K2Cr2O7 добавить к подкисленным растворам, содержащим: а)Cl-,Br-,I--ионы б)NO2- ион в)SO32-ион г)H2O2? Напишите уравнения реакций, расставьте коэффициенты, используя метод ионно-электронного баланса?
6. Напишите уравнения реакций, при помощи которых можно осуществить следующие превращения:
Cr2(SO4)3 ® Cr(OH)3 ® Na2CrO4 ® Na2Cr2O7 ® Cr(OH)3 ® [Cr(OH)4]- ®Cr(OH)3
Опишите реакцию обнаружения соединений Cr(VI) с помощью серной


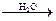 SiF4 + O2
SiF4 + O2