 |
Контрольные вопросы. Лекция 29. Моноклональные антитела, области применения. План лекции
|
|
|
|
Контрольные вопросы
1. Важные области использования методов иммунобиотехнологии.
2. Области применения гибридом.
3. Метод гибридомной технологии.
Лекция 29
Моноклональные антитела, области применения
Форма проведения лекции: проблемная
План лекции
1. Моноклональные антитела.
2. Области применения моноклональных антител – медицинская и ветеринарная диагностика, терапия.
1. Лекарственные вещества, проявляющие высокую активность при тестировании in vitro (обычно в культуре клеток), зачастую оказываются значительно менее эффективными in vivo. Кажущееся снижение их активности объясняется тем, что они не достигают органа или клетки-мишени в нужной концентрации. Увеличение дозы принимаемого препарата не решает проблему, поскольку при этом часто возникают побочные эффекты. Более того, чтобы избежать этих эффектов, многие терапевтические средства заведомо вводят в дозах, не достигающих оптимальных, что дополнительно снижает их эффективность. Для облегчения доставки лекарственного вещества к месту его действия используют несколько приемов:
· заключают его в липосомы, липидная оболочка которых имеет высокое сродство к нужным органам;
· встраивают гены специфических токсинов в инфильтруюшие опухоль лимфоциты, которые высвобождают эти токсины непосредственно в опухоли;
· присоединяют молекулы лекарственных веществ к моноклональным антителам, специфичным по отношению к белкам, на
ходящимся на поверхности строго определенных клеток, напри
мер опухолевых (рис. 9, а);
· используют лекарственные вещества в неактивной форме,
переводя их в активное состояние при помощи ферментов. Чтобы
такое превращение происходило только вблизи клетки-мишени,
фермент присоединяют к моноклональному антителу, специфич
ному к поверхностному антигену этой клетки (рис. 9, б).
|
|
|
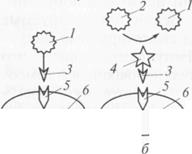 Рис. 9. Использование моноклональных антител для целевой доставки лекарственных веществ:
Рис. 9. Использование моноклональных антител для целевой доставки лекарственных веществ:
1-лекарственное вещество;
2-инертная форма лекарственного вещества;
3-моноклональное антитело; 4-фермент;
5-поверхностный белок; 6-клетка-мишень
Несмотря на весьма существенные достижения применения моноклональных антител в терапии разных заболеваний, имеются все-таки и некоторые ограничения их использования в клиниках. Прежде всего они как гибридомные продукты могут быть контаминированы генетическим материалом ретровирусов, так как все миеломы как опухолевые партнеры гибридизации имеют в геноме гены ретровирусов, являющиеся онкогенными и соответственно опасными для человека. Поэтому все препараты моноклональных антител обязательно тестируются на отсутствие вирусного генетического материала.
Для получения антител используют мышей, морских свинок, кроликов, кур, овец, коз, лошадей, которым делают инъекции антигена. В присутствии стимуляторов иммунного ответа в сыворотке крови накапливаются специфические антитела. Обычно антитела выделяют из сыворотки крови сульфатом аммония, спиртом или полиэтиленгликолем. Эти антитела имеют много примесей белков. Высокоочищенные антитела выделяют с помощью ионообменной и аффинной хроматографии на иммуносорбентах.
Для организации масштабного производства моноклональных антител ключевую роль сыграл метод гибридомной технологии. Хорошо известно, что в результате иммунного ответа на какой-либо антиген образуется высокогетерогенный продукт — антисыворотка со смесью антител, продуцируемых разными линиями В-лимфоцитов и направленных к разным антигенным детерминантам антигена. Проблема получения определенной линии лимфоцитов, которые не растут на искусственной среде in vitro в культуре, была решена, как только стало возможным получение соматических гибридов. Известно, что миеломы (злокачественные опухоли костного мозга, клетки которых обладают способностью к неограниченному росту) продуцируют большое количество аномальных иммуноглобулинов.
|
|
|
В 1975 г. Г. Келер и К. Мильштейн сумели впервые выделить клоны клеток, способные секретировать только один тип молекул антител и в то же время расти в культуре. Эти клоны клеток были получены слиянием антителообразующих и опухолевых клеток — клеток-химер, названных гибридомами, так как, с одной стороны, они наследовали способность к практически неограниченному росту в культуре, а с другой стороны, способность к продукции антител определенной специфичности (моноклональных антител).
Весьма существенно для биотехнолога то, что отобранные клоны могут длительно храниться в замороженном состоянии, поэтому в случае необходимости можно взять определенную дозу такого клона и ввести животному, у которого будет развиваться опухоль, продуцирующая моноклональные антитела заданной специфичности. Вскоре в сыворотке животного будут обнаружены антитела в очень высокой концентрации от 10 до 30 мг/мл. Клетки такого клона можно также выращивать in vitro, а секретируемые ими антитела получать из культуральной жидкости. В настоящее время гибридомная технология получила широкое применение. Создание гибридом, которые можно хранить в замороженном состоянии (криоконсервирование), позволило организовать целые гибридомные банки, что в свою очередь открыло большие перспективы по применению моноклональных антител.
2. Сфера их применения помимо количественного определения разных веществ включает самую разнообразную диагностику, например идентификацию определенного гормона, вирусных или бактериальных антигенов, антигенов группы крови и тканевых антигенов (табл. 10).
Только благодаря использованию моноклональных антител, полученных в результате иммунизации животных лекарствами, стало возможно определение дозы этих лекарств. Такая «иммунодозировка» надежна и экономична. В 1990-х гг. в США «Управление по контролю за качеством пищевых продуктов, медикаментов и косметических средств» (FDA) впервые утвердило к продаже коммерческий набор для диагностического скрининга на основе гибридом, предназначенный для установления аллергена.
|
|
|
С помощью моноклональных антител возможно выделение биологически активных веществ (белков, гормонов, токсинов) из сложных смесей. Например, при использовании иммуноадсорбции для очистки интерферона был получен препарат высочайшей степени очистки (до 99 %). Только после одного пассажа через колонку с иммобилизованными моноклональными антителами препарат очищался в 5 000 раз!
Таблица 10
Области применения моноклональных антител
| Диагностика | Терапия | Технология | Научные исследования |
| 1 Иммунохи мические анализы био-логических жидкостей, клеток орга- низма, мик-рорганизмов, вирусов и т. д. 2. Иммуногис тохимические методы 3. Иммунос-цинтиграфия опухолей. 4. Типирова- ние групп крови и тканей | 1. Воздействие на опреде-ленные кле-точные попу-ляции. 2. Влияние на иммунные ре-гуляторные ме-ханизмы с по-мощью антител к лимфокинам 3. Иммуно-регуляция с помощью ан-тиидиотипических антител. 4. Направлен-ный транспорт лекарств с помощью моноклональ-ных антител. 5. Элиминация токсинов, иммуноглобулинов из класса lgE | 1. Идентификация молекул. 2. Очистка клеток, несущих специфи-ческий антиген. | 1. Исследование этиологии и патогенеза различных заболеваний. 2. Исследование системных и межсистемных механизмов регуляции. 3. Создание новых лекарственных средств и биопрепаратов. |
Можно использовать моноклональные антитела и в качестве меток для точной идентификации специализированных клеток, например нейронов. Существует также технология использования моноклональных антител для изучения клеточных мембран, позволяющая выделять мембранные белки в чистом виде и измерять их биологическую активность. Моноклональные антитела можно использовать как в качестве стандартного реагента для обнаружения определенных молекул на клеточной мембране, так и для разделения популяции клеток, несущих на поверхности разные антигены. Кроме того, с помощью моноклональных антител можно создавать высокоспецифичные вакцины, особенно против определенных вирусных штаммов и паразитов. Моноклональные антитела способны также к нейтрализации лимфоцитов, ответственных за отторжение трансплантата и аутоантител, образующихся при аутоиммунных заболеваниях (некоторые формы диабета, рассеянный склероз, ревматические болезни). В сочетании с лекарственными средствами они могут значительно усиливать эффективность действия последних на клетки-мишени, позволяя избегать серьезных побочных явлений, весьма обычных, например при химиотерапии рака.
|
|
|
Некоторое время назад считалось, что геном эмбриональных клеток в процессе дифференцировки соматических клеток (стадия образования разных тканей организма) не изменяется, а все разнообразие форм и функций дифференцированных клеток относится к различиям в экспрессии одних и тех же генов. Однако в дальнейшем было показано, что разнообразие молекул антител, которые образуются зрелыми лимфоцитами, связано с так называемой «активной перетасовкой» нескольких сотен генов в клетках-предшественниках лимфоцитов. Причем именно степень активности этой «перетасовки» и обусловливает широчайшее разнообразие антител.
Было также показано, что рекомбинация ДНК позволяет изменять геном клетки, направляя ее метаболизм (клеточную специализацию) на увеличение генетического разнообразия. Как известно, молекула антитела является результатом сборки из нескольких белковых цепей, а синтез любого белка определяется соответствующим геном. Соответственно предполагалось, что должны существовать миллионы генов, кодирующих синтез определенных молекул антител, вырабатываемых организмом млекопитающих.
Однако было установлено, что в геноме клеток последних из сотен тысяч генов только незначительная их часть вызывает синтез антител в результате того, что так называемые стволовые (эмбриональные) клетки не содержат полного набора генов всех антител, а обладают лишь набором генетических элементов, которые способны очень быстро перестраиваться в процессе дифференцировки и созревания клеток иммунной системы (В-лимфоцитов), что, собственно, и приводит к образованию миллионов клеточных линий, вырабатывающих разные антитела.
Что касается молекулы самого антитела (иммуноглобулина), то она состоит из двух «легких» (L) и двух «тяжелых» (Н) белковых цепей, которые соединены расположенными в строго определенных местах дисульфидными мостиками и водородными связями. Каждая цепь имеет постоянную (константную) и вариабельную области. N-концевые участки (L) и (Н) цепей образуют антигенсвязывающий сайт. Отдельные домены (области) молекулы антитела выполняют разные функции, что облегчает манипуляции с генами антител. Антигенсвязывающие сайты состоят из трех участков CDR — complementarity-determining regions, определяющих комплементарность антител к антигену и образующих вариабельные (VH и VL) области на N-концах (Н) и (L) цепей. Для CDR характерна очень высокая изменчивость последовательности аминокислот, поэтому их называют еще гипервариабельными.
|
|
|
Легкие цепи идентичны у всех видов животных, а тяжелые цепи представлены пятью типами (ц, 5, у, е и а), которые и определяют пять классов иммуноглобулинов, обнаруженных у млекопитающих: IgM, IgD, IgG, IgE и IgA.
При контролируемом ферментативном гидролизе иммуноглобулинов образуются фрагменты двух типов: Fab и Fc, причем N-концевая часть Fab фрагмента, называемая Fу-фрагментом, обладает антигенсвязывающей активностью, присущей интактной молекуле антитела. Существуют около миллиона разных специфических антител, что обеспечивает определение практически любых биологически активных веществ как природного, так и синтетического происхождения. Например, в антителах класса IgM все тяжелые цепи имеют одинаковую постоянную область m, вариабельные же области у разных молекул антител различны и отражают их антигенные свойства. Таким образом, константная (постоянная) область тяжелых цепей определяет способ действия антитела в организме: если она, например, d-типа, т. е. антитело принадлежит к классу IgD, то оно является связанным с поверхностью синтезирующей его клетки; если же тяжелая цепь, например е-типа, то соответствующее антитело IgE может связываться с поверхностью специализированной клетки, способной выделять гистамин, что приводит к появлению симптомов астмы или лихорадки, когда антитело взаимодействует с антигеном (например, с пыльцой какого-либо растения).
Моноклональные антитела с успехом применяются для дифференциальной диагностики многих инфекционных и неинфекционных заболеваний, а также для стандартизации определения групп крови путем иммунохимического анализа. Именно с помощью моноклональных антител были идентифицированы индивидуальные маркеры многих возбудителей инфекционных заболеваний как вирусной, так и бактериальной природы. Изучение генетических механизмов многих заболеваний стало возможным благодаря уникальной специфичности моноклональных антител. Так, методом иммуносцинтиграфии опухолей можно идентифицировать локализацию опухоли с ее метастазами размером 0, 5— 1, 0 см.
Самыми важными областями использования иммунохимического анализа являются:
· контроль банков крови и продуктов из донорской крови;
· обнаружение возбудителей в объектах внешней среды;
· диагностика инфекционных заболеваний;
· диагностика диабета.
Сегодня количество проводимых иммунохимических анализов в мире растет настолько стремительно, что производство иммунодиагностикумов совместно с приборами и вспомогательными материалами можно рассматривать уже как отдельную, самостоятельную область биотехнологической промышленности.
Принципы иммунохимического анализа можно представить реакцией растворимого антигена (АГ) с антителом (AT), зная о двухвалентности AT и поливалентности АГ. Антитело, образуя комплекс с антигеном, обеспечивает уникальное по специфичности узнавание определяемого вещества в любых сложных многокомпонентных системах.
Этот процесс описывается системой уравнений двух стадий:
аг + at = агат
агат +ат = агn (ат)
Первая стадия характеризует взаимодействие активного центра антител с антигенной детерминантой, которая представляет участок молекулы АГ, способного связываться с активным центром специфического AT. Здесь проявляется свойство AT «склеивать» антигены (АГ). Причем размеры антигенных детерминант (эпитопов), например, для белковых антигенов составляют всего несколько аминокислот.
Вторая стадия характеризуется образованием комплексов сложного состава, когда двухвалентная молекула AT способна связаться лишь с двумя молекулами АГ в комплекс, который в свою очередь может связать еще одно AT и т. д. Образующиеся агрегаты таких комплексов обнаруживаются либо по возникающей мутности раствора, либо по выпадению в осадок.
Такая реакция взаимодействия белковых антигенов с антителами лежит в основе определения групп крови, когда происходит «склеивание» эритроцитов антителами той или иной специфичности. Эта реакция получила название гемагглютинации и очень широко используется на практике. Этот метод также широко применяется при определении белков плазмы крови в концентрации до 1 мг/л. Однако методы агглютинации вследствие довольно низкой точности относятся только к качественным или полуколичественным методам анализа.
Для расширения пределов чувствительности и повышения специфичности иммунохимических тестов в один из компонентов системы вводят маркер, концентрацию которого можно легко определять. После отделения продуктов реакции от исходных компонентов находят концентрацию АГАТ и по калибровочному графику рассчитывают содержание АГ.
Концентрацию антигена определяют из принципа конкурентного связывания антителами меченого и немеченого антигенов. Происходит следующая реакция:
АГ + АГ* + AT = АТАГ + АТАГ*
где АГ и АГ* — определяемый антиген без метки и с меткой; AT -антитела; АТАГ и АТАГ* — соответствующие комплексы.
Итак, если в пробирку с раствором, содержащим постоянную концентрацию антител и меченого антигена, добавить разные количества немеченого антигена, то концентрация комплекса АТАГ* (с меткой) будет обратно пропорциональна концентрации немеченого антигена. Для того чтобы отделить комплексы АТАГ от несвязавшихся компонентов анализируемой смеси, AT или АГ ковалентно связывают с твердой фазой, например с полистероловыми шариками. После промывки твердой фазы отделяют связавшиеся и несвязавшиеся компоненты. Такой тип анализа называют гетерогенным (принцип двух фаз: твердой и жидкой).
С большим успехом в гинекологическую практику вошел экспресс-метод определения беременности по уровню хориогонического гонадотропина в моче. Тесты таких типов можно проводить не только в специальных лабораториях, но и в домашних условиях. В качестве практического примера использования твердофазного иммуноферментного анализа ELISA можно рассмотреть метод определения хорионического гонадотропина. В этом методе на полистирольные шарики сорбируются моноклональные антитела к хорионическому гонадотропину. К сенсибилизированным шарикам добавляют исследуемую пробу (мочу) и конъюгат, состоящий из маркера и моноклональных антител, меченных пероксидазой. В результате иммунологической реакции хорионический гонадотропин связывается одной детерминантой с моноклональными антителами, иммобилизованными на поверхности шариков, а другой — с моноклональными антителами коньюгата с маркером. Затем шарики отмывают от всех несвязавшихся компонентов мочи и определяют активность фермента в составе иммунных комплексов с помощью субстрат-хромогенной смеси. При этом степень окраски раствора будет прямо пропорциональна количеству хорионического гонадотропина в образце мочи.
Лекарственный мониторинг также осуществляется посредством использования методов иммунохимического анализа. Необходимость контроля за концентрацией лекарственного препарата в процессе терапии у больного возникает при следующих ситуациях:
· длительных курсовых приемах лекарственных средств;
· низком терапевтическом эффекте или полном его отсутствии;
· возникновении побочных явлений в случае превышения терапевтической дозы препарата;
· трудно определяемом фармакологическом эффекте;
· особых обстоятельствах (например, при лечении новорожденных).
Лекарственный мониторинг может применяться, например, при терапии такими препаратами, как бронхолитик теофиллин, сердечный гликозид дигоксин и т. д. Известно, что успешный клинический результат зависит не от дозы препарата, а от его концентрации в плазме крови. Поэтому при достижении одного и того же лечебного эффекта у разных больных лекарственная дозировка препарата может разниться в десятки раз. Совершенно очевидно, что в этих случаях необходим индивидуальный подбор доз для каждого пациента. Кроме того, мониторинг лекарственных средств исключает передозировку лекарственного препарата и, соответственно, проявления токсических эффектов.
Рентабельными, экспрессными методами определения низкомолекулярных соединений в плазме крови являются иммуноаналитические методы, которые отличаются универсальностью (применимы к любому веществу, способному к индукции антител), высокой селективностью и чувствительностью; не требуют предварительной обработки образцов и имеют сравнительно низкую стоимость.
Известно, что иммунизация низкомолекулярными веществами не может вызывать иммунный ответ, поэтому для получения антител нужно предварительно лекарственный препарат ковалентно связать с иммуногенным высокомолекулярным носителем. Сначала лекарственное вещество делают реакционноспособным, вводя разные функциональные группы, которые затем взаимодействуют с соответствующими функциональными группами белка и образуют так называемый синтетический конъюгированный антиген. При иммунизации животного таким комплексным антигеном будут образовываться поликлональные антитела, т. е. антитела к антигенным детерминантам самого белка и к антигенным детерминантам лекарственного средства.
В настоящее время иммунодиагностические тест-системы с использованием поликлональных антител созданы практически для всех лекарственных препаратов. При проведении лекарственного мониторинга с использованием методов иммунохимического анализа в качестве «маркеров» применяются:
· радиоактивные метки (радиоиммунный анализ с использованием радиоактивных атомов-трития, радиоактивного йода и др. );
· ферментные метки (если ферменты стабильны, активны и
действуют в минимальных концентрациях);
· субстратные метки (АТФ и НАД), которые «пришиваются» к молекуле антигена через адениновый остаток и сохраняют способность взаимодействия с ферментом.
В качестве примера можно привести радиоиммунный метод количественного определения инсулина, основные принципы которого рассмотрим более подробно.
Общеизвестно, что инсулин влияет на концентрацию глюкозы в крови. В лабораторных условиях при наличии животных можно по снижению уровня глюкозы в крови сравнивать отдельные препараты инсулина. Но этот путь совершенно неприемлем для определения инсулина в крови больных, учитывая, что в контроле фактически нуждается если не миллионный, то многотысячный контингент больных. Клиническая лаборатория обязана определять количество эндогенного инсулина в крови больных, которым предписано введение инсулина извне. В противном случае возможны передозировки инсулина. Метод отличается высокой избирательностью (на результаты не влияют любые белки крови) и высокой точностью. В качестве лабораторного оборудования необходимы стандартный гамма-счетчик (например ГСБ-1) и коммерческий набор реагентов (в него входят меченый (по йоду) инсулин, у которого кодированы остатки тирозина и гистидина; антисыворотка к инсулину (антитела к инсулину), получаемая из крови кроликов, которым вводили инсулин).
У больного отбирается проба крови, где количество эндогенного (немеченого) инсулина неизвестно (х). Создается реакционная смесь: меченый инсулин + антисыворотка (фиксированное количество), т. е. комплекс антигена с антителом, который затем осаждается. Количество метки в осадке, определяемое радиометрическим методом, соответствует количеству меченого инсулина. Принцип анализа: если в реакционную смесь одновременно с меченым инсулином вводится проба крови с эндогенным инсулином, то количество метки в осадке будет тем меньше, чем больше х. В данной ситуации возникает конкуренция за антитело между меченым и немеченым инсулином. Количество немеченого инсулина не должно резко превышать количество меченого, иначе возможны погрешности в точности измерения. В соответствии с этим пробы крови принято разводить: х, x/1, х/4 и т. д. Избыток меченого инсулина помешать не может, так как метка определяется в осадке — там, где находится только связанный с антителом меченый инсулин. Расчеты проводятся по калибровочным кривым. Метод пригоден для определения числа микрограммов инсулина в 1 мл крови и не требует предварительных препаративных процедур. Один счетчик типа ГСБ-1 дает возможность анализа нескольких сотен проб в неделю. Радиоиммунный анализ удобен для мониторинга не только инсулина, но и многих других биологически активных агентов.
Существуют гетерогенные и гомогенные иммуноферментные методы: с разделением компонентов после проведения иммунохимической реакции (роль пассивного маркера выполняет фермент, не меняющий своей активности в ходе реакции) и без разделения компонентов (также используется ферментная метка, активность которой в ходе иммунной реакции меняется).
Гетерогенный иммуноферментный анализ основан на конкурентной реакции антител с исследуемым веществом и меченым веществом с последующим отделением антител и измерением активности фермента, связавшегося с ними.
Гомогенный иммуноферментный метод основан на способности антител модулировать активность некоторых ферментов, ковалентно связанных с измеряемым веществом. Антитела влияют на конформацию активного центра фермента, а добавление свободного вещества восстанавливает активность фермента. Чувствительность гомогенных методов, как правило, меньше, чем гетерогенных, но вполне достаточна для определения практически всех лекарственных препаратов и даже некоторых гормонов. Гомогенные методы достаточно просты; анализ проводится в одну стадию и длится несколько минут.
Также в иммуноанализе используют липосомы, содержащие метку. Существует множество модификаций этого метода, например, на мембране липосом находится антиген, взаимодействующий с антителами в присутствии комплемента и вызывающий лизис липосом с последующим высвобождением метки.
Существуют также и неинструментальные полуколичественные методы экспресс-анализа на бумаге, например на многослойных целлюлозных полосках, которые пропитывают разными реагентами иммунохимической реакции и затем склеивают вместе на пластике. Такой же принцип последовательного взаимодействия находится в основе еще одного полуколичественного метода — иммунохроматографического. На полоску бумаги сорбируют антитела. Затем конец этой полоски вносится в раствор пробы и конъюгата. В процессе диффузии раствора вверх по полоске меченый и свободный лекарственный препарат конкурентно взаимодействует с антителами, вызывая их насыщение. Чем больше концентрация препарата в пробе, тем выше будет зона насыщения. Затем следует проявление (детекция) полоски в растворе субстрата. Высота окрашенного столбика определяет концентрацию препарата в исследуемом образце (пробе).
|
|
|


