 |
Амиды – функциональные производные карбоновых кислот, в которых гидроксильная группа заменена аминогруппой.
|
|
|
|
Существуют N -замещенные амиды: производные первичных и вторичных аминов. В систематической номенклатуре к родоначальной структуре добавляют суффикс –амид. Символ N показывает, что заместитель связан с атомом азота в амидной группе.
СН3СО-NН2 СН3СН2СО-NН2 СН3СН2 СН2СО-NН2 С6Н5СО- NН2
Ацетамид пропанамид бутанамид бензамид
СН3СН2 СН2СО-NНСН3 СН3СН2СО-NНС2Н5 С6Н5- NН-СО С2Н5
N-метилбутанамид N-этилпропанамид N-фенилпропанамид
Получают ацилированием аммиака и аминов ангидридами и хлорангидридами кислот, а также сложными эфирами.
·  С6Н5СОСl + 2NН3 С6Н5СО NН2 + NН4Сl
С6Н5СОСl + 2NН3 С6Н5СО NН2 + NН4Сl
Бензоилхлорид бензамид
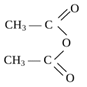
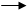 +:NН2СН3 СН3-СОNНСН3 + СН3-СООН
+:NН2СН3 СН3-СОNНСН3 + СН3-СООН
N-метилацетамид
Уксусный ангидрид
·  СН3СООС2Н5 + NН(СН3)2 СН3СО N(СН3)2 + С2Н5ОН
СН3СООС2Н5 + NН(СН3)2 СН3СО N(СН3)2 + С2Н5ОН
Этилацетат диметиламин N, N-диметилацетамид
Большинство амидов – кристаллические соединения с более высокими температурами плавления и кипения по сравнению с карбоновыми кислотами. Это объясняется образованием прочных межмолекулярных водородных связей. Водородные связи такого типа участвуют в формировании вторичной и третичной структур белков, определяя их пространственное строение.
В амидной группе электронное строение во многом схоже с карбоксильной группой. За счет сильного +М эффекта аминогруппы, положительный заряд на карбонильном атоме углерода значительно меньше, чем у других функциональных производных карбоновых кислот. Поэтому, амиды практически не вступают в реакции ацилирования, гидролизуются значительно труднее. Гидролиз проводится в присутствии кислот или оснований.
 СН3-СОNНСН3 + Н2О + НСl t СН3-СООН + СН3 NН3 Сl
СН3-СОNНСН3 + Н2О + НСl t СН3-СООН + СН3 NН3 Сl
 СН3-СОNНСН3 + NаОН Н2О, t СН3-СООNа + СН3NН2
СН3-СОNНСН3 + NаОН Н2О, t СН3-СООNа + СН3NН2
4. Обобщение.
Из рассмотренных свойств мы видим, что карбоновые кислоты и их производные обладают разной реакционной способностью в реакциях нуклеофильного замещения (ацилирования).
|
|
|
Ангидриды и хлорангидриды легко вступают в реакции ацилирования. Из них можно получить любые производные карбоновых кислот. Сами кислоты и сложные эфиры значительно менее активные ацилирующие агенты, реакции ЅN с их участием проводятся в присутствии катализаторов. Амиды - практически не вступают в реакции ацилирования.
Соли карбоновых кислот ацилирующей способностью не обладают.
Все функциональные производные кислот находятся в тесной взаимосвязи друг с другом. Работа с учебником О-1 с. 197 рис. 11.3;
 Угольная кислота и ее производные. Н2СО3 СО2 + Н2О
Угольная кислота и ее производные. Н2СО3 СО2 + Н2О
Фосген (карбонилхлорид) – СОСl2 – полный хлорангидрид угольной кислоты.
 СО + Сl2 СОСl2 газ с запахом прелого сена, токсичен, вызывает оттек легких. Применялся в качестве боевого отравляющего вещества. Образуется из хлороформа при неправильном его хранении. Используют для получения красителей,, пластмасс, лекарственных веществ.
СО + Сl2 СОСl2 газ с запахом прелого сена, токсичен, вызывает оттек легких. Применялся в качестве боевого отравляющего вещества. Образуется из хлороформа при неправильном его хранении. Используют для получения красителей,, пластмасс, лекарственных веществ.
Карбаминовая кислота Н2N-СООН не существует в свободном состоянии.
Эфиры карбаминовой кислоты называются уретанами, их систематическое название - карбаматы.
 Н2N-СОСl + С2Н5ОН Н2N-СОО С2Н5 + НСl этилкарбамат (уретан)
Н2N-СОСl + С2Н5ОН Н2N-СОО С2Н5 + НСl этилкарбамат (уретан)
Н2N-СООСН2-С(СН3)(С3Н7)- СН2ООС- NН2 мепротан – снотворное средство
Мочевина (карбамид)- (NН2)2С=О – полный амид угольной кислоты.
Основной конечный продукт распада белков у млекопитающих. Используется в качестве азотного удобрения.
На закрепление выполните вопросы после параграфа: уравнения на химические свойства кислот и их получение, а также цепочка превращения. Не забывайте называть вещества, указывать условия реакции и тип, механизм реакции. Задание 11.32 повышенного уровня!
За 5.02.2016
Амины. Строение, номенклатура, изомерия, свойства. Представители.
Стр. 205-211, стр. 217 вопросы 12.1, 12.4, 12.5, 12.8
|
|
|


