 |
Критерий 1. Генетическая нестабильность
|
|
|
|
Основные функции нашего тела контролируются генами, находящимися в хромосомах ядра. В каждой клетке имеется всего две копии каждой хромосомы, да и те не являются идентичными – могут иметь разные варианты одного и того же гена (аллели). Поэтому повреждение молекул ДНК, из которых состоят хромосомы, может иметь печальные последствия для функций, выполняемых клеткой. Всплеск повреждений ДНК и мутаций, наблюдаемый при старении, носит название генетической нестабильности. Рассмотрим некоторые разновидности этой нестабильности.
Теломеры и теломераза
На концах каждой из хромосом имеются особые участки, называемые теломерами. Это важные области ДНК, за которые хромосомы прицепляются к внутренней оболочке клеточного ядра (рис. 22). На теломерах расположены особые белки, которые защищают хромосомы от атаки некоторых ферментов. Например, экзонуклеаз, в норме охраняющих наши клетки от вирусных ДНК, или лигаз, сращивающих обрывы нитей ДНК. Если бы не было теломер и связанных с ними защитных белков, экзонуклеазы отрезали бы от хромосом куски, а лигазы пришивали одни хромосомы к другим. Теломеры играют важную защитную роль, поэтому клетки с поврежденными хромосомами не способны поделиться или даже выжить, а иногда, напротив, начинают бесконтрольно делиться – становятся раковыми. Области хромосом, если они расположены близко от теломер, содержат большое количество метильной метки – это химическая модификация букв ДНК, способствующая более компактной упаковке нити ДНК и заставляющая молчать расположенные вблизи метилированного участка гены. Расположение теломер на самых концах хромосом приводит к тому, что с каждым клеточным делением они немного укорачиваются. Процесс укорочения хромосом при делении был предсказан советским иммунологом А. М. Оловниковым в 1971 году и экспериментально доказан нобелевскими лауреатами К. Грейдер и Э. Блекберн. Укорочение теломер не всегда связано с делением клетки. На концах хромосом могут возникать опасные разрывы, например при избытке свободных радикалов, что также провоцирует укорочение хромосом.
|
|
|
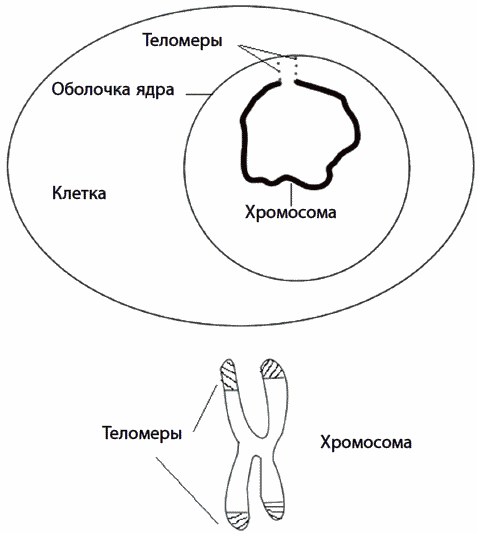
Рис. 22. Теломеры на концах хромосом в покоящемся ядре клетки (вверху) и на стадии клеточного деления (внизу)
В делящихся клетках с возрастом концы хромосом укорачиваются настолько, что они теряют защитный комплекс белков. В близко расположенных к укороченным теломерам генах также пропадает метильная метка, которая заставляла эти гены молчать. Прителомерные гены активизируются, что сеет хаос в сбалансированной системе клеточных белков. «Оголившиеся» концы воспринимаются клеткой как сигнал об обрыве. В отличие от обычного разрыва ДНК попытка клетки залечить такой «обрыв» по понятным причинам является безуспешной.
Далее возможны два варианта событий.
В одних клетках происходит необратимая остановка клеточных делений. Особенно неприятно, когда перестают делиться стволовые клетки – незрелые предшественники прочих типов клеток в каждой ткани. Это приводит к тому, что клеток нужной ткани определенного органа становится недостаточно, в результате чего нарушается функция этой ткани или органа. Например, от укорочения теломер с возрастом страдают клетки – основательницы клеток крови и клеток, выстилающих поверхность сосудов. Это является одной из причин анемий, иммунных расстройств и атеросклероза.
В других клетках при обнаружении псевдообрыва ДНК включается программа самоликвидации (апоптоза). Она также приводит к нарушениям в тканях.
О смертельной опасности укорочения концов хромосом говорит тот факт, что у лиц старше 60 лет чем короче теломеры, например в лимфоцитах крови, тем более высокими являются показатели смертности от инфекционных и сердечно-сосудистых заболеваний.
|
|
|
Для того чтобы теломеры не укорачивались в половых клетках и эмбриональных стволовых клетках, в них активен специальный фермент – теломераза. Он достраивает теломеры после каждого деления. Однако в клетках большинства тканей и органов человека ген одного из компонентов теломеразы отключен или работает очень слабо. Побочным следствием такого выключения является так называемое репликативное старение – прекращение способности к делению. Природа пошла на этот шаг, чтобы обезопасить развивающийся организм от смертельного заболевания – рака. Обычные клетки не могут делиться более определенного числа раз, что тормозит образование опухолей. Действительно, теломераза каким-то образом реактивируется в большинстве видов опухолевых клеток, делая их защищенными от клеточного старения, практически бессмертными. В то время как обычные фибробласты делятся в чашках Петри примерно 50 раз и погибают, претерпевшие злокачественное перерождение способны делиться в клеточной культуре десятилетиями. Искусственная индукция теломеразы в обычных фибробластах тоже вызывает их бесконечное деление. Научной группе под руководством Марии Бласко удалось с помощью генной терапии вернуть активность теломеразы тканям старых мышей, в результате чего они стали жить дольше и меньше болеть возраст-зависимыми заболеваниями.
Мутации
В 1958 году в статье «О природе процесса старения» Лео Сцилард, заложивший принципы создания атомной бомбы, выдвинул гипотезу о том, что элементарным событием старения является случайное повреждение хромосомы, инактивирующее ее гены. С возрастом накапливаются поломки хромосом не только в области теломер, но и по всей их длине. Это связано прежде всего с тем, что механизмы починки (репарации) ДНК перестают эффективно работать. Любое повреждение «букв» (нуклеотидов), из которых состоят наши гены, или разрыв цепочки ДНК на фоне недостатка репарации в стареющей клетке становится причиной мутации. Чем больше мутаций приобретает клетка, тем она менее жизнеспособна или выше риск, что она станет опухолевой.
|
|
|
Узнай больше
Ошибки в ДНК могут возникать также в процессе ее удвоения при делении клеток. Процесс этот сложный, он включает в себя несколько стадий. Сначала двойная спираль ДНК раскручивается и разделяется на две отдельные нити с образованием так называемой репликационной вилки. Легче всего вообразить этот процесс как расстегивание молнии на одежде. Затем специальные ферменты выполняют копирование каждой нити расплетенной двойной спирали ДНК. После этого происходит сплетение дочерних нитей с родительскими с образованием двух новых спиралей ДНК. В идеальном случае каждая дочерняя нить должна быть полностью идентичной материнской, но на практике в процесс могут закрадываться разнообразные ошибки. Это могут быть однобуквенные замены при неправильном копировании дочерней нити на материнской нити ДНК, а может быть запутывание нитей, ведущее к остановке репликационной вилки и разрывам ДНК (репликативный стресс). К репликативному стрессу ведут также межнитевые сшивки ДНК и сшивки ДНК с расположенными на ней белками. Эти неприятные явления вызываются уже знакомыми нам продуктами перекисного окисления липидов мембран и конечными продуктами гликирования, которых с возрастом возникает все больше.
|
|
|


