 |
Скорость химических реакций. Факторы, влияющие на скорость. Влияние катализаторов на скорость протекания реакции
|
|
|
|
Стехиометрические законы. Закон кратных отношений. Закон постоянства состава
Стехиометрия — раздел химии, в котором рассматриваются массовые или объемные соотношения между реагирующими веществами. Исключительное значение для развития химии имело установление основных стехиометрических законов.
Закон кратных отношений (Д. Дальтон): Если два элемента образуют между собой несколько молекулярных соединений, то масса одного элемента, приходящаяся на одну и ту же массу другого, относятся между собой как небольшие целые числа.
При взаимодействии азота с кислородом образуются пять оксидов. На 1 грамм азота в образующихся молекулах приходится 0,57, 1,14, 1,71, 2,28, 2,85 грамм кислорода, что соответствует отношением 2:1, 1:1, 2:3, 1:2, 2:5 в этих оксидах; их составы N2O, NO, N2O3, NO2, N2O5. Закон постоянства состава вещества (Ж. Л. Пруст, 1808 г.). Каждое чистое вещество независимо от способа его получения всегда имеет постоянный качественный и количественный состав. Атомно-молекулярное учение позволяет объяснить закон постоянства состава. Например, воду можно получить по любой из следующих реакций:
2Н2+О2=2Н2О
Са(ОН)2=СаО+Н2О
CuSO4•5Н2О=CuSO4+5Н2О
Химически чистая вода содержит 11,19% водорода и 88,81% кислорода, независимо от способа ее получения, то есть на один атом кислорода приходится два атома водорода. Иной состав свидетельствует либо о наличии примесей, либо о том, что это другое вещество (например, Н2О2). Ж. Пруст писал: «От одного полюса Земли до другого соединения имеют одинаковый состав и одинаковые свойства. Никакой разницы нет между оксидом железа из Южного полушария и Северного. Малахит из Сибири имеет тот же состав, как и малахит из Испании».В этой формулировке закона, как и в приведенном выше, подчеркивается постоянство состава соединения независимо от способа получения и места нахождения.
|
|
|
Строение внешнего электронного уровня атома калия и кальция. 1 правило Клечковского. Строение внешнего электронного уровня атома скандия. 2правило Клечковского
У атома аргона остаются незанятыми все орбитали 3d-подуровня. Однако у следующих за аргоном элементов – калия и кальция – заполнение 3-го электронного слоя временно прекращается, и начинает формироваться s-подуровень 4-го слоя. Такой порядок заполнения вытекает из первого.Первое и второе правила Клечковского часто не разделяют, а считают одним совместным правилом правила Клечковского: при увеличении заряда ядра атомов заполнение энергетических уровней происходит от орбиталей с меньшим значением суммы главного * и орбитального * квантовых чисел (n+l) к орбиталям с большим значением этой суммы. Следовательно, 4s-подуровень (n + l =4) должен заполняться раньше, чем 3d (n+l =5). Для атома скандия возникает вопрос: какой из подуровней должен заполняться – 3d или 4p, т.к. сумма n+l для них одинакова и равна 5. В подобных случаях порядок заполнения определяется вторым. Первое и второе правила Клечковского часто не разделяют, а считают одним совместным правилом правилом Клечковского, согласно которому при одинаковых значениях суммы (n+l) орбитали заполняются в порядке возрастания главного квантового числа n. Заполнение 3d-подуровня происходит у десяти элементов от Sc до Zn. Это атомы d-элементов. Затем начинается формирование 4p-подуровня (p-элементы от Ga до Kr). Как и атомы предшествующих благородных газов – неона и аргона – атом криптона характеризуется структурой внешнего электронного слоя ns2np6.
Скорость химических реакций. Факторы, влияющие на скорость. Влияние катализаторов на скорость протекания реакции
|
|
|
Скорость химической реакции определяется как изменение молярной концентрации одного из реагирующих веществ за единицу времени. Скорость химической реакции — величина всегда положительная, поэтому, если она определяется по исходному веществу (концентрация которого убывает в процессе реакции), то полученное значение домножается на −1.
Например для реакции:
A + B → C + D
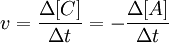 .
.
В 1865 году Н. Н. Бекетовым и в 1867 году Гульдбергом и Вааге был сформулирован закон действующих масс: скорость химической реакции в каждый момент времени пропорциональна концентрациям реагентов, возведенным в некоторые степени.
Для элементарных реакций показатель степени при значении концентрации каждого вещества равен его стехиометрическому коэффициенту, для более сложных реакций это правило не соблюдается. Кроме концентрации на скорость химической реакции оказывают влияние следующие факторы:
· природа реагирующих веществ,
· наличие катализатора,
· температура (правило Вант-Гоффа),
· площадь поверхности реагирующих веществ.
Если мы рассмотрим самую простую химическую реакцию A + B → C, то мы заметим, что мгновенная скорость химической реакции величина непостоянная.
Зависимость скорости химической реакции от катализаторов. Катализ – явление изменения скорости химической реакции в присутствии веществ, состояние и количество которых после реакции остаются неизменными.
Различают положительный и отрицательный катализ (соответственно увеличение и уменьшение скорости реакции); отрицательный катализ называют ингибированием, а вещества, уменьшающие скорость химической реакции, – ингибиторами.
|
|
|


