 |
Преодоление несовместимости в данном случае: необходимо приготовить раздельно порошки ГМТА и аскорбиновой кислоты по согласованию с врачом.
|
|
|
|
Вопрос 3. Radices Althaeae корни алтея (Althaeae radix — алтея корень)
Алтея лекарственного (Althaea offlcinalis L.) и алтея армянского (Althaea armeniaca Ten.) из сем. мальвовых (Malvaceae); используют в качестве лекарственного средства и лекарственного сырья.
Заготовка сырья, первичная обработка, сушка. Корни заготавливают осенью, после отмирания надземных частей растений (сентябрь — октябрь), или весной, до начала отрастания (апрель — начало мая). После выкапывания лопатами или плугами корни тщательно очищают от земли, обрезают корневища и мелкие корни, удаляют одревесневшую верхнюю часть главного корня; неодревесневшие корни подвяливают 2-3 дня на воздухе, затем снимают пробку. Длинные корни режут поперечно на куски длиной до 35 см, толстые — вдоль на 2-4 части.
Для получения неочищенного сырья после выкапывания и отряхивания от земли корни помещают в корзины и быстро промывают в холодной проточной воде. В остальном обработка проводится так же. как для очищенного от пробки сырья.
Траву алтея заготавливают во время цветения (в течение месяца от начала зацветания), скашивая механизированным способом, удаляют пожелтевшие листья и примесь других растений.
Корни и траву алтея сушат либо в сушилках при температуре 50-60 °С. либо в хорошо проветриваемых помещениях. В южных районах страны корни сушат также на солнце, укрывая их на ночь. При сушке этого сырья необходимо учитывать его гигроскопичность. Раскладывают его тонким слоем, рыхло, на сетках или рамах, обтянутых тканью. После сушки из сырья удаляют примеси, заплесневевшие и изменившие окраску корни и части травы.
Внешние признаки. Корни алтея. Цельное сырье представляет собой очищенные от пробки корни почти цилиндрической формы или расщепленные вдоль на 2-4 части длиной 10-35 см, толщиной до 2 см, продольно-бороздчатые с отслаивающимися длинными, мягкими лубяными волокнами и темными точками — следами опавших или отрезанных мелких корней. Излом в центральной части зернисто-шероховатый, снаружи волокнистый. Цвет корня снаружи и в изломе белый, желтовато-белый, сероватый. Запах слабый, своеобразный. Вкус сладковатый с ощущением слизистости.
|
|
|
Измельченное сырье. Смесь кусочков корней различной формы размером от 1 до 7 мм. Цвет желтовато-белый или серовато-белый.
Порошок. Имеет белый, желтовато-белый или сероватый цвет, проходит сквозь сито с отверстиями размером 0.31 мм.
Качественные реакции. При смачивании среза или порошка корня раствором аммиака или натрия гидроксида появляется желтое окрашивание (слизь).
Микроскопия. При анатомическом исследовании корня алтея диагностическое значение имеют: вторичное строение корня с преобладанием в ксилеме тонкостенной паренхимной
ткани; многочисленные со слабоутолщенными. неодревесневшими или слабо одревесневшими стенками группы волокон, расположенные прерывистыми концентрическими поясами во флоэме и более мелкими группами в ксилеме; небольшие группы сосудов и трахеид; одно-, реже двурядные сердцевинные лучи: крупные клетки со слизью; клетки паренхимы с крахмальными зернами; мелкие друзы кальция оксалата. При микроскопическом исследовании неочищенного корня алтея, помимо указанных признаков, надо отметить наличие тонкого слоя пробки.
При исследовании порошка видны паренхимные клетки с крахмальными зернами и отдельные крахмальные зерна округлой, овальной или яйцевидной формы размером 3-27 мкм, обрывки сетчатых и лестничных сосудов, волокон, друзы кальция оксалата. Слизь обнаруживают при рассмотрении в разведенной туши.
Хранение. Хранят сырье в хорошо проветриваемых сухих помещениях. Срок годности корней, очищенных и не очищенных от пробки — 3 года; травы — 5 лет.
|
|
|
Использование. Корни используют в качестве отхаркивающего, мягчительного, противовоспалительного и обволакивающего средства в виде порошка, настоя, сухого экстракта и сиропа и в составе грудных сборов при острых и хронических заболеваниях дыхательных путей, а также при заболеваниях желудочно-кишечного тракта.
Вопрос 4. Рецепт выписан не верно. Рецепт должен быть выписан на бланке ф.№107/У, заверенный личной печатью и подписью врача. НЕО не регламентированы. НЕО установлены пр.№328.
Срок действия рецепта - 2 мес. Рецепт отдается больному с указание на обороте количества отпущенного препарата и даты отпуска и не хранится в аптеке. По истечении срока действия рецепт гасится штампом «Рецепт не действителен».
Способ применения ЛС обозначается на русском или русском и национальном языках с указанием дозы, частоты, времени приема и его длительности.
Порошки до прихода больного хранят в сухо, защищ. от света месте при Т не выше 25С в тсч. 10 дней.___________^^
I Биле №20. Вопрос 1. s*
в-Лактамные антибиотики (в-лактамиды) содержат в молекуле лактамный цикл.. К бициклическим относятся соединения, в которых четырехчленный лактамный цикл сконденсирован с другим циклом по атому азота и соседнему с ним атому углерода. Вторым циклом в системе является пятичленный тиазолидиновый (пенами), пирролидиновый (карбопенамы) или оксазолидиновый (оксапенамы) цикл, либо шестичленный дигидротиазиновый цикл (цефалоспорины и цефамицины)
К бициклическим в-лактамидам относятся пенициллины

Механизм антибактериального действия в-лактамидов состоит в блокировании конечной стадии образования стенки бактерий, которое вызывает лизис клетки. Под влиянием ферментов — лактамаз происходит процесс инактивации антибиотиков. Действие этих ингибиторов основано на конкурентном антагонизме с пенициллинами. поскольку и те и другие содержат в-лактамное ядро.
При окислении атома серы тиазолидинового цикла у производных пенициллановой кислоты образуются соединения, способные подавлять в-лактамазы. Примером могут служить производные 1,1-диоксида пенициллановой кислоты (III): 
Различие в механизме каталитического действия пенициллиназы.
|
|
|
Природный бензилпенициллин применяют в виде натриевой,' калиевой и других солей. Созданные на его основе многочисленные лекарственные формы отличаются наиболее высокой химиотерапевтической эффективностью и наименьшей токсичностью. Однако Ь-лактамный цикл бензилпенициллина легко разрушается под действием фермента пенициллиназы (Ъ-лактамазы), продуцируемой многими микроорганизмами. Кроме того, многолетнее его применение привело к широкому распространению резистентных микробов. Эти обстоятельства послужили предпосылкой создания полусинтетических пенициллинов.
Решение такой сложной проблемы стало возможным после выделения в 1957 г. 6-аминопенщиллановой кислоты (6-АПК). являющейся «ядром» пенициллина. Получают 6-АПК из бензилпенициллина (или других пенициллинов), воздействуя ферментом пенициллинацилазой, продуцируемым бактериями. Процесс происходит по схеме:
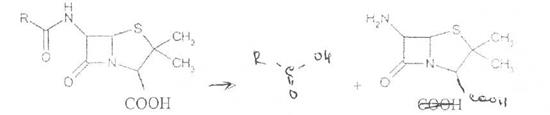
природные пенициллины 6-аминопенициллановая кислота (6-АНК)
Извлекают 6-АПК из водного гидролизата экстракцией или с помощью ионообменной хроматографии.
Таким образом, первая стадия производства полусинтетических пенициллинов состоит из биосинтеза 6-АПК. На второй стадии осуществляется ацилирование амина в молекуле 6-АПК соответствующей кислотой или ее хлорангидридом.
Пенициллины
Структурной основой лекарственных веществ природных и полусинтетических пенициллинов является 6-аминопенициллановая кислота, которая включает конденсированные тиазолидиновый (А) и лактамный (В) циклы:

Специфичность биологической активности пенициллинов прежде всего обусловлена наличием в молекуле тиазолидинового и b-лактамного циклов. Расщепление одного из них приводит к полной потере активности. Важная роль в сохранении антибактериальной активности принадлежит также пространственной конфигурации молекул пенициллинов. Характер группировок, присоединенных к гетероциклической системе в положениях 2 и 3, не оказывает заметного влияния на биологическую активность. Различную химическую структуру может иметь радикал, замещающий атом водорода в аминогруппе, которая присоединена клактамному циклу в положении 6. Это позволило получить ряд высокоактивных полусинтетических аналогов более устойчивых, чем природный пенициллин.
|
|
|
По физическим свойствам природные пенициллины и их синтетические аналоги представляют собой белые или почти белые кристаллические порошки без запаха. Натриевая и калиевая соли бензилпенипиллина слегка гигроскопичны. Натриевая соль бензилпенициллина очень легко растворима в воде. Натриевая и калиевая соли бензилпенициллина. растворимы в этиловом и метиловом спиртах, Натриевые и калиевые соли пенициллинов практически нерастворимы в хлороформе и эфире.
Свойства пенициллинов

Подлинность природных и синтетических пенициллинов подтверждают с помощью УФ- и ИК-спектрофотометрии. Устанавливают значения оптических плотностей растворов солей бензилпенициллина при длинах волн 280 и 263 нм, разность между которыми должна быть не менее 0.72.
ИК-спектры природных и полусинтетических пенициллинов идентифицируют по совпадению с полосами поглощения соответствующих стандартных образцов в области 4000— 400 см-. Подлинность бензилпенициллина натриевой соли устанавливают также методом ТСХ на силикагеле Н или пластинках Сорбфил с последующим проявлением в парах иода.
Важная физическая константа пенициллинов — удельное вращение водных или спиртовых растворов. Все они вращают плоскость поляризованного света вправо.
Химические реакции, используемые для испытаний подлинности пенициллинов. основаны на обнаружении в их молекулах различных функциональных групп, продуктов деструкции, атома серы, связанных аминов, катионов калия и натрия.
Для испытания подлинности пенициллинов и их полусинтетических аналогов используют цветную реакцию, основанную на разрыве в-лактамного цикла с образованием внутрикомплексной соли меди (II) с гидроксамовой кислотой (осадок зеленого цвета) или железа (III) —- красное или фиолетовое окрашивание:

хлороводородной кислоты, то в осадок выпадает свободный бензилпенициллин, растворимый в избытке хлороводородной кислоты, а также в этаноле, хлороформе, эфире.
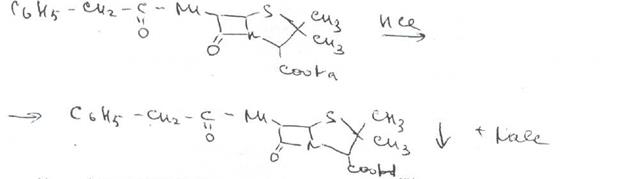
Соли бензилпенициллина при кипячении в 4%-ном растворе гидроксида натрия гидролизуются с образованием натриевой соли фенилуксусной кислоты, которая после добавления избытка разбавленной серной кислоты обнаруживается по характерному запаху.

Ьензилпенйциллин подвергает кислотному "Гидролизу до бензилпеницилленовой кислоты. Она вступает в реакцию сочетания с производным глютаконового альдегида, который образуется (рН 4.9) в результате расщепления пиридинового цикла пол действием тиоцианата
|
|
|
хл°Ра- СсЛ<.- см..^^. -
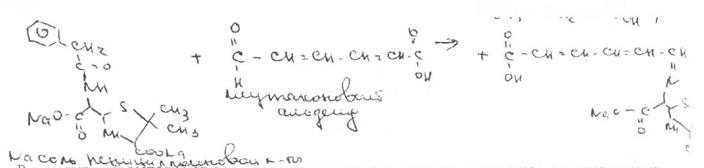
Г ял испытании выполняют для установления степени чистоты природных и синтетических пенициллинов. По величине оптической плотности растворов определяют светопоглощающие примеси. Выбор длины волны и допустимые значения оптической плотности зависят от химической структуры испытуемого пенициллина. В некоторых пенициллинах устанавливают допустимое ФС содержание иодсорбирующих примесей (0.5-6%) методом обратного иодометрического определения в фосфатном или ацетатном буфере.
Природные и синтетические пенициллины испытывают на наличие воды (по методу К. Фишера) и устанавливают рН растворов или водных суспензий (потенциометрически).
Испытание на токсичность
Испытание проводят на здоровых белых мышах обоего пола массой 19—21 г. на которых ранее не проводили никаких испытаний.
Для испытания на токсичность отбирают по 2 флакона или ампулы от каждой серии, -содержащей не более 10 000 флаконов или ампул. При количестве в серии флаконов или ампул более 10 000 отбирают по 3 флакона или ампулы от каждой серии. Для проведения испытания из отобранных флаконов или ампул готовят общий раствор (смешанная проба). Общее количество отобранного лекарственного средства должно быть достаточным для проведения трех полных испытаний.испытание на пирогенность
Испытание проводят на здоровых кроликах обоего пола, не альбиносах, массой 2—3.5 кг, содержавшихся на полноценном рационе. Каждый кролик должен находиться в отдельной клетке в помещении с постоянной температурой. Колебания температуры не могут превышать ±3 °С. При уборке клеток и взвешивании животных их оберегают от возбуждения (избегать шума и резких движений).
ОПРЕДЕЛЕНИЕ АНТИМИКРОБНОЙ АКТИВНОСТИ АНТИБИОТИКОВ МЕТОДОМ ДИФФУЗИИ В АГАР
Определение антимикробной активности антибиотиков основано на их способности угнетать рост микроорганизмов. Определение проводят методом диффузии в агар на плотной питательной среде путем сравнения размеров зон угнетения роста тест-микробов, образующихся при испытании растворов определенных концентраций Государственного стандартного образца и испытуемого препарата.
Антимикробная активность антибиотиков выражается в единицах действия — ЕД или «мгк». Для большинства антибиотиков 1 ЕД или «мкг» соответствуют 1 мкг активного вещества (кислоты или основания); для антибиотиков, имеющих иное количественное выражение единицы, соответствующие указания даются в частных статьях.
При определении антимикробной активности антибиотиков используют стандартные образцы, активность которых, как правило, устанавливают в соответствии с Международными биологическими стандартами. При отсутствии последних для указанных целей могут быть использованы международные химические стандарты, антимикробную активность которых рассчитывают на основании показателей качества, установленных физико-химическими методами. Антимикробную активность стандартных образцов антибиотиков, не имеющих аналогов в международной коллекции стандартов, рассчитывают также на основании показателей качества, установленных физико-химическими методами.
Стандартные образцы антибиотиков утверждаются и рассылаются Государственным научно-исследовательским институтом по стандартизации и контролю лекарственных средств Минздрава СССР, хранятся и используются в соответствии с рекомендациями, указанными на этикетке стандартного образца.
Методы количественного определения пенициллинов
Количественное определение пенициллинов выполняют химическими методами. В некоторых из них (натриевой, калиевой, новокаиновой солях бензилпенициллина. феноксиметилпенициллине и амоксициллине) сумму пенициллинов определяют иодометрическим методом. Сущность способа заключается в том, что продукт инактивации пенициллина (1 М раствором гидроксида натрия при комнатной температуре) — натриевую соль пенициллоиновой кислоты — окисляют иодом. Процесс окисления необходимо проводить при рН 4,5 (ацетатный буфер).
Схема инактивации и окисления на примере бензилпенициллина:
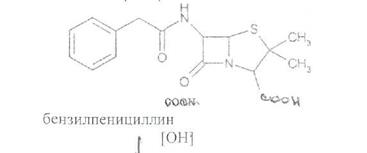

дегидропенальдиновая кислота пеницилламиновая кислота
Определение суммы пенициллинов выполняют обратным иодометрическим методом. Избыток 0.01 N4 раствора иода оттитровывают раствором тиосульфата натрия той же концентрации после 20 мин пребывания ее в темном месте (индикатор крахмал). Одновременно проводят контрольный опыт с тем же количеством пенициллина, не подвергнутого щелочному гидролизу, а также иодометрическое определение соответствующего ГСО.
Количественное определение натриевой соли бензилпенициллина выполняют гравиметрическим методом. Бензилпенициллин извлекают амилацетатом и количественно осаждают в виде N-этилпиперидиновой соли:


п-зшлпииеридиииъая ииль исыдишеницидлина
Осадок N-этилпиперидиновой соли бензилпенициллина промывают, высушивают до постоянной массы и взвешивают. Затем делают пересчет на соответствующую соль.
Активность пенициллинов устанавливают микробиологическим методом по антибактериальному действию на определенный штамм золотистого стафилококка. Одна единица действия соответствует активности 0,5988 мкг химически чистой натриевой соли бензилпенициллина (1670 ЕД в 1 мг). Микробиологический метод определения пенициллинов дает воспроизводимость результатов 5-10%. Этот метод приведен в ряде ФС как альтернативный вместе с химическим или спектрофотометрическим методом. Алкалиметрический метод определения суммы пенициллинов имеет удовлетворительную воспроизводимость, но дает завышенные результаты, так как одновременно титруются вес примеси, взаимодействующие со щелочью.
Наиболее точные, сопоставимые с микробиологическим методом результаты дает спектрофотометрическое определение пенициллинов, основанное на их гидролизе до пеницилленовых кислот. Они имеют максимум светоп or лощения при 320-324 или 335 нм.
Для определения бензилпенициллина натриевой соли, феноксиметилпенициллина соли МФ также рекомендовано спектрофотометрическое определение. Оно основано на взаимодействии раствора пенициллинов при нагревании на водяной бане с имидазолом и хлоридом ртути (II). Светопоглошение полученного раствора измеряют при 325 нм относительно смеси реактивов. Фотоколориметрические методы определения природных пенициллинов основаны на реакциях образования окрашенных гидроксаматов железа или меди.
Пенициллины хранят по списку Б, в сухом месте, при комнатной температуре. Упаковывают соли бензилпенициллина во флаконы, герметически закрытые резиновыми пробками, обжатыми алюминиевыми колпачками. На воздухе, при повышении температуры, в присутствии влаги, тяжелых металлов они быстро разлагаются. Натриевая соли бензилпенициллина содержат в каждом флаконе по 125 000. 250 000, 500 000 и 1 000 000 ЕД: Природные пенициллины применяют для лечения пневмонии, гонореи, сифилиса, раневых и гнойных инфекций, перитонита, дифтерии, скарлатины, ангин различной этиологии и инфекционных заболеваний, вызванных чувствительными к пенициллину микроорганизмами. Полусинтетические аналоги имеют более широкий спектр антибактериального действия.
В процессе использования антибиотиков к ним может развиваться устойчивость
микроорганизмов (антибиотикорезистентность). Возможна так называемая перекрестная
устойчивость, которая относится не только к применяемому препарату, но и к другим
антибиотикам, сходным с ним по химическому строению (например, ко всем
тетрациклинам). Вероятность развития устойчивости уменьшается, если дозы и длительность
введения антибиотиков оптимальны, а также при рациональной комбинации антибиотиков.
Если к основному антибиотику возникла устойчивость, его следует заменить другим,
резервным, антибиотиком.
Основной механизм и характер антимик робного действия антибиотиков
Преимуществен
Спектр действия Антибиотики Основной механизм ный характер
антимикробного антимикробного
действия
действияАнтибиотики, влияющие
преимущественно на грамположительные бактерии
Антибиотики, влияющие на
гр ам отри ц ател ьн ые бактерии
Антибиотики широкого спектра действия
Препараты
бензилпеницилли
на
Оксациллин
Эритромицин
Полимиксины
Полусинтетическ ие
пенициллины широкого спектра действия
Угнетение синтеза клеточной стенки
То же
Угнетение белка
синтеза
Нарушение проницаемости цитоплазматической мембраны
Угнетение синтеза клеточной стенки
Бактерицидный
То же
Бактериостати ческий
Бактерицидный
Бактерицидный
Вопрос 2. Получение воды для инъекций в промышленных условиях.
Согласно требованиям ФС 42-2620-89 вода для инъекций (Aqua pro ingectionibus) должна удовлетворять всем требованиям, предъявляемым к воде очищенной, а также должна быть стерильной и апирогенной. Стерильность воды определяется методами, изложенными в статье «Испытания на стерильность» ГФ XJ издания, с. 187—192. Испытание пирогенности воды проводят биологическим методом, приведенным в статье «Испытание на пирогенность» ГФ XI издания, с. 183—185.
Оборудование для получения воды очищенной и воды для инъекций
В промышленных условиях получение воды для инъекций и воды очищенной осуществляют с помощью высокопроизводительных корпусных аппаратов, термокомпрессионных дистилляторов различных конструкций и установок обратного осмоса.
К колонным многокамерным аппаратам относятся прежде всего многоступенчатые аппараты. Установки подобного типа для. получения очищенной воды бывают различной конструкции. Производительность крупных моделей достигает 10 т/ч.
Чаще всего применяются трехступенчатые колонные аппараты с тремя корпусами (испарителями), расположенными вертикально или горизонтально. Особенность колонных аппаратов в том, что только первый испаритель нагревается паром, вторичный пар из первого корпуса поступает во второй в качестве греющего, где конденсируется и получается дистиллированная вода. Из второго корпуса вторичный пар поступает в третий - в качестве греющего, где также конденсируется. Таким образом, дистиллированную воду получают из 2-го и 3-го корпусов. Производительность такой установки до 10 т/ч дистиллята. Качество получаемого дистиллята хорошее, так как в корпусах достаточная высота парового пространства и предусмотрено удаление капельной фазы из пара с помощью сепараторов.
Для обеспечения апирогенности получаемой воды необходимо создать условия, препятствующие попаданию пирогенных веществ в дистиллят. Эти вещества нелетучи и неперегоняются с водяным паром. Загрязнение ими дистиллята происходит путем переброса капелек воды или уноса их струей пара в холодильник. Поэтому конструктивным решением вопроса повышения качества дистиллята является применение дистилляционных аппаратов соответствующих конструкций, в которых исключена возможность переброса капельно-жидкой фазы через конденсатор в сборник. Этг достигается устройством специальных ловушек и отражателей, высоким расположение, паропроводов по отношению к поверхности парообразования. Целесообразно также регулировать обогрев испарителя, обеспечивая равномерное кипение и оптимальную скорость парообразования, так как чрезмерный нагрев ведет к бурному кипению и перебросу капельной фазы. Проведение водоподготовки путем обессоливания также уменьшает ценообразование и, следовательно, выделение капелек воды в паровую фазу.
На некоторых химико-фармацевтических предприятиях воду для инъекций получают с помощью дистиллятора «Mascarini» —производительность этого аппарата 1500 л/ч. Он снабжен прибором контроля чистоты воды, бактерицидными лампами, воздушными фильтрами, прибором для удаления пирогенных веществ, а также установкой двойной дистилляции воды производительностью 3000 л/ч.
Трехкорпусной аквадистиллятор «Финн-аква» (Финляндия) функционирует за счет использования деминерализованной воды (рис.12).
Вода поступает через регулятор давления в конденсатор, проходит теплообменники камер предварительного нагрева, а после нагревания поступает в зону испарения, состоящую из системы трубок, обогреваемых внутри греющим паром. Нагретая вода подается на наружную поверхность обогреваемых трубок в виде пленки, стекает по ним и нагревается до кипения.

Рис. 12. Аквадистиллятор «Финн-аква»:
1 — регулятор давления; 2 — конденсатор-холодильник: 3 — теплообменник камер предварительного нагрева; 4 — парозапорное устройство; 5 — зона испарения; 6, 7,8 — труба; 9 ■— теплообменник
В испарителе за счет поверхности кипящих пленок создается интенсивный поток пара, движущийся снизу вверх со скоростью 20— 60 м/с. Центробежная сила, возникающая при этом, обеспечивает стекание капель в нижнюю часть корпуса, прижимая их к стенкам. Наиболее совершенными в настоящее время считаются термокомпрессионные дистилляторы (рис.13), конструкция которых разработана итальянской фирмой «Вопарасе». Их преимущество перед дистилляторами других типов заключается в том, что для получения 1 л воды для инъекций необходимо израсходовать 1,1 л холодной водопроводной воды. В других аппаратах это соотношение составляет 1:9— 1:15. Принцип работы аппарата заключается в том, что образующийся в нем пар, перед тем как поступить в конденсатор, проходит через компрессор и сжимается. При охлаждении и конденсации он выделяет тепло, по величине, соответствующей скрытой теплоте парообразования, которая затрачивается на нагревание охлаждающей воды в верхней части трубчатого конденсатора. Питание аппарата водой осуществляется в направлении снизу вверх, выход дистиллятора — сверху вниз.
Нагревание и кипение в трубках происходит равномерно, без перебросов, в тонком слое. Задерживанию капель из пара способствует также высота парового пространства. Недостатки аппарата — сложность устройства и эксплуатации.Наиболее широко распространенным до последних лет методом получения воды для инъекций была дистилляция. Такой метод требует затрат большого количества энергии, что является серьезным недостатком. Среди других недостатков следует отметить громоздкость оборудования и большую занимаемую им площадь; возможность присутствия в воде пирогенных веществ; сложность обслуживания.
Этих недостатков лишены новые методы мембранного разделения, все больше внедряемые в производство. Они протекают без фазовых превращений и требуют для своей реализации значительно меньших затрат энергии, сопоставимых с минимальной теоретически определяемой энергией разделения.

Рис. 13. Принцип работы термокомпрессионного дистиллятора: 1 - конденсатор-холодильник; 2 - паровое пространство; 3 — компрессор; 4 — регулятор давления; 5 — камера предварительного нагрева: б - трубки испарителя
Мембранные методы очистки основаны на свойствах перегородки (мембраны). обладающей селективной проницаемостью, благодаря чему возможно разделение без химических и фазовых превращений. Для получения воды для инъекций в практическом отношении представляют интерес следующие аппараты.
С использованием принципа мембранной очистки работает установка высокоочищенной воды «Шарья-500». Производительность ее по питающей воде 500 л/ч, получаемая после этой установки высокоочищенная вода, свободная от механических примесей, органических и
неорганических веществ. Она применяется в производстве иммунобиологических бактерийных препаратов и для приготовления инъекционных растворов.
Установка (УВВ) включает блоки предфильтрации, обратного осмоса и финишной очистки.
Блок фильтрации предназначен для очистки питьевой водопроводной воды от механических примесей размером 5 мкм и включает фильтр катионитный и два фильтра угольных, работающих параллельно или взаимозаменяемо.
Блок обратного осмоса работает при давлении не ниже 15 атм. Поступающая на блок вода разделяется после фильтрования на два потока, один из которых проходит сквозь обратноосмотические мембраны, а второй поток, проходящий вдоль поверхности мембраны и содержащий повышенное количество солей (концентрат) отводится из установки. Для обеспечения работы данного блока необходимо, чтобы соотношение объемов воды на подаче, сливе и проходящей через мембрану составляло 3:2:1 соответственно. Таким образом, для получения 1 л высокоочищенной воды необходимо израсходовать приблизительно 3 л воды водопроводной. При этом скорость слива достаточно высока, что устраняет вредное влияние концентрированной поляризации на работу установки.
В блоке обратноосмотическом осуществляется очистка воды от растворимых солей, органических примесей, твердых взвесей и бактерий. Качество воды контролируется по удельному сопротивлению с помощью кондуктометра.
После блока обратного осмоса вода поступает на блок финишной очистки, включающей ионообмен и ультрафильтрацию. Ионообменная очистка воды осуществляется с помощью последовательно соединенных фильтров — катионного и анионного, за которыми установлен смешанный катионно-анионный фильтр, где происходит очистка от оставшихся катионов и анионов.
Окончательная доочистка воды проводится в двух ультрафильтрационных аппаратах с полыми волокнами АР-2.0, предназначенных для отделения органических микропримесей (коллоидных частиц и макромолекул).Для производства иммунных и бактерийных препаратов не всегда пригодна вода для инъекций, полученная дистилляцией. Поэтому часто возникает необходимость в доочистке воды, которая может быть проведена с помощью установки «Супер-Кью». Производительность — 720 л/ч. вода пропускается через угольный фильтр, где происходит освобождение от органических веществ; затем — через смешанный слой ионитов; после чего поступает на патронный бактериальный фильтр с размером пор 0.22 нм (0.00022 мкм). Далее вода поступает на обратноосмотический модуль, где происходит удаление пирогенных веществ. Полученную воду используют для приготовления инъекционных лекарственных форм, а концентрат используют как техническую воду или повторно отправляют на очистку.
Мембранные методы получения высокоочищенной воды для инъекций широко используются в мировой практике и признаны экономически целесообразными и перспективными.
Rp: Benzylpenicillini Sodii 100 000 ED Sol. Ephedrmi hydrochloride 2% 10 ml M.D.S. По З капли в нос 4 раза в день.
Приготовление растворов (капель) с антибиотиками. Водные растворы антибиотиков (капли для глаз, носа) готовят в аптеке по правилам технологии глазных капель в асептических условиях. Многие антибиотики термолабильны, поэтому их растворы не стерилизуют тепловыми методами.
Паспорт
Эфедрина гидрохлорида 0,2
Бензилпенициллина натриевой соли 100 000 ЕД (0.06 г)
Воды для инъекций 10 мл
В асептических условиях в стерильной подставке растворяют приблизительно в 5 мл стерильной воды для инъекций (правило двух цилиндров) 0,2 эфедрина гидрохлорида, кот. получают у провизора-технолога по контролю кач-ва лекарств под роспись и 0,06 г бензилпенициллина натриевой соли. Раствор фильтруют через предварительно промытый стерильный бумажный складчатый фильтр с подложенным тампоном ваты в стерильный флакон нейтрального стекла вместимостью 10 мл. фильтр промывают оставшимся количеством воды для инъекций. Флакон с раствором укупоривают стерильной резиновой пробкой, проверяют раствор на отсутствие механических включений, при необходимости фильтруют вторично. Флакон укупоривают металлическим колпачком «под обкатку» и оформляют этикеткой «Капли». Лек. форму опечатывают и до прихода больного хранят в сейфе в теч. 2 сут.
Осмотическая активность раствора = 0,06*0,15 + 0,2 * 0,28 = 0,065 или 0,65%, раствор явл-ся гипотоничным, т.к. мене 0.9%. На воздухе, при повышении температуры, в присутствии влаги, тяжелых металлов антибиотики быстро разлагаются.
Вопрос 3. Cortex Frangulae (Cortex Frangulae aini) — кора крушины {Frangulae cortex — рутины кора)
Крушины ольховидной, или крушины ломкой, — Frangula alnus Mill. (= Rhamnusfrangula L.) из сем. крушиновых (Rhamnaceae);
Химический состав. Кора крушины содержит до 8 % производных антрацена — франгуларозид, гетеро-и диантроны франгулина, а также мономерные соединения как в восстановленной, так и в окисленной формах (глюкофрангулин, франгулин, франгулаэмодин).
он- —он-----ен— 
Франгуларозид
Заготовка, первичная обработка и сушка. Кору крушины заготавливают весной, в период набухания почек, до начала цветения. В местах, отведенных лесничеством, крушину срубают топором или срезают ножовкой, оставляя пеньки высотой 10-15 см для порослевого возобновления. На срубленных стволиках и толстых ветвях делают кольцевые надрезы на расстоянии 25-30 см друг от друга, которые соединяют продольным надрезом. Снимают кору в виде желобоватых или трубчатых кусков. Нельзя состругивать ее. так как куски получаются узкими и содержат остатки древесины. Кору очищают от лишайников. Заготовку проводят с растений не моложе 8 лет и высотой не менее 3 м. Повторная заготовка на том же месте возможна через 10-15 лет.
Сушат кору крушины на открытом воздухе под навесами или хорошо проветриваемых чердаках, рыхлым слоем, периодически (1-2 раза) переворачивая, следя за тем, чтобы куски не вкладывались друг в друга. При сушке на открытом воздухе на ночь накрывают брезентом или заносят в помещение.
При заготовке неопытными сборщиками возможен сбор коры других сопутствующих растений — жостера, ольхи, рябины, черемухи и различных видов ивы. Кора крушины отличается тем, что при легком соскабливании наружного слоя пробки обнаруживается малиново-красный слой, в то время как у примесей — бурый или зеленый.
Внешние признаки. Цельное сырье. Это трубчатые или желобоватые куски коры различной длины, толщиной 0,5-2 мм. Наружная поверхность темно-бурая, серо-бурая, темно-серая или серая, часто с беловатыми поперечно вытянутыми чечевичками или серыми пятнами. При легком соскабливании наружной части пробки обнаруживается малиново-красный (франгулиновый) слой. Внутренняя поверхность гладкая, желтовато-оранжевого или красновато-бурого
Измельченное сырье представлено кусочками коры различной формы, проходящими сквозь сито с отверстиями диаметром 7 мм.
Крупный порошок. Смесь частиц, проходящих сквозь сито с отверстиями диаметром 2 мм.
Порошкованное сырье желто-бурого цвета, проходящее сквозь сито с отверстиями диаметром 0,16 мм.
Микроскопия. При исследовании поперечных срезов коры крушины виден пробковый слой темно-красного цвета, он представлен 10-20 рядами клеток. Под пробкой располагается пластинчатая колленхима. Клетки паренхимы наружной коры овальные с большим количеством друз кальция оксалата. Механические волокна с малоутолщенными и слабо одревесневшими оболочками. Во внутренней коре сердцевинные лучи часто изогнутые, одно- и двухрядные. Между сердцевинными лучами концентрическими кругами расположены группы толстостенных лубяных волокон, окруженные кристаллоносными обкладками.
При микроскопии измельченного и порошкованного сырья диагностическое значение имеют группы лубяных волокон с кристаллоносной обкладкой, друзы и обрывки темно-красной пробковой ткани.
Подлинность сырья подтверждается также с помощью люминесцентной микроскопии.Качественные реакции. Для диагностики сырья проводят также качественные реакции ьа антраценпроизводные. При смачивании внутренней поверхности коры 1—2 каплями 10% раствора натра едкого наблюдается кроваво-красное окрашивание.
Порошок в количестве 0,5 г кипятят несколько минут с 10 мл 10% спиртового раствора натра едкого и фильтруют. По охлаждении фильтрат подкисляют разведенной хлористоводородной кислотой до слабокислой реакции и прибавляют 10 мл эфира; эфирный слой окрашивается в желтый цвет; 5 мл эфирного извлечения взбалтывают с 5 мл раствора аммиака, последний окрашивается в вишнево-красный цвет (эмодины), эфирный слой остается окрашенным в желтый цвет (хризофанол).
При микровозгонке порошка образуется желтый кристаллический налет, который от прибавления 10% спиртового раствора натра едкого приобретает вишнево-красное окрашивание (производные антрацена).
При проведении реакции Борнтрегера раствор аммиака окрашивается в вишнево-красный цвет (эм
|
|
|


