 |
Определение влажности лекарственного растительного сырья
|
|
|
|
Под влажностью сырья понимают потерю в массе за счет гигроскопической влаги и летучих веществ, которую определяют в сырье при высушивании до постоянной массы.
Аналитическую пробу сырья измельчают до размера частиц около 10 мм, перемешивают и берут две навески массой 3-—5 г, взвешенные с погрешностью ±0,01 г. Каждую навеску помещают в предварительно высушенную и взвешенную вместе с крышкой бюксу и ставят в нагретый до 100—105°С сушильный шкаф. Время высушивания отсчитывают с того момента, когда температура в сушильном шкафу вновь достигнет 100— 105°С. Первое взвешивание листьев, трав и цветков проводят через 2 ч, корней, корневищ, коры, плодов, семян и других видов сырья —- через 3 ч.
Высушивание проводят до постоянной массы. Постоянная масса считается достигнутой, если разница между двумя последующими взвешиваниями после 30 мин высушивания и 30 мин охлаждения в эксикаторе не превышает 0,01 г.
Определение потери в массе при высушивании для пересчета количества действующих веществ и золы на абсолютно сухое сырье проводят в навесках 1— -2 г (точная навеска), взятых из аналитической пробы, предназначенной для определения содержания золы и действующих веществ вышеописанным методом, но при разнице между взвешиваниями, не превышающей 0,0005 г. Контроль качества растворов для инъекций и инфузионных растворов. Контролируют внешний вид раствора (прозрачность, цвет), отсутствие механических включений (дважды — до и после стерилизации раствора): подлинность, рН, количественное содержание лекарственных веществ (до и после стерилизации), а также подлинность и количественное содержание всех вспомогательных веществ (до стерилизации). Для контроля чистоты применяют устройство УК-2, состоящее из корпуса с осветителем, отражателем и экраном, смонтированных на основании. Экран можно поворачивать вокруг вертикальной оси и фиксировать в необходимом положении. Одна рабочая поверхность экрана окрашена эмалью черного цвета, другая — белого. Источником освещения служат две электрические лампочки мощностью 40 — 60 Вт.
|
|
|
Растворы просматривают невооруженным глазом на расстоянии до 25 см от флакона.
Маркировка изготовленных препаратов (оформление к отпуску). Флаконы и бутылки с растворами оформляют согласно действующим единым правилам оформления лекарств, изготовленных в аптеках.
Оформление основной этикетки и подготовка дополнительных этикеток (надписей) для флаконов с инъекционными растворами в аптеке лечебно-профилактического учреждения, осуществляется до начала изготовления. На основной этикетке синего цвета с надписью «Для инъекций» или «Стерильно» должны быть номер рецепта или требования, название раствора, концентрация, объем, путь введения (внутривенно, для инфильтрационной анестезии и т.п.), адрес, номер больницы, название отделения больницы, номер аптеки, дата изготовления, срок годности, теоретическая осмолярность (для инфузионных растворов), кто изготовил, проверил, отпустил, серия, номер анализа, цена. В необходимых случаях флакон снабжают дополнительными этикетками или надписями «Беречь от детей», «Сохранять в прохладном месте», «Хранить в темном месте».
Если раствор не стерилизовался, то. зачеркнув «Стерильно», помещают этикетку «Изготовлено асептически». Заполняют сигнатуру, если в прописи содержатся вещества списка А и наркотические средства. На рецепте (требовании) указывают количество изотонирующих и стабилизирующих веществ.
При отпуске стерильных растворов еще раз проверяют правильность оформления сопроводительных документов: ППК, рецепта, этикетки, сигнатуры.
|
|
|
Условия и сроки хранения. Срок годности растворов, стерилизованных насыщенным паром и укупоренных под обкатку, как правило, составляет 30 дней.
Значительно меньший срок хранения имеют растворы новокаина 5 % для спинномозговой анестезии и раствор Рингера—Локка после смешивания двух растворов — 1 сут. натрия нитрита 1 %, натрия тиосульфата 30 %, викасола 1 %, глюкозы 40 % с кислотой аскорбиновой 1 %, глюкозы 25 % с метиленовым синим 1 %. новокаинамида 10 %, пиридоксина гидрохлорида 1 %, 2,5 %, 5 %, платифиллина гидротартрата 0,2 %, прозерина 0,05 %, промедола 1 % и 2 %, тиамина бромида 3 % и 6 %. эуфиллина 2,4 % и некоторые другие — двое суток, натрия парааминосалицилата 3 %, кальция глюконата 10 %, фурагина растворимого 0,1 % — 7 сут.
Срок хранения многих растворов, благодаря стабилизации, высокой степени чистоты лекарственных веществ и стерилизации, более 30 сут.
Например, 5-, 10-. 20-. 30%-ные растворы глюкозы, изготовленные без стабилизатора, раствор кардиоплегический № 2, растворы дибазола 0,5- и 1%-ный. кислоты никотиновой 1%-ный имеют срок хранения 60 сут.
90 сут могут храниться растворы глюкозы 5-, 10-, 20-, 40%-ный со стабилизатором Вейбеля, глюкозы 5%-ный с калием хлоридом 0,5- или 1%-ного, натрия хлорида 0.9- и 10%-ного, новокаина 0,25-. 0,5-, 2-, 5-, 10%-ных. В течение 180 сут могут храниться растворы кардиоплегический № 1; этазола-натрия 10- и 20%-ный. В течение 1 года — раствор кардиоплегический № 3.
Хранить растворы следует в прохладном, защищенном от света месте.
После вскрытия упаковки и неполном использовании раствор не подлежит хранению.Влажность сырья (X) в процентах вычисляют по формуле: Х*=(м—м1)*100/м
где т ■— масса сырья до высушивания в граммах; ml — масса сырья после высушивания в граммах.
За окончательный результат определения принимают среднее арифметическое двух параллельных определений, вычисленных до десятых долей процента. Допускаемое расхождение между результатами двух параллельных определений не должно превышать 0.5%.
ОПРЕДЕЛЕНИЕ ЗОЛЫ
Около 1 г препарата или 3—5 г измельченного лекарственного растительного сырья (точная навеска) помещают в предварительно прокаленный и точно взвешенный фарфоровый, кварцевый или платиновый тигель, равномерно распределяя вещество по дну тигля. Затем тигель осторожно нагревают, давая сначала веществу сгореть или улетучиться при возможно более низкой температуре. Сжигание оставшихся частиц угля надо тоже вести при возможно более низкой температуре; после того как уголь сгорит почти полностью, увеличивают пламя.
|
|
|
При неполном сгорании частиц угля остаток охлаждают, смачивают водой или насыщенным раствором аммония нитрата, выпаривают на водяной бане и остаток прокаливают. В случае необходимости такую операцию повторяют несколько раз.
Прокаливание ведут при слабом красном калении (около 500 °С) до постоянной массы, избегая сплавления золы и спекания ее со стенками тигля. По окончании прокаливания тигель охлаждают в эксикаторе и взвешивают.
Вопрос 4. Рецепт выписан правильно. Оплата производится через кассовый аппарат наличными. НЕО не регламентированы. Рецепт, выписанный правильно, таксируется, т. е. определяется его розничная цена. В аптеках с оборудованным АРМ этот процесс происходит с помощью различного программного обеспечения (на компьютерах). Розничная цена на экстемпоральные лекарственные формы и внутриаптечную заготовку складывается:
из стоимости исходных ингредиентов;
стоимости аптечной посуды; тарифа за изготовление лекарства.
Аптекам — юридическим лицам предоставлено право самостоятельно разрабатывать тарифы за изготовление и расфасовку ЛС.
Тарифы должны быть утверждены приказом по аптеке. В основу тарификации положены:
нормативы затрат времени на отдельные операции по изготовлению, контролю, фасовке и отпуску экстемпоральных лекарственных форм и внутриаптечной заготовки (разработаны ВНИИФ);
стоимость 1 мин рабочего времени, рассчитанная с учетом средней заработной платы.
К сумме ингредиентов (0,54 +1.25 + 4,18 + 1,2) прибавляем стоимость склянки (3.68) и тариф за изготовление жидких лекарственных форм: 10,0 за 3 ингредиента и за каждый последующий ингредиент (0.7 х 1 = = 0,7).
Итого стоимость лекарственной формы: 0,54 + 1,25 + 4.18 + 1,2 + 3,68 + ■+ 10.0 + 0.7 = 21,05 (р.).
Регистрации рецептов. Для рецептов, требующих индивидуального изготовления, регистрация может осуществляться различными способами. Наиболее распространенной является квитанционная форма регистрации рецептов. Квитанция заполняется в одном экземпляре при приеме рецептов. Условно в ней можно выделить три части. Первая часть (корешок) квитанции с указанием номера лекарства, Ф.И.О. больного, стоимости и ЛФ остается в аптеке. Корешок квитанции служит основанием для учета ЛС, изготовленных по рецептам. По корешкам в конце смены подсчитывают количество принятых рецептов и общую стоимость отпущенных по ним лекарств. В целях учета корешки комплектуются по 50 и 100 шт. и хранятся в аптеке. 
|
|
|
Соединения магния количественно определяют прямым комплексонометрическим методом с использованием индикатора кислотного хром черного специального (эриохром черный Т). После добавления индикатора к титруемому раствору ионы магния образуют с ним непрочное комплексное соединение:
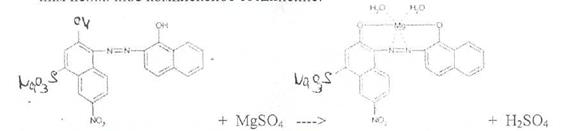
Титрант — 0,05 М раствор трилона Б (ЭДТАХ^г) связывает находящиеся в растворе ионы магния в комплексное соединение;

Поскольку при этом происходит выделение серной кислоты, для поддержания оптимального значения рН среды необходимо прибавлять аммиачный буферный раствор.
В эквивалентной точке, когда все ионы магния будут связаны в комплексное соединение металл — ЭДТА Na2, титрант вступает во взаимодействие с ионами магния, содержащимися в составе комплекса металл — индикатор. Последний имеет меньшую константу устойчивости, чем комплексное соединение ЭДТА Na2 ■— металл, поэтому происходил разрушение комплекса индикатора с ионами магния. При этом красно-фиолетовая (окраска раствора переходит в синюю окраску свободного индикатора:
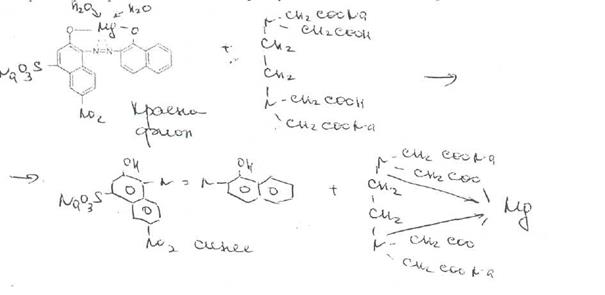
Соединения магния хранят в хорошо укупоренной таре, так как магния сульфат в плохо укупоренной таре постепенно теряет кристаллизационную воду.
Вопрос 2. Требования, предъявляемые к инъекционным лекарственным формам.
1. Стерильность - отсутствие жизнеспособных микроорганизмов и их спор.
2. Апирогенность - отсутствие продуктов жизнедеятельности и распада микроорганизмов.
3. Стабильность - неизменяемость по составу и количеству находящихся в растворе лекарственных веществ в течение установленных сроков хранения
4. Отсутствие механических включении - прозрачность инъекционного раствора (или отсутствие каких-либо взвешенных частиц)
Обеспечить эти требования должен весь технологический процесс (помещения, технологическое оборудование, упаковка, система вентиляции, транспортные системы ввода сырья и вывода готового продукта, обслуживающий персонал).
|
|
|
Большая часть инъекционных препаратов является лекарственными формами промышленного производства (ампулы, флаконы, шприц-тюбики).
В аптеках готовят растворы для инъекций, которые отпускают в герметично укупоренных флаконах вместимостью 5—1000 мл. На флаконы наклеиваются этикетки «Стерильно».
Технология инъекционных препаратов — сложный многостадийный процесс, состоящий из основных и вспомогательных этапов. Условия изготовления лекарственных форм для инъекций должны быть асептическими, т. е. исключающими попадание в готовый продукт микроорганизмов и механических частиц. Только после определения способов стерилизации для различных инъекционных лекарственных форм стало возможно их практическое применение.
Выработаны специальные условия выполнения стадий и операций технологического процесса для соответствия готового раствора требуемым стандартам.
Повышенные требования предъявляются к следующим объектам:
1) производственным помещениям;
2) технологическому оборудованию;
3) системам подготовки основных и вспомогательных материалов;
4) вентиляции;
5) обслуживающиему персоналу.
На каждой из стадий производственного процесса существует угроза микробной контаминации и внесения в раствор загрязнений иного рода. Технология ампулир о ванных препаратов: 1) получение ампул (флаконов);2) подготовка ампул (флаконов) к заполнению. Параллельно с этими процессами идут:
1) получение и подготовка растворителей;
2) приготовления раствора. Далее производят:
1) ампулирование (наполнение и укупорку флаконов):
2) стерилизацию;
3) контроль качества, маркировку и упаковку.
Особенно ответственно нужно подходить к стадиям получения раствора и ампулирования.
Принимая во внимание то, что в городском воздухе содержится от 100 000 до 1 000 000 частиц размером 0,5 мкм и более в 1 л, в 1982 г. в нашей стране были введены «Требования к помещениям для производства лекарственных средств в асептических условиях РДП 46-3-80».
Все производственные помещения в соответствии с этими требованиями следует делить на четыре класса:
Ранее системы очистки и вентиляции воздуха в производственных помещениях обеспечивали содержание в 1 л около 1000 частиц. Эти параметры не отвечали требуемым условиям асептики, так как изначально на 1000 частиц в воздухе приходится 1 микроорганизм, а каждый член персонала при дыхании за 1 мин в неподвижном состоянии выделяет 100 000 частиц, а при ходьбе до 10 000 000 частиц.
Одной из характеристик данных систем являлось то, что они создавали турбулентные потоки, смешивающие чистый фильтрованный воздух с поступающим нефильтрованным, при этом происходило разбавление концентрации взвеси частиц в воздухе помещения.
Для того чтобы избавиться от данного недостатка, были разработаны системы с применением ламинарного потока фильтрованного воздуха со скоростью около 27,5 м/мин по всему сечению помещения.
В результате был достигнут допустимый результат — содержание 10 частиц в 1 л воздуха.
Автономный ламинарный поток стерильного воздуха применяется для создания условий сверхчистых помещений или отдельных зон внутри помещения (размещаемых в виде специального блока).
При применении данной технологии чистота воздуха достигает 1 частицы в 1 л, что соответствует условиям стерильности и асептики.
Между помещениями разных классов чистоты устанавливают шлюзовые соединения, создается подпор воздуха 533,288 Н/м.
НПП рекомендует для обеспечения стерильности продукции использовать способы производства, сводящие к минимуму или устраняющие присутствие персонала в производственных помещениях, например, полностью замкнутые и автоматизированные системы.
Использование изолирующих технологий (GMP ЕС) сокращает необходимость присутствия человека в производственных зонах, в результате чего значительно сокращается риск микробной контаминации продукции, производимой в асептических условиях, из окружающей среды. Изолирующие технологии.предусматривают применение различныхтипов изоляторов и передаточных устройств. Изолятор и окружающая его среда должны быть спроектированы таким образом, чтобы в соответствующих рабочих зонах достигалось требуемое качество воздуха. Возможно использование полностью герметизированных систем, включающих оборудование для стерилизации.
GMP (правила надлежащего производства) - это единая система требований по организации производства и контролю качества лекарственных средств от начала переработки сырья до производства готовых продуктов, включая общие требования к помещениям, оборудования и персоналу. В России данную функцию выполняет руководящий нормативный документ РД 64-125-91 "Правила организации производства и контроля качества лекарственных средств", утвержденный приказом Министра медицинской промышленности СССР в 1992 г.
Согласно данному документу все помещения для производства лекарств в асептических условиях делятся на 4 класса в зависимости от чистоты воздуха.
Во время технологического процесса производства инъекционных растворов обязательно проводят промежуточный (постадийный) контроль качества, т. е. после каждой технологической стадии или операции проводится бракераж ампул, флаконов, гибких контейнеров, не отвечающих определенным требованиям. Так, после растворения (изотонизации, стабилизации и т. д.) лекарственного вещества, контролируется качественный и количественный состав. рН раствора, плотность и др.; после операции наполнения — проверяется выборочно объем наполнения сосудов.
Определение норм наполнения. Фактический объем наполнения сосудов должен быть больше номинального, чтобы обеспечить нужную дозу при наполнении шприца. ГФ XI издания устанавливает нормы налива и количества сосудов для контроля. В сосудах вместимостью до 50 мл наполнение проверяют калиброванным шприцем, в сосудах вместимостью 50 мл и более — калиброванным цилиндром при температуре 20±2 °С. Таблица норм наполнения ампул растворами приведена выше.
Определение герметичности. Контроль качества запайки или укупорки проходят 100% сосудов и для определения герметичности используют 3 метода:
— вакуумирование;
— с помощью растворов индикаторов (для водных растворов) и воды или мыльного раствора (для масляных растворов);
— по свечению газовой среды внутри сосуда под действием высокочастотного электрического поля.
Контроль на механические включения. Проводят путем просмотра сосудов на черном и белом фоне при освещении 60 Вт. На черном фоне проверяются прозрачность и наличие механических включений — стеклянная пыль, волокна фильтрующих материалов, нерастворенные частицы лекарственного вещества и т. д.; на белом — цветность раствора, отсутствие механических включений черного цвета и целостность стеклянного изделия. Метод имеет недостатки: субъективизм контролера — острота зрения, опыт работы, усталость и т. д. Допустимая ошибка метода составляет 30%.Для более объективной оценки качества раствора по этому параметру были разработаны другие методы:
— визуально-оптические, основанные на использовании проекторов, увеличительных линз, поляризационного света и т. д.;
, — оптические, с автоматической регистрацией фотоэлементами поглощения или рассеивания проходящего света;
— мембранно-микроскопические;
— проточные методы.
Количественное содержание лекарственных веществ, входящих в состав инъекционных растворов, определяют согласно указаниям ФС или другой нормативно-технической документации. Определение количественного состава проводится на каждой серии раствора.
Препараты, анализируемые биологическим методом, должны содержать активные ингредиенты в пределах, указанных в соответствующей НТД.
Определение стерильности растворов проводится путем посева и инкубации на специальных тест-средах образцов каждой серии продукции. При обнаружении роста микроорганизмов хотя бы в одной пробирке испытание повторяют на таком же количестве сосудов. И только при отсутствии роста при повторном посеве серия считается стерильной. Определению стерильности подвергают ампулы или флаконы каждой серии, одновременно подвергавшиеся стерилизации в одном стерилизующем аппарате.
Метод мембранного фильтрования при определении стерильности рекомендован при выраженном антимикробном действии лекарственного вещества и испытании растворов в больших объемах (более 100 мл). Отбирается 30 ампул, их делят на 3 группы по 10 штук, 20 используют для испытания на стерильность, 10 — для контроля полноты отмывания мембраны от лекарственного вещества. Для фильтрования применяют установку с мембраной диаметром 47 мм и размером пор 0,45±0,02 мкм. Фильтры стерилизуют при температуре 121±1 °С 20 мин. Если испытывают порошок, его растворяют в воде для инъекций, фильтруют через стерильную мембрану, которую промывают от раствора 3—5 порциями растворителя по 100 мл, разрезают стерильными ножницами на 2 части, одну из них помещают в колбу с тиогликолевой средой, вторую — в среду Сабуро, 7 дней инкубируют при ежедневном просмотре. Все операции проводят в асептических условиях. При отсутствии роста на двух средах делают заключение о стерильности серии.
Определение пирогенности растворов проводят биологическим методом согласно ГФ XI издания. За рубежом широко применяют лимулус-тест (лим-тест), основанный на образовании геля при взаимодействии бактериальных пирогенов с лизатом амебоцитов крови крабов Liraulus polyphemus. В России разработан аналогичный метод, основанный на способности грамотрицательных микроорганизмов (основные продуценты пирогенных веществ) образовывать гель в 3% растворе калия гидроксида.
Оборудование для наполнения ампул.
В технологическом процессе ампулирования применяют три известных способа наполнения ампул: вакуумный, шприцевой и пароконденсационный. Вакуумный способнашел широкое распространение в отечественной промышленности. Этот способ по сравнению со шприцевым, яв%Ясь групповым, обладает более чем в 2 раза большей производительностью при точности дозирования ±10—15%. Так, производительность наполнительного аппарата Мариупольского завода достигает 25 тыс. мелкоемких ампул в час, тогда как автомата шприцевОГо наполнения фирмы «Штрунк» только 12 тыс. ампул.
Вакуумный способ наполнения заключается в том, что ампулы в кассетах помещают в герметичный аппарат, в емкость которого заливают раствор, подлежащий наполнению, и создают вакуум; при этом воздух из ампул отсасывается, и после сброса вакуума раствор заполняет ампулы.
При вакуумном способе дозирование раствора в ампулы производится с помощью изменения глубины разрежения, т. е. фактически регулируется объем, подлежащий заполнению, при этом сама амПула является дозирующей емкостью. Ампулы с разными объемами заполняются при соответственно созданной глубине вакуума в аппарате.
Для точного наполнения ампул с помощью вакуума предварительно определяют глубину создаваемого разрежения. Обы^но на заводах составляются таблицы необходимой степени разрежения в зависимости от атмосферного давления, размеров ампул и требуемого объема наполнения. В случаях, когда та^их таблиц нет, ампулы наполняют при рабочем разрежении, дающем объем наполнения несколько больше и меньше требуемого, и методом интерполяции рассчитывают его искомую глубину.
Невозможность точного дотирования раствора — основной недостаток вакуумного способа наполнения. К другие недостаткам можно отнести также то, что ампулы при наполнении погружаются капиллярами в дозируемый раствор, через него при создании вакуума проходят пузырьки отсасываемого воздуха, и в ампулы попадает только часть раствора, большая часть которого остается в аппарате и после цикла наполнения сливается из аппарата на перефильтращцо; все это приводит к дополнительному загрязнению и неэкономному расходу раствора. Кроме того, при наполнении загрязняются капилляры ампул, в результате чего при запайке образуются нежелательные «черные» головки от пригара раствора на конце капилляра. К недостаткам вакуумного способа наполнения следует отнести также и то, что после наполнения до проведения операции запайки ампул проходит значительный, по сравнению с0 шприцевым методом наполнения, интервал времени, отрицательно сказывающийся на чистоте раствора и требующий применения специальных устройств для заполнения капилляра инертным газом. При применяемой отечественной технологии между наполнением и запайкой ампул проходит более 3 мин. Большой промежуток времени создает дополнительные условия для загрязнения раствора в ампулах механическими частицами и микрофлорой из окружающей среды.
К преимуществам вакуумного способа наполнения ампул, кроме высокой производительности, можно отнести универсальность размеров и форм капилляров наполняемых ампул. За рубежо^ вакуумный способ наполнения ампул применяется только для недорогих препаратов и питьевых растворов.
Полуавтомат для наполнения ампул состоит из корпуса с укрепленной в нем емкостьюаппарата, внутри которой имеется ложное дно, удерживаемое на патрубке для подач раствора. Патрубок снабжен насадкой с боковыми щелями непосредственно над верхне плоскостью ложного днища. Емкость аппарата имеет нижний спуск с клапаном и на боково. стенке — упоры для установки на них кассеты с ампулами. Сверху аппарат закрыт крышкой имеющей автоматический пневмопривод для ее открывания и закрытия.
Нижний спуск выведен в приемную емкость. Для замера вакуума автомат оснаще* контактными вакуумманометрами. К емкости аппарата подсоединены трубопроводь питания раствором с вакуумной магистралью цеха. Процесс работы автоматизирован.

Рис.15. Схема полуавтомата для наполнения ампул (модель АП-4М2):
1 — корпус; 2 — крышка; 3 — кассета с ампулами; 4 — ложное дно; 5 — патрубок подачи раствора; б — клапан нижнего спуска; 7 —- емкость для слива раствора из аппарата; <?— контактный вакуумманометр (наполнение аппарата); 9 — контактный вакуумманометр
(дозирование раствора при наполнении ампул): 10 — трубопровод подачи раствора; II — вакуумпровод
В емкость устанавливают кассету с ампулами, закрывают крышку и в аппарате создают вакуум, при этом клапаном на нижнем спуске герметизируют аппарат. Подают раствор. Под воздействием вакуума раствор струями поступает из щелей насадки и, омывая верхнюю поверхность ложного дна, стекает под ложное дно, смывая туда механические частицы. Затем в аппарате создают требуемое разрежение, соответствующее дозе раствора, заполняемого в ампулу, и гасят вакуум. Оставшийся в аппарате раствор сливается в приемную емкость и идет на перефильтрацию. Производительность полуавтомата — 60 кассет в час. Длительность цикла наполнения 50 с. После наполнения ампул вакуумным способом в капиллярах ампул остается раствор, что мешает качественной запайке и загрязняет инъекционный раствор продуктами сгорания.
Растворы из капилляров ампул можно удалить:
— отсасыванием раствора под вакуумом:
- продавливанием раствора стерильным воздухом или инертным газом (в полуавтомате АП-5М2);
■— обработкой струей пара или водой апирогенной.
Полуавтомат для продавливания раствора из капилляров в ампулу типа АП-5М2. В сорпусе полуавтомата установлена емкость с крышкой. К емкости присоединены системыпитания сжатым воздухом, инертным газом, вакуумом, она также соединена с атмосферой. Емкость имеет нижний спуск. Крышка аппарата имеет привод и запорные устройства. Цикл работы автоматизирован. В емкость устанавливают кассету с ампулами, затем заполняют фильтрованным воздухом. Вакуумом закрывают крышку аппарата, создают в аппарате давление. В полуавтомате можно проводить задавливание раствора из капилляров в ампулы емкостью 1 — 20 мл. Производительность аппарата (ампулы 1—2 мл) составляет 40 тыс. ампул в час. Давление воздуха при продавливании раствора составляет 2—5 кГ/см2.
Шприцевой способ наполнения ампул получил широкое распространение за рубежом и осуществляется при помощи установок со специальными дозаторами (поршневыми, мембранными и др.). Метод имеет более сложное аппаратурное оформление, чем вакуумный и более жесткие требования к размерам и форме капилляров ампул, но из-за ряда преимуществ относится к более предпочтительным для применения в технологии ампулирования. При проведении операций наполнения и запайки в одном автомате особенно сказываются эти преимущества.


ампул в час.
В настоящее время создан ряд конструкций дозирующих элементов, работающих без движущих частей,- что позволяет полностью предотвратить загрязнение раствора в процессе дозирования. Ряд зарубежных фирм применяют для этой цели перистальтические насосы, различные дозаторы мембранного типа. Ввод дозы в ампулу под давлением позволяет применить при наполнении дополнительную фильтрацию раствора непосредственно в момент наполнения, что дает возможность гарантировать чистоту, а при фильтрации с помощью ультрафильтра — и стерильность раствора в ампуле.
Пароконденсационный способ. На основе пароконденсацион-ного способа мойки ампул сотрудниками ГНЦЛС предложена принципиально новая технологическая линия амаудирования инъекционных растворов
Охлаждение Стерильный воздух или СО:, Nz аргон

Рис.16. Принципиальная схема ампулирования инъекционных растворов на основе пароконденсационного способа
Ампулы после резки 1 полностью погружают капиллярами вверх в емкость 2 с водой, снабженную ультразвуковыми излучателями. При воздействии ультразвука ампулы быстро заполняются водой и тут же дополнительно озвучаются. После этого ампулы переводят в положение «капиллярами вниз» и направляют в камеру, где промывают сначала наружную поверхность душированием 3, а затем внутреннюю пароконденсационным способом. Во время выхода воды из ампул их подвергают вибрации 4 с целью максимального удаления из них механических частиц. Ампулы после промывки поступают в камеру для дозированного заполнения раствором пароконденсационным способом 5 и запайки б. Промывная вода непрерывно фильтруется 7 и возвращается в схему.
Ампулы перед запайкой несколько охлаждают для того, чтобы удалить раствор из капилляров, после чего их концы опускают в емкость с жидкой пластмассой б и тут же вынимают; капли пластмассы, удерживаемые на концах капилляров, затвердевают и герметически закупоривают ампулы с раствором.
Отдельные элементы пароконденсационного способа нашли применение при создании автоматизированных линий ампулирования типа «АП-30». установки для термической 

Колич. опред. эфирных масел: Взятие навеси, измельчение, просеивание. Содержание эфирного масла определяют методом 1 или 2 путем перегонки с водяным паром из ЛРС с последующим измерением объема. Расчет содер масла в объемно-весовых % в пересчете на абсолютно сухое сырье.
Заготовка сырья, первичная обработка и сушка. Заготовку сырья проводят в фазу цветения. Срезают секаторами или серпами верхние части цветоносных побегов без грубых одревесневших оснований стеблей. Не следует выдергивать растения с корнями, так как это ведет к уничтожению зарослей.
Информация для потребителей: смотри Билет №1. Вопрос 4.
Билет №29. Возрос 1.
Большинство сердечных гликозидов по химическому строению представляют собой карденолиды. Их агликоны имеют общую формулу

и отличаются друг от друга радикалами R, XI, Х2, ХЗ
Агликоны Радикалы ____________^______
________________R_________ХЗ_______ Х2 XI
Дигитоксигенин -СНз _
Молекула сердечного гликозида включает один, два или три остатка Сахаров, соединенных в положении с агликоном а- или в-гликозидной связью.
При гидролитическом расщеплении, а также при хранении и высушивании сырья под действием энзимов первичные гликозиды разрушаются с образованием вторичных гл икозидов и других продуктов гидролиза. ________________________________
Вид Первичные Продукты Вторичные
наперстянки гликозиды _________ гидролиза г ликозиды
Наперстянка Пурпуреагликозид Глюкоза Дигитоксин
пурпуровая
Вторичные гликозиды обоих видов наперстянок после потери указанных продуктов гидролиза состоят из агликонов и сахарной части, причем последняя у всех трех вторичных гликозидов одинакова
Химически й состав втори чных гликозидов наперстянок
Вторичный * Агликон Сахарная часть
гликозид __________________________^______^_^__^____-__^_
Дигитоксин Дигитоксигенин Три молекулы дигитоксозы
Формула дигитоксина (вторичного гликозида): Digitoxin — дигитоксин

Дигитоксин применяют в виде индивидуальных лекарственных веществ.Срезанные части растений сушат на открытом воздухе в тени, под навесами, в хорошо проветриваемых помещениях, на чердаках, рассыпая слоем толщиной 5-7 см и периодически перемешивая; в сушилках — при температуре 35-40 °С. Затем траву обмолачивают и отделяют грубые стебли на решетах или веялках.
Стандартизация. Качество травы чабреца должно отвечать требованиям ГФ XI,
Числовые показатели. Цельное сырье. Экстрактивных веществ, извлекаемых 30 %-ным спиртом, не менее 18 %; влажность не более 13 %; золы общей не более 12 %; золы, нерастворимой в 10 % кислоте хлористоводородной, не более 5 %; кусочков стеблей толщиной свыше 0,5 мм не более 10 %: органической примеси не более 1 %; минеральной — не более 1 %.
Хранение. Сырье хранят на стеллажах в прохладных помещениях отдельно от других видов сырья. Срок годности цельного и измельченного сырья 2 года; порошка полтора года.
Использование. Траву чабреца используют в виде настоя как отхаркивающее средство, а также при радикулитах и невритах как болеутоляющее. В специальных клиниках настой назначают и для лечения хронического алкоголизма у женщин. Жидкий экстракт чабреца входит в состав препарата «Пертуссин». Трава чабреца используется как пряность в пищевой, парфюмерно-косметической, ликеро-водочной промышленности. Растение входит в арсенал лекарственных средств гомеопатии. Входит в состав БАДов, используемых как общеукрепляющее и легкое тонизирующее средство. Пряность.
Вопрос 4. Рецепт выписан не верно. Рецепт должен быть выписан на бланке ф. №107/У, заверенный личной печатью и подписью врача.
Срок действия рецепта - 2 мес. Рецепт отдается больному с указание на обороте количества отпущенного препарата и даты отпуска и не хранится в аптеке. По истечении срока действия рецепт гасится штампом «Рецепт не действителен».
Способ применения ЛС обозначается на русском или русском и национальном языках с указанием дозы, частоты, времени приема и его длительности.
Все неправильно выписанные рецепты остаются в аптеке, погашаются штампом «Рецепт недействителен» и регистрируются в специальном журнале. Информация о них передается руководителю соответствующего ЛПУ для принятия мер дисциплинарного воздействия к работникам, нарушающим правила выписывания рецептов.
Готовые средства укладываются в упаковке этикеткой наружу. На шкафы и полки прикрепляется стеллажная карта, в которой отражены наименование лекарства, серия и срок годности.
Такая карта заводится на каждую вновь поступившую серию, что позволяет осуществлять контроль своевременной ее реализации.
В отделе должна находиться картотека по срокам годности препаратов.
Лекарственные средства с истекшим сроком годности хранятся отдельно и подлежат переконтролю (после получения результатов анализа).
Инъекционные препараты хранят в прохладном темном месте в шкафу или изолированном помещении.Свойства и стандартизация сердечных гликозидов
Белый кристаллический порошок. Практически нерастворим в воде, мало растворим в этаноле, трудно — в хлороформе. Удельное вращение от +16 до +19 ° (1 %-ный раствор в хлороформе)
Объективную оценку подлинности сложных по химической структуре индивидуальных сердечных гликозидов позволяет сделать ИК-спектр, снятый после прессования в таблетках с бромидом калия в области 4000-400 см"1.
Для установления подлинности сердечных гликозидов могут быть использованы общие химические реакции. Первая группа цветных реакций позволяет обнаружить наличие стероидного цикла в молекуле, например реакция Либермана — Бурхардта. Она основана на способности стероидов к дегидратации под действием уксусного ангидрида и концентрированной серной кислоты. В результате реакции слой уксусного ангидрида окрашивается в зеленый цвет.
Стероидный цикл в карденолидах обнаруживают флуориметрическим методом, используя в качестве реактива смесь фосфорной и серной кислот с хлоридом железа (III), раствор перхлората железа в серной кислоте и др. Реакции приемлемы тогда, когда анализируемый гликозид в результате дегидрирования образует окраше
|
|
|


