 |
Электродный потенциал. Стандартный электродный потенциал. Ряд стандартных электродных потенциалов
|
|
|
|
Теоретические аспекты электрохимических процессов
Какие процессы называются электрохимическими?
Все электрохимические процессы можно разделить на две противоположные группы: процессы электролиза, при которых под действием внешнего источника электроэнергии происходят химические реакции, и процессы возникновения электродвижущей силы и электрического тока вследствие определенных химических реакций.
В первой группе процессов электрическая энергия превращается в химическую, во второй ‒ наоборот, химическая ‒ в электрическую.
Все электрохимические реакции происходят при протекании электрического тока в цепи. Этот круг обязательно состоит из последовательно соединенных металлических проводников и раствора (или расплава) электролита. В металлических проводниках ток переносят электроны, в растворе электролитов ‒ ионы. Непрерывность протекания тока в цепи обеспечивается только тогда, когда происходят процессы на электродах, т.е. на границе металл ‒ электролит. На одном электроде происходит процесс приема электронов ‒ восстановление, на втором электроде - процесс отдачи электронов, т.е. окисления.
Особенностью электрохимических процессов, в отличие от обычных химических, является пространственное разделение процессов окисления и восстановления. Из этих процессов, которые не могут происходить друг без друга, и состоит в целом химический процесс в электрохимической системе.
В чем заключается сущность механизма образования электродного потенциала?
Гальванический элемент (химический источник тока) – это устройство, в котором химическая энергия окислительно-восстановительной реакции превращается в электрическую. Гальванический элемент состоит из двух электродов (полуэлементов).
|
|
|
Система, в которой металл погружен в раствор собственной соли, называется электродом или полуэлементом. При погружении металлической пластинки в раствор собственной соли имеют место два основных процесса. Первый процесс – это ионизация металла пластинки, где в узлах кристаллической решетки находятся ионы – атомы:
 .
.
Ионизация происходит под действием полярных молекул растворителя (воды). Образующиеся при этом электроны концентрируются на пластинке, заряжая ее отрицательно, а образующиеся катионы металла переходят с пластинки в раствор и концентрируются возле пластинки (рис. 1).

Рисунок1 – Схема металлического электрода
Второй процесс – это взаимодействие молекул растворителя с ионами металла, т.е. сольватация образующихся ионов:
 .
.
При погружении пластинки металла в раствор вначале преобладает процесс ионизации металла, но со временем скорость прямой реакции уменьшается, а растет скорость обратной реакции, пока между этими процессами не установится динамическое равновесие
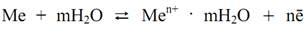
При этом на границе металл-раствор (твердая фаза — жидкость) устанавливается равновесный двойной электрический слой (ДЭС), состоящий из положительных ионов и электронов. Условное обозначение системы металл-раствор – Ме/Меn+, где вертикальной чертой отмечена граница раздела твердая фаза-раствор.
Электродный потенциал. Стандартный электродный потенциал. Ряд стандартных электродных потенциалов
Между положительными ионами и электронами возникает скачок потенциала, который называется электродным потенциалом. Потенциал, возникающий в условиях равновесия электродной реакции, называется равновесным электродным потенциалом.
Значение электродного потенциала, возникающего на границе металл-раствор, зависит от природы металла, активности ионов этого металла и от температуры.
|
|
|
Абсолютное значение электродного потенциала в настоящее время измерить или рассчитать невозможно. Но можно определить значение электродного потенциала относительно какого-либо электрода, выбранного в качестве стандарта. Согласно международному соглашению таким стандартом служит стандартный (нормальный) водородный электрод, потенциал которого условно принят за нуль:  = 0.0 В.
= 0.0 В.
Стандартный водородный электрод представляет собой платиновую пластинку, покрытую платиновой чернью и опущенную в раствор Н2SO4 или HCI с  = 1 моль/л, через который все время пропускается газообразный Н2 под давлением 101.3 кПа при 298 К (рис. 2).
= 1 моль/л, через который все время пропускается газообразный Н2 под давлением 101.3 кПа при 298 К (рис. 2).

Рисунок 2 – Водородный электрод
Платина, отличающаяся высокой химической стойкостью, в электродном процессе не участвует. Ее роль сводится к адсорбции на своей поверхности водорода и переносу электронов. На поверхности платины протекает процесс:
H2 ⇄ 2Н+ + 2  .
.
Если пластинку любого металла соединить со стандартным водородным электродом, то получим значение стандартного электродного потенциала данного металла.
Располагая металлы в порядке увеличения стандартных электродных потенциалов, получают электрохимический ряд напряжений металлов. Металлы, стоящие в ряду напряжений после водорода, не способны вытеснять водород из кислот. Вытеснение металла из солей другим металлом осуществляется только в том случае, если вытесняющий металл расположен в ряду напряжений до вытесняемого. Чем дальше друг от друга удалены металлы в электрохимическом ряду напряжений (т.е. чем больше разница между стандартными потенциалами металлов), тем больше ЭДС гальванического элемента, в котором эти металлы использованы.
Стандартные потенциалы являются количественной мерой окислительно-восстановительной способности системы. Чем выше значение φ0, тем большей окислительной способностью обладает окисленная форма данной пары. Восстановительные свойства сильнее выражены у восстановленной формы в паре с меньшим значением φ0.
Все металлы в ряду напряжений делятся на: активные (литий – алюминий), средней активности (до водорода), неактивные.
|
|
|


