 |
Строение атомных ядер. Изотопьi.
|
|
|
|
1. Атом состоит из ядра и электронов.
2. Ядро заряжено положительно, а электроны отрицательно.
3. Ядро состоит из протонов и нейтронов.
4. Протон является носителем элементарного положительного заряда, равного по значению (1,6•10-19 Кл), но противоположного по знаку заряду электрона. Нейтрон заряда не имеет. Таким образом, заряд ядра (Z) равен числу протонов.
Z=Np.
5. Число протонов определяет порядковый номер элемента. Общее название протонов и нейтронов — нуклоны.
6. Протоны и нейтроны имеют примерно одинаковые массы (mp=mn=1 а.е.м.). Масса атома определяется суммарным числом протонов и нейтронов, поскольку масса электрона в 2000 раз меньше массы протона. Сумма чисел протонов (Np) и нейтронов (N) определяет массовое число атома (А).
7. Электроны вращаются вокруг ядра. Число электронов равно числу протонов (атом электронейтрален).
Принадлежность атома к какому-либо элементу определяется зарядом его ядра Z, т.е. числом протонов. При этом число нейтронов и, соответственно, массовое число у атомов одного и того же элемента может различаться. Такие атомы называются изотопами.
Изотопами называют атомы с одинаковым зарядом ядра, но имеющие разные массовые числа.
Таким образом, изотопы — это атомы одного элемента, имеющие разную массу.
Каждый изотоп характеризуется двумя величинами: А (проставляется вверху слева от химического знака) и N (проставляется снизу слева от химического знака) и обозначается символом соответствующего элемента. Например: изотоп углерода 126C или словами: «углерод-12» Эта форма записи распространена на
элементарные частицы: электронов, нейтрон 10n, протон 11p, нейтрино 00vi. Изотопы известны для всех химических элементов: кислород имеет изотопы с массовыми числами 16, 17, 18: 168О, 178O, 188O. Изотопы аргона: 3618Ar, 3818Ar, 4018Ar; калия: 3919K, 4019K, 4119K.
|
|
|
Атомная масса элемента равна среднему значению из масс всех его природных изотопов с учетом распространенности их.
Например, средняя атомная масса природного лития, содержащего 92,48% 73Li и 7,52% 63Li, равна 6,94 и т.д.
Атомная масса элементов, приводимых в периодической системе Д. И. Менделеева, есть средние массовые числа природных смесей изотопов.
61 61 61 Периодический закон Менделеева. Периодическая таблица (периоды и группы).
Периодический закон (1869 г.): свойства простых тел, а также свойства и формы соединений элементов находятся в периодической зависимости от величины атомных весов элементов.
До появления сведений о сложном строении атома основной характеристикой элемента служил атомный вес (относительная атомная масса). Развитие теории строения атома привело к установлению того факта, что главной характеристикой атома является положительный заряд ядра.
В современной формулировке периодический закон звучит: свойства химических элементов, а также формулы и свойства образуемых ими соединений находятся в периодической зависимости от величины заряда ядер их атомов.
Физической основой структуры периодической системы элементов служит определённая последовательность формирования электронных конфигураций атомов по мере роста порядкового номера элемента.
В зависимости от того, какой энергетический подуровень заполняется электронами последним, различают 4 типа элементов:
1. S – элементы (последним заполняется S -подуровень внешнего энергетического уровня)
2. p – элементы (последним заполняется p -подуровень внешнего энергетического уровня)
3. d – элементы (последним заполняется d -подуровень предпоследнего энергетического уровня)
4. f – элементы (последним заполняется f -подуровень 3-го снаружи энергетического уровня).
|
|
|
Горизонтально располагаются периоды – последовательный ряд элементов, электронная конфигурация внешнего энергетического уровня которых изменяется от 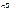 до
до  . Номер периода совпадает со значением главного квантового числа
. Номер периода совпадает со значением главного квантового числа  внешнего энергетического уровня.
внешнего энергетического уровня.
Вертикально располагаются группы – элементы имеющие сходное электронное строение. У элементов главной подгруппы последним заполняется  и
и  подуровни внешнего энергетического уровня, у элементов побочной подгруппы происходит заполнение внутренних
подуровни внешнего энергетического уровня, у элементов побочной подгруппы происходит заполнение внутренних  и
и  подуровней. Одинаковый номер группы, как правило, определяет число электронов, которое может участвовать в образовании химических связей.
подуровней. Одинаковый номер группы, как правило, определяет число электронов, которое может участвовать в образовании химических связей.
|
|
|


