 |
Тема 13. Растворение твердых веществ и газов.
|
|
|
|
Учебные вопросы
1. Растворение и растворы.
2. Понятие растворимости вещества.
3. Концентрация раствора.
4. Поведение веществ в растворах.
Растворение и растворы.
Понятие раствора. Раствор - это гомогенная (однородная) смесь, состоящая из частиц растворённого вещества, растворителя и продуктов их взаимодействия.
Агрегатное состояние растворов. Наиболее распространенное агрегатное состояние растворов – жидкое.
В общем виде любой раствор – это однородная смесь переменного состава из двух или более веществ.
Переменность состава раствора. Соотношение смешиваемых в растворе веществ может непрерывно изменяться в задаваемых пределах. Например, раствор соли можно разбавлять чистой водой или, наоборот, упаривать, но полученные при этом жидкости в любом случае будут называться растворами соли. Именно поэтому любой раствор характеризуется своим переменным составом.
Понятие растворителя. Из двух или нескольких компонентов раствора растворителем является тот, который взят в большем количестве и имеет то же агрегатное состояние, что и раствор в целом. Когда речь идет о водных растворах, воду считают растворителем и в тех случаях, когда ее меньше (96%-ный раствор спирта в воде).
Физическая теория растворов. Основоположники: Вант Гофф и Вильгельм Оствальд. Процесс растворения является результатом диффузии (взаимного перемешивания веществ).
Химическая теория растворов. Д.И. Менделеев доказывал, что растворение является результатом химического взаимодействия растворенного вещества с молекулами воды и что правильнее определять раствор как однородную систему, которая состоит из частиц растворенного вещества, растворителя и продуктов их взаимодействия.
|
|
|
Современная физико-химическая теория растворов. Образование того или иного типа раствора обусловливается интенсивностью:
межмолекулярного,
межатомного,
межионного,
другого вида взаимодействия.
Это те силы, которые определяют возникновение того или иного агрегатного состояния. При этом, т.к. растворы бывают газовыми, жидкими и твёрдыми, их возникновение определяется характером и интенсивностью взаимодействия частиц разных веществ.
Значение теории растворов Д.И. Менделеева. Ученый физико-химическую теорию растворов предсказывал еще в 1906 г., описав в своем учебнике «Основы химии».
Понятие твердого раствора. В твердых растворах частицы одного вещества хаотично распределены среди частиц какого-нибудь другого, но обязательно твердого вещества.
Растворение, как химический процесс. Растворение, как один из основных процессов химической технологии, представляет гетерогенное физико-химическое взаимодействие твердого тела и жидкости, в процессе которого происходит переход твердой фазы в раствор.
Понятия сольватации и гидратации в теории растворов. Растворение сопровождается сольватацией (электростатическим взаимодействием между молекулами растворенного вещества и растворителя), или гидратацией (если растворитель - вода).
Понятия кристаллизации и физического растворения в теории растворов. При растворении образуются более или менее устойчивые соединения растворенных частиц с молекулами растворителя. В случае, если возможна обратная кристаллизация растворившегося вещества из раствора, такое растворение называется физическим растворением.
Понятие химического растворения. Химическим является растворение, при котором растворитель или содержащийся в нем активный реагент таким образом взаимодействуют с растворяемым веществом, что в результате выделить растворившееся вещество из полученного раствора кристаллизацией невозможно.
|
|
|
Диффузия. В процессе растворения молекулы вещества, перешедшие из кристалла в раствор, передвигаются по всему объему раствора вместе с молекулами растворителя благодаря тепловому движению (диффузии).
Химические характеристики насыщенного раствора. Раствор, в котором данное вещество при данной температуре уже больше не растворяется, называется насыщенным. Насыщенным называется такой раствор, который находится в динамическом равновесии с избытком растворенного вещества.
Понятие растворимости вещества.
Определение растворимости в химии. Растворимостью называется способность вещества растворяться в том или ином растворителе.
Мера растворимости. Мерой растворимости вещества при данных условиях является его содержание в насыщенном растворе.
Зависимость растворимости от температуры. Растворимость большинства (но не всех!) твердых веществ с увеличением температуры увеличивается, а растворимость газов – уменьшается. Это связано с тем, что молекулы газов при тепловом движении способны покидать раствор гораздо легче, чем молекулы твердых веществ.
Понятие «кривых растворимости вещества». Значения растворимости, полученные опытным путем, и нанесенные на оси координат, дают «кривые растворимости различных веществ».
Понятие пересыщенного раствора. При охлаждении насыщенного раствора образуется пересыщенный раствор, из которого кристаллы начинают самопроизвольно выпадать (или после добавления кристаллика чистого вещества, который служит центром дальнейшей кристаллизации).
Перекристаллизация раствора, как метод его очистки. Путем фильтрации чистые кристаллы вещества отделяют от охлажденного, загрязненного примесями раствора. Этот способ очистки называется перекристаллизацией. Так очищают многие лекарственные препараты.
Понятие кристаллогидратов. Молекулы воды из гидратной оболочки иногда могут вступать в химическую реакцию с растворенным веществом, образуя новое прочное химическое соединение с постоянным составом, которые можно выделить из раствора, осторожно упаривая воду.Эти соединения называются кристаллогидратами.
|
|
|
Выпаривание растворов как физико-химический процесс. При выпаривании можно вернуть растворенное вещество в первоначальное состояние. Но при выпаривании растворов происходит разрушение гидратов (реакция разложения) и вновь образуется кристаллическое вещество. Таким образом, и растворение вещества и выпаривание раствора имеют признаки химических реакций.
Концентрация раствора.
Массовая доля вещества в растворе. Массовая доля растворенного вещества – это отношение массы растворенного вещества m1 к общей массе раствора m, выраженное в процентах.
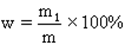
Понятие концентрации и концентрированного раствора (концентрата). Концентрация – это относительное количество растворенного вещества в растворе.
Понятие процентной концентрацией раствора. Массовая доля растворенного вещества называют процентной концентрацией раствора.
Понятие молярной (мольной) концентрации. Помимо процентной концентрации, используется молярная концентрация. Молярная концентрация С – это отношение количества растворенного вещества v (в молях) к объему раствора V в литрах.
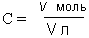
|
|
|


