 |
Устойчивость дисперсных систем
|
|
|
|
Агрегативная устойчивость – это способность частиц сохранять свою дисперсность (прерывистость), т. е. противостоять слипанию. Агрегативная устойчивость обусловлена наличием одноименного электрического заряда частиц дисперсной фазы, вызывающего их взаимное отталкивание. В случае потери агрегативной устойчивости происходит процесс коагуляции. Коагуляция– сцепление частиц дисперсной фазы – сопровождается частичным насыщением поверхностных сил в зоне контакта частиц при их сближении и снижением вследствие этого поверхностной энергии. Для увеличения агрегативной устойчивости в дисперсную систему вводят поверхностно-активные вещества.
Кинетическая устойчивостьпредполагает способность дисперсных систем сохранять равномерное распределение частиц дисперсной фазы в дисперсионной среде. Иначе – это способность противостоять силам земного притяжения. Обусловлена кинетическая устойчивость тепловым (броуновским) движением частиц дисперсной фазы. Для ее увеличения необходимо уменьшить размеры частиц дисперсной фазы или увеличить вязкость среды.
Потеря агрегативной устойчивости всегда приводит к потере кинетической устойчивости – к выпадению осадка или седиментации.
Средне- и грубодисперсные системы устойчивы агрегативно, но не устойчивы кинетически. Тонкодисперсные коллоиды устойчивы и агрегативно и кинетически но в узком интервале параметров температуры и концентрации.
Применение ПАВ и электролитов позволяет эффективно управлять процессами возникновения и разрушения дисперсных систем, регулировать их устойчивость, структурно-механические и другие свойства. ПАВ участвуют в самых разнообразных микрогетерогенных химических, биохимических, физиологических процессах, таких как мицеллярный катализ, явления обмена, проницаемость мембран и т. д. Управление устойчивостью всевозможных дисперсных систем лежит в основе многих технологических процессов.
|
|
|
Коллоидные растворы
Коллоидное состояние получило свое название от греческого слова «колла» (клей). Коллоиды относятся к числу дисперсных систем, характеризующихся высокой степенью раздробленности одного компонента в другом. Линейные размеры частиц дисперсной фазы коллоидной системы лежат в пределах от 1 до 500 нм. Такая дисперсность называется коллоидной. Как дисперсионная среда, так и дисперсная фаза коллоидных систем могут находиться в различных агрегатных состояниях. Коллоидные системы, дисперсионная среда которых жидкость, называются коллоидными растворами или золями.
Коллоидные растворы по внешнему виду напоминают истинные растворы (они прозрачны). Однако при рассмотрении пути светового луча, проходящего через совершенно прозрачный коллоидный раствор, сбоку на темном фоне, он становится видимым. Этот оптический эффект называется конусом Тиндаля.
Причиной рассеяния света является оптическая неоднородность коллоидных систем, т. е. разные оптические свойства дисперсной фазы и дисперсионной среды. Из этих свойств, прежде всего, следует указать показатель преломления, значение которого для дисперсной фазы и дисперсионной среды различны. Вследствие этого луч света, проходя через дисперсионную среду и попадая на частицу дисперсной фазы, обязательно изменяет свое направление, причем тем резче, чем больше показатель преломления дисперсной фазы отличается от показателя преломления дисперсионной среды (рисунок 5).
а)
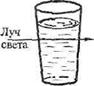
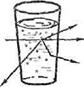
а) – истинный раствор (наблюдатель не видит света);
б) – коллоидный раствор (наблюдатель видит свет).
Рисунок 5 – Эффект светорассеяния при прохождении луча света через коллоидный раствор
|
|
|


