 |
Кинетика процесса деаэрации
|
|
|
|
При отсутствии равновесия между фазами происходит переход вещества из одной фазы в другую, то есть идет процесс массопередачи. Массопередача есть результирующий процесс, включающий процессы переноса вещества в пределах каждой фазы (массоотдача) и перенос вещества через границу раздела фаз (по аналогии с процессами теплопередачи).
Перенос вещества в пределах фазы может происходить за счет молекулярной, конвективной и турбулентной диффузии. Преобладание того или иного типа диффузии определяется гидродинамическими условиями протекания процесса [ 39 ].
Процесс молекулярной диффузии описывает закон Фика [ 39 ], который устанавливает связь между количеством WА компонента А, переносимого в направлении z через поверхность F за единицу времени:
 , (2.34)
, (2.34)
где DА – коэффициент молекулярной диффузии, dCA/dz – градиент концентрации компонента А в направлении z.
При наличии конвективного переноса массы выражение для WА принимает вид [ 39 ]:
 , (2.35)
, (2.35)
где w – скорость перемещения массы.
Для случая турбулентной диффузии можно получить уравнение для WА в виде [ 39 ]:
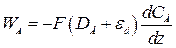 , (2.36)
, (2.36)
где εd – коэффициент турбулентной диффузии.
Иногда сумму (DА + εd) обозначают как Dэф и называют эффективным коэффициентом диффузии [ 39 ].
В многочисленных публикациях результатов исследований в области массопередачи [ 39–42, 44–50 ], предложен ряд моделей этого процесса, различающихся перечнями принятых допущений и, соответственно, адекватностью в каждом конкретном случае. Так, наиболее упрощенная гидродинамическая модель, основанная на пленочной (двухпленочной) теории [ 39, 41 ], построена исходя из следующих допущений: условия в пределах каждой из контактирующих фаз – постоянны (фазы изотропны); фазы разделены некоторой неподвижной пленкой (толщиной δ) (или двумя такими пленками – по одной в каждой фазе), процессы переноса через которую осуществляются путем молекулярной диффузии. Математическое развитие пленочной теории для случая массопередачи в условиях абсорбции (десорбции) приводит в выводу, что коэффициент физической абсорбции kL0 должен быть прямо пропорционален коэффициенту молекулярной диффузии Dж [ 41 ]:
|
|
|
kL0 = Dж / δ. (2.37)
Такой вывод противоречит экспериментальным данным [ 2–4, 39–50 ], которые указывают на другую пропорциональность между этими параметрами: kL0 должно быть пропорционально (Dж)0,5. Если считать, однако, что δ зависима от Dж, модель может считаться в ряде случаев приемлемой [ 39 ].
Лучшие результаты получаются при использовании моделей, построенных на базе теории проникновения (пенетрационной теории) [ 39, 41 ]. Согласно теории проникновения поверхность раздела фаз между газом и жидкостью состоит из небольших конечных элементов жидкости, которые непрерывно подводятся к поверхности из объема жидкой фазы и, наоборот, отводятся от неё за счет движения самой жидкости. Хигби [ 39, 41 ] принял допущение, что все элементы находятся на поверхности одинаковое время. С учетом этого, например, для случая барботажа газовых пузырей через слой жидкости выводится выражение для коэффициента физической абсорбции в виде:
 , (2.38)
, (2.38)
где t* – время нахождения элементов жидкости на границе раздела фаз.
Такой результат удовлетворительно подтверждается экспериментальными данными [ 41 ]; при этом t* соответствует среднему времени всплытия газовых пузырей.
Развитием модели Хигби является модель Данквертса [ 39, 41 ], который отказался от предположения о равенстве промежутков времени нахождения всех элементов жидкости на поверхности. При этом введена функция распределения возраста элементов, вид которой, в принципе, может быть различным, что позволяет «настраивать» модель под конкретные условия.
|
|
|
Модели Хигби и Данквертса могут быть приведены к виду [ 41 ]:
 , (2.39)
, (2.39)
где tD – эквивалентное время диффузии.
По физическому смыслу эквивалентное время диффузии есть время, достаточное для полного перемешивания. Его значение определяется гидродинамическими условиями протекания процесса.
Обе рассмотренные модели, основанные на теории проникновения, оперируют коэффициентом молекулярной диффузии. Вместе с тем Кишеневский [ 39 ] показал целесообразность использования в модели Хигби эффективного коэффициента диффузии, то есть Dэф вместо Dж.
Необходимо отметить, что рассмотренные физические модели массопереноса приводят к приемлемым результатам в тех случаях, когда удается определить площадь поверхности контакта фаз. Иначе, ввиду неопределенности этого параметра необходимо использовать различные статистические уравнения или критериальные зависимости, параметры идентификации которых определяются при обработке экспериментальных данных [ 1–4, 39–67 ].
Так или иначе, для применения указанных моделей к каждому конкретному случаю необходимо знание значений коэффициентов диффузии. К категории справочных данных могут быть отнесены коэффициенты молекулярной диффузии (как характеристика системы); коэффициент турбулентной диффузии зависим от гидродинамической ситуации и обычно специально не вычисляется.
Значения коэффициентов молекулярной диффузии в жидкостях обычно на четыре порядка меньше, чем в газах, в связи с чем их экспериментальное определение затруднительно. Имеющиеся данные о полученных экспериментальным путем значениях коэффициентов диффузии в жидкостях редко выходят за границы температурного диапазона 0 – 40 оС [ 68 ]. Для расчета процессов атмосферной деаэрации воды необходимо располагать значениями коэффициентов молекулярной диффузии кислорода в воде при температурах порядка 100 оС. Существуют зависимости, позволяющие экстраполировать коэффициенты молекулярной диффузии в область более высоких температур, например, формулы Шейбеля, Отмера и Тейкара, Арнольда и др. [ 39, 68 ]. Для примера в табл. 2.3 приведены числовые значения коэффициентов молекулярной диффузии в воде кислорода и диоксида углерода [ 9, 39, 40, 68–70 ].
|
|
|
Таблица 2.3. Значения коэффициентов молекулярной диффузии в воде кислорода (DО2) и диоксида углерода (DСО2) при абсолютном давлении 0,1 МПа в зависимости от температуры раствора (t)
| t, оС | 21,7 | 29,6 | ||||
| DО2 ·105, см2/с | 1,86 | – | 1,8 | 1,875 | от 2,4 до 2,5 | 3,19 |
| DСО2 ·105, см2/с | – | 1,458 | 1,77 | – | от 1,96 до 2,0 | – |
Термическая деаэрация есть сочетание протекающих параллельно в двухфазной среде процессов тепло- и массообмена в системе «вода – водяной пар» и процессов массообмена в системе «газ, содержащийся в жидкой фазе – газ, присутствующий в паровой фазе» (процессы газообмена). Поскольку относительное содержание газов в технологических водах энергетических установок мало, процессы газообмена не оказывают ощутимого влияния на теплофизические свойства воды и водяного пара и, следовательно, практически не влияют на процессы тепломассообмена в системе «вода – водяной пар». Напротив, растворимость газов в воде, интенсивность протекания реакций, сопровождающих хемосорбцию-десорбцию химически связанных газов существенно зависят от температуры среды. Интенсивность собственно процессов диффузии (молекулярной, конвективной, турбулентной) газов также определяется гидродинамическими условиями, складывающимися в том или ином элементе деаэратора, а значит интенсивностью процессов тепломассообмена в системе «вода – водяной пар».
В практике расчета процессов термической деаэрации в качестве градиента концентрации газа в воде dCA/dz принято использовать разность текущей концентрации газа и равновесной концентрации этого газа в данных условиях. Иными словами, движущей силой процесса переноса газов из одной фазы в другую является степень отклонения системы от состояния равновесия.
В термических деаэраторах равновесные условия, как правило, не достигаются из-за недостаточности времени контакта фаз. Состояние, в той или иной степени близкое к равновесному, достигается, в основном, благодаря образованию и удалению пузырьков газа и диффузии газов через поверхность контакта фаз. Образование газовых пузырьков протекает наиболее интенсивно и при рациональной конструкции деаэратора этим путем можно удалить из воды 90-95 % растворенных в ней газов. Образование пузырьков газа происходит в тот момент, когда сумма парциальных давлений всех растворённых газов и водяного пара достигает или превосходит давление внутри жидкости. Вместе с тем вследствие ряда факторов в воде остается некоторое количество растворенного газа, которое должно быть удалено за счет диффузии. Необходимость глубокого удаления из жидкости этого остаточного количества растворенного газа является весьма трудной задачей и предъявляет большие требования к деаэраторной установке, а эффект дегазации при этом является решающим критерием для оценки работоспособности деаэратора [ 2–4 ].
|
|
|
Применительно к процессам десорбции химически-связанных газов, например, диоксида углерода, необходимо учитывать не только время, предоставленное процессу десорбции сложившимися в деаэраторе гидродинамическими условиями (время диффузии), но и время реакции (время, необходимое для завершения комплекса химических реакций с участием рассматриваемого газа). Для каждого отдельного случая необходимо определять достаточность времени контакта фаз в элементе деаэратора для протекания всего комплекса химических реакций и на основе этого расчета выявлять наиболее «медленную» стадию процесса, которая в итоге и определяет интенсивность хемосорбции-десорбции в целом.
|
|
|


