|
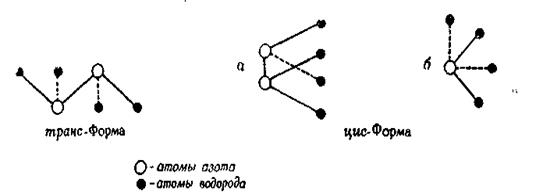
Строение молекулы и дипольный момент
|
|
|
|
Большой дипольный момент гидразина (1,83—1,90 дебая) связан с некоторыми очень интересными вопросами, касающимися его строения. В принципе возможно несколько различных структур, отличающихся друг от друга положением атомов водорода по отношению к оси азот — азот в молекуле гидразина. Гидразин можно рассматривать как производное аммиака, в котором вместо одного из атомов водорода находится второй атом азота, расположенный в той же плоскости, что и три атома водорода молекулы аммиака. При этом получается симметричная структура, в которой противоположные моменты связей N—Н должны компенсировать друг друга и давать суммарный дипольный момент, равный нулю. Такая симметричная структура является маловероятной, о чем свидетельствуют как высокий дипольный момент гидразина, так и данные, полученные при изучении этого вопроса, в особенности результаты исследования инфракрасного спектра гидразина. Сначала предполагали, что имеется возможность свободного вращения вокруг оси азот—азот, благодаря чему может существовать любая из возможных форм; считалось также, что большой дипольный момент является результатом равновесия, которое устанавливается между этими предельными структурами. Более поздние исследования N-замещенных гидразина, особенно фенилгидразина и других арилзамещенных, показывают, что эти вещества также характеризуются относительно большими дипольными моментами. Эти дополнительные исследования заставляют предположить, что вращение вокруг оси азот — азот ограничено, если оно вообще возможно. Поэтому симметричная транс-форма маловероятна. Если вращение ограничено, то большой дипольный момент может быть объяснен только конфигурацией, соответствующей изображенной на рис. 2 цис-форме.
|
|
|
Если связи N—Н расположены в пространстве так, как это указано на рисунке, то очевидно, что цис-форма гидразина должна иметь два стереоизомера. Эти выводы подтверждают предположение, впервые высказанное Пенни и Сазерлендом, которые вычислили, что дипольный момент структуры, соответствующей несимметричной цис-форме, равен 1,70 дебая; они предположили также, что валентные углы N—N—Н и Н—N—Н составляют приблизительно 110°С. Электронографические исследования паров гидразина показывают, что углы Н—N—Н и Н—N—N приблизительно составляют 108±10°С. Межатомные расстояния равны:
rN-H=1,04 ± 0,06Е и rN-N = 1,47 ± 0,02 Е. Эти значения валентных углов и межатомных расстояний очень близки к соответствующим значениям для молекулы аммиака. Возможно также, что гидразин существует в таутомерной аминоимидной форме, Н3N → NН, и что протон при этом способен мигрировать, образуя молекулу с указанной структурой.
|
|
Рис. 1. Структуры гидразина.
а—в перспективе; б— ось N-N перпендикулярна к плоскости рисунка.
Возросший интерес к гидразину и его производным обусловлен отчасти использованием некоторых гидразинов в военной технике [и космических исследованиях] в качестве ракетных топлив, а также разнообразным применением производных гидразина в медицине и сельском хозяйстве.
Гидразин—весьма реакционноспособное соединение: он окисляется на воздухе, окисление протекает через промежуточное образование диимида, давая азот. Как уже отмечалось, превращение гидразина в элементарный азот сопровождается выделением большого количества энергии. Поэтому, а также в результате легкости его получения по методу Рашига гидразин нашел широкое применение в. качестве ракетного топлива. Если использовать его в сочетании с азотной кислотой как окисляющим агентом, то газообразные продукты окисления гидразина (азот, окислы азота) развивают очень эффективную тягу. Некоторыми недостатками гидразина как топлива являются высокая температура плавления, малая стабильность на воздухе и коррозионная активность, затрудняющие хранение и работу с ним.
|
|
|
Из трехфтористого азота при повышенной температуре был получен тетрафторгидразин, но, как и ожидалось, наличие сильно электроотрицательных атомов фтора делает это соединение еще менее стабильным, чем гидразин. Метилгидразин, превосходя гидразин по некоторым физическим показателям, по-видимому, вытеснит последний как жидкое ракетное топливо.
Производные гидразина можно разделить на моно-, ди-, три- и тетразамещенные:
RNH-NH2 RNH-NHR 


1 2а 2б 3 4
Дизамещенные гидразины 2 следует подразделить на два класса и рассматривать их отдельно, так как первичная аминная функция в 1,1-дизамещенных гидразинах 2б обусловливает свойства, которыми не обладают 1,2-дизамеш.енные гидразины 2а.
Был описан удобный метод аминирования вторичных и третичных аминов до гидразинов и гидразиниевых солей О-гидроксиламинсульфокислотой:
NH 2 O S О3H + R 2 NH —>- R 2 N—NH 2 + H 2S О4
Этот реагент является удобным источником частиц NH2 и может найти в будущем более широкое применение.
Сильно нуклеофильный характер гидразина и алкилгидразинов проявляется в различных реакциях. Так, ряд активированных ароматических галогенпроизводных можно ввести в реакцию с гидразином, в результате образуются арилгидразины:

Аналогично гидразин атакует олефины, обедненные электронами, например б,в-ненасыщенные сложные эфиры, с последующей циклизацией в пиразолидоны:
 |
 ArCH = CHCOOR + H2N—NH2 → ArCHCH2COOR →
ArCH = CHCOOR + H2N—NH2 → ArCHCH2COOR →
NH — NH2
Интересный вариант приведенной выше реакции был найден при взаимодействии 1, 1-диалкилгидразинов и акролеина. Здесь начальная атака более нуклеофильного трехзамещен-пого атома азота с последующей циклизацией приводит к четвертичной пиразолиниевой соли. Мягкое разложение этой соли щелочью разрывает связь N—N, давая в-аминонитрил:
 |
R2N – NH2 + CH2=CHCHO R2NCH2CH2CN
Первой стадией этой реакции является образование диметилгидразона, циклизующегося в кислой среде. Последняя стадия представляет собой один из частных случаев аминонитрильной перегруппировки четвертичных альдогидразониевых структур под действием щелочей.
|
|
|
МОНОЗАМЕЩЕННЫЕ ГИДРАЗИНЫ
Монозамещенные гидразины 1 по химическим свойствам подобны незамещенному родоначальнику и также легко окисляются многими окислителями, включая воздух. Другие окислители легко реагируют с монозамещенными гидразинами; так, бром окисляет фенилгидразин до бромбензола и азота. Алкилирование монозамещенных гидразинов дает 1, 1-диалкил- и более замещенные гидразины. Фенилгидразин алкилируется по первому замещенному атому азота (1), хотя многие утверждали, что он метилируется йодистым метилом по второму атому азота, образуя 1-фенил-2-метилгидразин.
Следует отметить, что из возможных переходных состояний при алкилировании замещенного гидразина возникающий положительный заряд будет больше стабилизирован при замещенном атоме азота; промежуточное соединение уравнения (1) стабилизировано индуктивным эффектом ароматического кольца, что невозможно в альтернативном 1,2-ди-замещенном промежуточном соединении:
 |
(1)
(2)
Монозамещенные гидразины реагируют с различными карбонильными соединениями. В реакции с альдегидами или кетонами продуктами будут гидразоны и вода. С карбоновыми кислотами, хлорангидридами или сложными эфирами образуются 1-замещенные гидразиды.
Из многих гидразинов типа 1 фенилгидразин нашел применение в химии углеводов (например, образование озазонов), а 2,4-динитрофенилгидразин широко используется при идентификации альдегидов и кетонов в виде твердых динитрофенилгидразонов.
ДИЗАМЕЩЕННЫЕ ГИДРАЗИНЫ
1,2-Дизамещенные гидразины
|
|
|
Отщепление азота при окислении 1,2-дизамещенных гидразинов 2а включает две стадии, и промежуточное соединение часто можно выделить, особенно когда R или R' (или же оба) — ароматические группы:
RNH—NHR' → RN = NR' → R—R' + N2
В этой реакции были использованы различные окислители, включая окись ртути, хлорное железо и перманганат калия. Некоторые 1,2-дизамещенные гидразины, особенно те, в которых гидразинный фрагмент заключен в циклическую структуру, окисляются до соответствующих азосоединений при стоянии на воздухе. Многие из промежуточных азосоединений были выделены и затем разложены при нагревании или на свету до азота и углеводородов. Природа заместителей R и R' в этих азосоединениях определяет их устойчивость. Если R и R'— простые алкильные группы, для выделения азота требуется повышенная температура; некоторые циклические и бензилзамещенные азосоединения разлагаются при комнатной температуре; ароматические же азосоединения вполне устойчивы, 1,2-Диалкилгидразины реагируют с алифатическими альдегидами, давая 1,3, 4-оксадиазолидины, которые можно превратить в 1,2,4-триазолидипы реакцией с первичным амином:

Соединения с двумя атомами азота, связанными через метиленовую группу, можно рассматривать как 1,2-дизамещенные гидразины. Было показано, что трехчленные циклические гидразины можно легко приготовить общим методом из хлорамина и азометинов:

Диазиридины растворяются в органических растворителях, медленно реагируют с кислотой, устойчивы к щелочи и нагреванию (до 100° С). Альтернативным синтетическим методом может служить присоединение реактивов Гриньяра к диазиринам (трехчленным циклическим азосоединениям) с образованием N-алкилдиазиридинов, последние могут дальше гидролизоваться в алкилгидразины:
 |
B аналогичной реакции 2-метилдиазирина с этилмагнийбромидом получается 1-этил-2-метилдиазиридин, который может также быть приготовлен из хлорамина и этилиденэтиламина:

Известны многие другие примеры циклических гидразинов, в которых оба атома азота включены в цикл. О синтезе четырехчленных циклических гидразинов сведений мало, известна, например, реакция активированных олефинов с диэтил-азокарбоксилатом:

Под влиянием кислот ароматические 1,2-дизамещенные гидразины подвергаются перегруппировкам типа бензидиновой. Механизм этих реакций был предметом интенсивных исследований, и, по-видимому, он включает образование «протонного сандвича»:
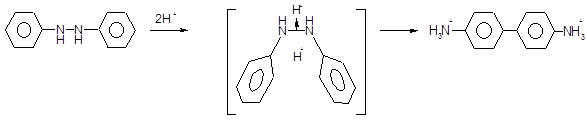
Изучалось поведение 1,2-диалкилгидразинов в условиях реакции Манниха. Реакция гидрохлоридов 1, 2-дизамещенных гидразинов с формальдегидом и ацетофеноном приводит к 3-фенил-1,2-диалкил-Д3-пиразолинам:
|
|
|
 С 6Н 5 С О С Н 3 + (C H 2O)x + RHN—NHR • НС1 → [C6H5C OCH2 C H2 NR-NHR]→
С 6Н 5 С О С Н 3 + (C H 2O)x + RHN—NHR • НС1 → [C6H5C OCH2 C H2 NR-NHR]→
1,1-Дизамещенные гидразины
Благодаря первичной аминной функции 1, 1-дизамещенные гидразины 2б способны к некоторым реакциям, невозможным у изомерных 1,2-дизамещенных гидразинов. Окисление 1,1-дизамещенных гидразинов может привести к двум продуктам и, вероятно, протекает через промежуточный N-нитрен:

Сочетание двух частиц нитрена или, что более вероятно, реакция нитрена с непрореагировавшим гидразином (по типу а) дает тетразены. Наблюдалось также разложение нитрена с образованием азота и углеводорода (по типу б). Продукты окисления зависят от природы заместителей R и R', однако обычно окисление дает тетразен. В некоторых случаях окисление 1,1-дизамещенных гидразинов приводит непосредственно к выделению азота и образованию углеводородо. Этот последний путь, называемый «аномальным окислением», требует, чтобы замещающие группы могли стабилизировать промежуточные фрагменты, образующие новую углерод-углеродную связь. Этими свойствами обладают такие группы, как бензнльная и цианометиленовая:
 C6H5CH2NCH2C6H5 + HgO → С6Н5СН2СН2С6Н5 + N2 + Hg + Н2О
C6H5CH2NCH2C6H5 + HgO → С6Н5СН2СН2С6Н5 + N2 + Hg + Н2О
NH2
Такие аномальные реакции окисления легко происходят в гетерогенных окисляющих системах (например, спирт — окись ртути) с большой поверхностью окислителя, увеличивающей скорость выделения азота. Аналогичные результаты были получены с гетерогенными системами и в других реакциях с выделением азота. Гомогенная среда часто благоприятствует образованию тетразена. Например, в методе получения тетрабензилтетразена из дибензилгидразина используется спиртовой раствор ацетата ртути.
Твердая поверхность, по-видимому, способствует снижению энергии активации выделения азота и, вероятно, помогает изолировать промежуточные частицы N-нитрена друг от друга, препятствуя образованию тетразена. Если в 1, 1-диза-мещенном гидразине присутствуют метальные, этильные, циклогексильные или подобные алкильпые группы, то неспособность этих групп стабилизировать промежуточные углеродные фрагменты (ионы или свободные радикалы — еще не выяснено) подавляет разрыв связей углерод—азот. В этих случаях даже в гетерогенной среде образование азота невыгодно энергетически, и вместо этого получается тетразен.
Такие соединения, как 1-бензил-1-бутилгидразин, окисляются окисью ртути в хлористом метилене, давая с низким выходом амилбензол; однако в этанольном растворе та же реакция приводит к соответствующему тетразену. Другими примерами аномального окисления могут служить:
окисление N-аминоизоиндолина до бензоциклобутена и 1, 2-диметилен-З, 5-циклогексадиена

окисление N-амино-1, 3-дифенилизоиндолина в 1,2-дифе-нилбензоциклобутен

(транс) (транс 81%)
Реакцией, аналогичной аномальному окислению гидразинов 2б, является щелочное разложение сульфонилгидразинов. Эти реакции, по-видимому, протекают через нитрен и продукты часто идентичны продуктам окисления соответствующих гидразинов:


Здесь, как и в реакциях аномального окисления, для образования азота и углеводорода желательны стабилизирующие заместители (например, бензил). Аналогично, обработка некоторых нитрозаминов гидросульфитом натрия в щелочной среде дает азот и углеводороды. Так как продукты реакции идентичны получаемым при окислении соответствующего гидразина окисью ртути, то промежуточное образование нитрена Предполагалось и для этой реакции:
|
|
|