 |
Убиквитин-зависимая система протеолиза в регулируемой деградации белков
|
|
|
|
Убиквитин-зависимая система протеолиза проводит поиск потенциальной мишени для протеолитической деградации среди огромного числа внутриклеточных белков. Все белки несут в себе специфические сигналы деградации по аналогии с сигнальными последовательностями, которые направляют вновь синтезируемые белки к определенным органеллам или микрокомпартментам клетки. Однако сигналы протеолитической деградации должны быть более сложными и разнообразными, так как с их помощью не только маркируются белки, удаляемые с помощью протеолиза, но и определяется время удаления, а также скорость их протеолитического расщепления. Для распознавания и декодирования таких сигналов в клетках эукариот имеется убиквитин-конъюгирующая система.
Как в ядре, так и в цитоплазме эта система отделена пространственно и функционально от протеолитических ферментов, организованных в протеасомы. Распознанные данной системой белки-субстраты маркируются путем ковалентного присоединения к ним молекул небольшого стабильного 76-звенного белка – убиквитина. В результате убиквитин соединяется C-концом с боковыми остатками лизина в субстрате. Наличие такой метки в белке, по-видимому, является первичным сигналом сортировки, направляющей образовавшиеся конъюгаты к протеасомам. В большинстве случаев к субстрату присоединяется несколько молекул убиквитина, которые организованы в виде бусинок на нитке. Молекулы белков, содержащие убиквитин, по-видимому, являются для протеасом предпочтительными субстратами. Конъюгацию убиквитина с субстратом можно представить следующим образом (рис. I.41). Вначале убиквитин-активирующий фермент (E1) связывает убиквитин, гидролизует ATP и образует тиоэфирную связь между AMP и убиквитином с последующим переносом молекулы убиквитина на один из своих остатков Cys. Молекула активированного убиквитина далее соединяется с одним из ферментов семейства убиквитин-конъюгирующих ферментов (E2) и часто вслед за этим с убиквитин-лигазой (E3). Процесс конъюгации убиквитина с субстратом может катализироваться как самим E2, так и E2 совместно с E3. Белки E2 и E3 в клетках существуют в виде больших семейств, члены которых различаются по свойствам и внутриклеточной локализации. Мутации в генах семейства E2 у дрожжей показывают, что в ДНК-репарацию, прохождение клеточного цикла, биогенез пероксисом, а также в обеспечение устойчивости к тепловому шоку и ионам кадмия вовлечены разнообразные ферменты. Некоторые из ферментов E2 способны образовывать между собой гетеродимеры, которые, вероятно, в сочетании с различными белками E3 обеспечивают весь большой репертуар субстратных специфичностей убиквитин-конъюгирующих комплексов.
|
|
|
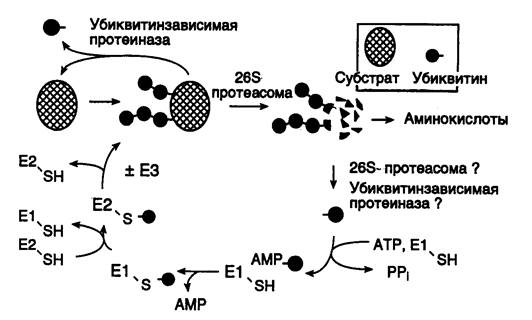
Рис. I.41. Этапы функционирования убиквитинзависимой системы протеолиза
Е1–Е3 – ферменты, активирующие убиквитин с функционально-активными SH-группами, PPi – неорганический пирофосфат
Структура и функционирование протеасомы. Белки, меченные цепями убиквитина, после взаимодействия с протеасомами расщепляются до коротких пептидов и свободных аминокислот в результате ATP-зависимой реакции. У эукариот протеасомы присутствуют в цитозоле и ядрах, но не в других клеточных органеллах. Протеасомы выделяют в виде индивидуальных частиц с коэффициентами седиментации 20S и 26S. 20S частица является коровой частью 26S частицы, которая обладает протеолитической активностью. Коровая частица представляет собой белковый комплекс в виде цилиндра, через центральный канал которого "протягивается" молекула гидролизуемого белка. В настоящее время в качестве модельного объекта часто используют протеасомы архебактерии Thermoplasma, которые были закристаллизованы и исследованы с помощью рентгеноструктурного анализа.
|
|
|
Установлено, что протеасома Thermoplasma построена из двух (a и b) субъединиц. Кольцевые структуры на обоих концах цилиндра протеасомы составлены из a-, а центральная часть – из b-субъединиц в отношении a7b7b7a7 (рис. I.42). Протеолитическая активность присуща b-субъединицам, причем их активные центры направлены внутрь полости цилиндра протеасомы. Кроме того, кольца a-субъединицы по обоим концам молекулы образуют узкие отверстия диаметром ~13 Å, через которые может пройти только развернутая цепь полипептида. Это механистически объясняет, каким образом протеасома избирательно расщепляет полипептидные цепи белков, меченные убиквитином. Прежде чем войти в контакт с активными центрами протеиназ, полипептидная цепь деградируемого белка должна быть развернута. Пептиды и аминокислоты, образующиеся в центральной части цилиндра протеасомы, покидают ее через переднее или заднее отверстия, сформированные a-субъединицами. Протеасомы Thermoplasma лишены специфичности в отношении деградируемых белков, и их функционирование требует наличия в N-концевой части b-полипептидов остатка Thr. Интересно, что остатки Thr эукариотических b-субъединиц являются мишенью для антибиотика лактацистина из Streptomyces, который ковалентно связывается с этими остатками, необратимо инактивируя протеасомы.
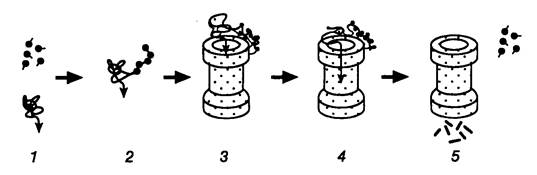
Рис. I.42. Гипотетическая схема функционирования протеасомы убиквитинзависимой системы протеолиза
Молекулы убиквитина присоединяются к деградируемой полипептидной цепи (1,2) и конъюгат далее взаимодействует с 26S протеасомой (3). Узкий цилиндр изображает кόровую 20S субчастицу протеасомы, обладающую протеолитической активностью. Полипептидная цепь, разворачиваясь, входит в центральную полость 20S субчастицы, где последовательно подвергается протеолизу (4, 5). При этом цепи убиквитина отделяются от деградируемого белка
Локализация активных центров b-субъединиц внутри протеасомы затрудняет неконтролируемую деградацию окружающих белков. Отдельные субъединицы до включения их в состав зрелых протеасом синтезируются в виде неактивных предшественников, что предотвращает их преждевременное протеолитическое действие и является общим принципом биосинтеза протеолитических ферментов. Подобно тому как ферменты лизосом активируются только после их перемещения в соответствующий компартмент клетки, процессинг b-предшественников сопряжен с их включением в состав протеасом. Сборка протеасом начинается с образования гептамерных a-субчастиц (a7), которые стимулируют аутокаталитическое удаление пропоследовательности предшественника b-субъединиц, что приводит к их упорядоченной самосборке с образованием гептамерных b-субчастиц (b7), состыкованных с a-субчастицами. Две предварительно собранные половины протеасомы (a7b7) далее ассоциируют друг с другом с образованием активных 20S протеасом. Очищенные 20S протеасомы эффективно расщепляют небольшие пептиды, но не способны гидролизовать интактные белки. Распознавание конъюгатов убиквитина и разворачивание белковой глобулы происходят с участием ~16 белков, ассоциированных с 20S протеасомой и образующих 26S комплекс. Эти белки способны объединяться в отдельные комплексы, получившие название 19S-кэп-структур. 19S-комплексы ассоциируют друг с другом в присутствии ATP и с 20S протеасомами in vitro, присоединяясь к концам цилиндра.
|
|
|
Протеасомы обеспечивают не только полную деградацию полипептидов, но и участвуют в процессинге предшественников с образованием зрелых, активных белков. В частности, процессинг субъединицы p50 транскрипционного фактора NF-kB животных, сопровождающийся отщеплением и деградацией С-концевой части полипептида, происходит с помощью 26S протеасом.
Процессинг антигенов. В настоящее время сформировалось мнение о том, что протеасомы клеток животных участвуют в процессинге антигенов, представляемых молекулами первого класса главного комплекса гистосовместимости (MHC). Из семи b-субъединиц протеасом человека лишь три обладают протеолитической активностью. Эндогенный антивирусный агент g-интерферон селективно стимулирует синтез неактивных b-субъединиц, одновременно подавляя образование активных. Две из этих стимулируемых субъединиц, названные LMP2 и LMP7, кодируются генами MHC. До конца не ясно, какой биологический смысл имеет замещение почти всех активных субъединиц на неактивные, однако предполагается, что такое явление может иметь отношение к процессингу антигенов, представляемых для распознавания молекулами MHC. Действительно, для мышей с дефектными LMP2 или LMP7 характерно нарушение презентации некоторых антигенов. По-видимому, пептиды, образующиеся в таких реконструированных протеасомах, по размерам или составу аминокислотных последовательностей соответствуют тому стандарту, который требуется для эффективного действия антигенных детерминант во время иммунного ответа.
|
|
|
Сплайсинг белков
Феномен сплайсинга белков, обнаруженный в 1990 г. в группой Т.Стивенса, пошатнул еще один постулат молекулярной биологии, в соответствии с которым последовательности нуклеотидов зрелых мРНК всегда колинеарны аминокислотным последовательностям кодируемых ими полипептидов. Во время сплайсинга белков удаление избыточной генетической информации из макромолекул происходит не на уровне пре-мРНК, как это имеет место во время обычного сплайсинга, а на уровне синтезированного полипептида путем вырезания из его внутренней части короткой аминокислотной последовательности. Именно данный механизм отличает сплайсинг белков от повсеместно распространенного процессинга предшественников полипептидов, который, как известно, сопровождается только протеолитическим расщеплением полипептида-предшественника с образованием более коротких белков без изменения их внутренней первичной структуры.
Открытие сплайсинга белков было сделано при исследовании экспрессии гена VMA1 дрожжей S. cerevisiae, известного также под названием TFP1, который кодирует субъединицу ATPазы вакуолей с молекулярной массой 119 кДа (рис. I.43,а). При исследовании гомологии данного гена с генами других ATPаз микроорганизмов было установлено, что все они кодируют более короткие полипептиды с молекулярными массами ~70 кДа, и их гомология с геном дрожжей распространяется только на концевые последовательности нуклеотидов, резко нарушаясь в центральной части гена. Более того, использование инсерционного мутагенеза (генного нокаута) (см. раздел 9.1.3) для инактивации этого гена приводило к прекращению синтеза в клетках дрожжей полипептида с молекулярной массой 69, а не 119 кДа. Механизм такого явления прояснился после постановки двух контрольных экспериментов. В первом из них введение мутаций со сдвигом рамки считывания в сегмент гена VMA1, который кодировал центральную часть полипептида, отсутствующую в зрелом белке, приводило к прекращению синтеза всего белка рибосомами из-за возникновения новых терминирующих кодонов в этой рамке считывания мРНК. Подобное бы не происходило, если бы центральная часть пре-мРНК гена VMA1 удалялась в результате сплайсинга. Во втором эксперименте исследование экстрактов клеток дрожжей с помощью антител к центральной части полипептида, отсутствующего в зрелой субъединице, обнаружило белковый продукт с предсказанной молекулярной массой 50 кДа. Он присутствовал в соотношении 1:1 к функционально активному полипептиду с молекулярной массой 69 кДа. Это указывало на то, что последовательности РНК центральной части гена транслируются рибосомами и соответствующая часть полипептида-предшественника удаляется посттрансляционно. Дальнейшие исследования данного явления полностью подтвердили предположение о том, что внутренняя аминокислотная последовательность из предшественника с молекулярной массой 119 кДа отщепляется в результате сплайсинга на уровне его полипептидной цепи (см. рис. I.43,а). Внутренняя часть полипептида, удаляемая в результате белкового сплайсинга, получила название интеина, а наружные N- и C-концевые части – экстеинов. Позднее белки, изменяемые посттрансляционно в результате белкового сплайсинга, были обнаружены у многих микроорганизмов (см. рис. I.43,б). Во всех случаях аминокислотные последовательности интеинов фланкированы короткими консервативными последовательностями. На основании особенностей первичной структуры интеинов и экстеинов разработаны алгоритмы поиска белков, подвергаемых сплайсингу посттрансляционно, в соответствующих базах данных. С использованием этого алгоритма, в частности обнаружена последовательность интеина в продукте гена dnaB хлоропластов красной водоросли Porphira porphira.
|
|
|
Для объяснения механизма белкового сплайсинга предложено несколько моделей. Одна из них, разработанная группой Ф. Перлера и включившая в себя многие черты ранних моделей, представлена на рис. I.44. В соответствии с этой моделью белковый сплайсинг является аутокаталитическим процессом и для своего осуществления не требует других кофакторов в дополнение к самому полипептиду-предшественнику. Событием, запускающим белковый сплайсинг, может быть: а) нуклеофильная атака OH-группой консервативного остатка Ser, расположенного в C-концевом сайте сплайсинга, по карбонильной группе пептидной связи, расположенной в N-концевом сайте сплайсинга, или же: б) N–O-сдвиг в N-концевом сайте сплайсинга с последующей атакой OH-группой C-концевого сайта и переэтерификацией. В результате функционирования обоих механизмов образуется разветвленное промежуточное соединение, которое при участии остатка Asn распадается на интеин-сукцинимид и экстеины, связанные друг с другом сложноэфирной связью. Эта связь преобразуется в пептидную в результате N–O-сдвига.

Рис. I.43. Сплайсинг белка гена TFP1 S. cerevisiae (а) и перечень генов, белки которых подвергаются сплайсингу на уровне полипептидных цепей (б)
Стрелки указывают места разрыва полипептидной цепи белка-предшественника TFP1. Консервативные последовательности 10 известных интеинов в окрестностях сайтов сплайсинга изображены с использованием однобуквенного кода
Генетическая мобильность последовательностей интеинов в ДНК является одной из самых больших неожиданностей, обнаруженных после их открытия. Оказалось, что полипептидная цепь интеина обладает эндонуклеазной активностью, которая обеспечивает транспозиции последовательностей интеинов в геноме. Аналогичный процесс, ранее получивший название "хоуминга интронов", описан у интронов группы I. В результате хоуминга происходит однонаправленный перенос копии последовательности ДНК интрона (или интеина) из гена, содержащего эту последовательность, к аллельному гену, не содержащему ее. Данная цепь реакций инициируется эндонуклеазным разрывом обеих цепей ДНК в аллельном безинтеиновом гене, образующемся под действием эндонуклеазы интеина. Далее с использованием последовательности ДНК интеина в качестве донора информации происходит репарация двухцепочечного разрыва, которая сопровождается конверсией гена с включением в его состав последовательности интеина. Это указывает на большое сходство механизмов хоуминга интронов группы I и интеинов.
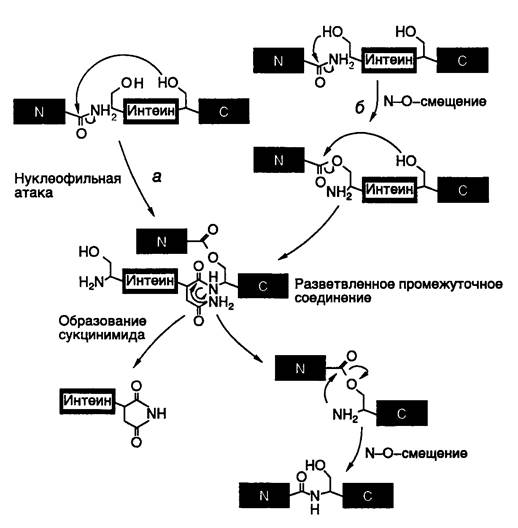
Рис. I.44. Предполагаемый механизм сплайсинга белков
а, б – альтернативные механизмы инициации сплайсинга, N, C – N- и C-концевые экстеины белков-предшественников
Сплайсинг белков является сложной задачей для исследования in vitro. Процесс вырезания последовательности интеина происходит настолько быстро, что не удается обнаружить промежуточные соединения. Проблему удалось решить методами генной инженерии, вставив последовательность ДНК интеина из гена ДНК-полимеразы термофильной бактерии Pyrococcus в одну рамку считывания между геном белка, связывающего мальтозу, и частью гена парамиозина Dirofilaria immitis. Образующийся химерный белок не претерпевал сплайсинга при 12–20°, но при 37–65° сплайсинг индуцировался. Именно с помощью этого подхода удалось обнаружить разветвленные промежуточные соединения, образующиеся при сплайсинге белков. Кроме того, такой подход может стать продуктивным для биотехнологии, так как он позволяет нарабатывать токсические для клетки белки в виде химерных предшественников при низких температурах, которые затем простым повышением температуры быстро превращаются в полезные белковые продукты.
|
|
|


