 |
Общая характеристика альдегидов и кетонов.
|
|
|
|
Карбонильные соединения (оксосоединения) – это соединения, содержащие карбонильную
 группу
группу
Оксосоединения делятся на две группы:
1. Альдегиды – соединения, содержащие альдегидную группу 
Им можно дать и такое определение: «Это соединения, содержащие карбонильную группу, связанную с атомом водорода и углеводородным радикалом».

общая формула альдегидов.
2. Кетоны – соединения, содержащие карбонильную группу 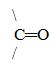 , связанную с двумя
, связанную с двумя
углеводородными радикалами.
Группу 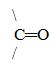 называют также кетонной группой. Кетоны – это соединения, содержащие в составе кетонную группу:
называют также кетонной группой. Кетоны – это соединения, содержащие в составе кетонную группу: 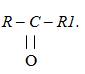
|
Альдегиды и кетоны бывают:
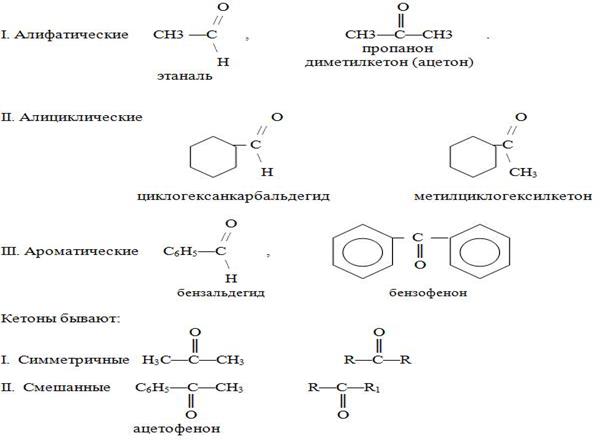 2. Номенклатура.
2. Номенклатура.
Нумерацию начинают в альдегидах с альдегидной группы. Название альдегидам дают с суффиксом – аль на конце.
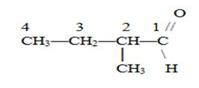 2-метилбутаналь
2-метилбутаналь
Кетоны начинают номеровать с того конца, к которому ближе кетонная группа, называют с суффиксом – он на конце.
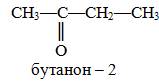
бутанон – 2
метилэтилкетон
Гомологический ряд альдегидов:
Изомерия.
Для альдегидов характерна изомерия только углеродной цепи.
Для кетонов характерна изомерия:
1. Углеродной цепи.
2. Положения кетонной группы.
Способы получения
а) Из углеводородов:

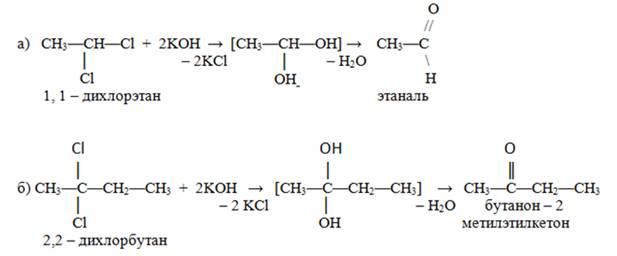
б)Из дигалогенопроизводных:
 Получение из спиртов:
Получение из спиртов:
I. Окисление спиртов:
а) Окисление первичных спиртов:

б) Окисление вторичных спиртов:

II. Дегидрирование спиртов:
а) Первичных спиртов:

б) Вторичных спиртов:

Химические свойства.
Химические свойства оксосоединений опредеяются наличием карбонильной группы. Атомы углерода и кислорода карбонильной группы находятся в состоянии sp2 -гибридизации и связаны- и π-связями, составляющими двойную связь. π-Связь образуется в результате перекрывания негибридных рz-орбиталей обоих атомов. Из шести валентных электронов атома кислорода один расходуется на образование -связи, второй – на образование π-связи. Две неподелённые пары электронов располагаются на гибридных орбиталях, которые лежат в плоскости -связей. Карбонильная группа и непосредственно связанные с ней атомы находятся в одной плоскости.
|
|
|
Строение двойной связи
Из сравнения характеристик двойной связи С=О оксосоединений и двойной связи С=С алкенов видно, что связь С-О короче, а её энергия больше, чем связи С=С. Высокая электроотрицательность атома кислорода способствует сильной поляризации связи С=О. Атом углерода карбонильной группы несёт частичный положительный заряд и является электрофильным центром.
№32.Альдегиды. Реакции нуклеофильного присоединения (взаимодействие с цианидами металлов, спиртами, производными аммиака), окисления, восстановления.
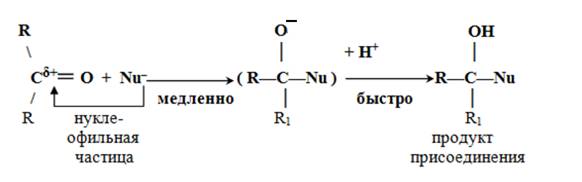
Для альдегидов характерны реакции, протекающие по механизму нуклеофильного присоединения
1. Взаимодействие с цианидом натрия:
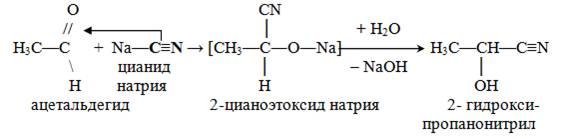
2. Взаимодействие с водой:

3. Взаимодействие со спиртами:
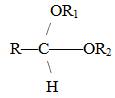
Полуацетали – соединения, содержащие при одном атоме углерода гидроксильную иалкоксильную группу:

Ацетали – соединения, содержащие при одном атоме углерода две алкоксильные группы (—OR): ацеталь
Взаимодействие с аминами.
Взаимодействие оксосоединений с первичными аминами протекает по механизму присоединения – отщепления. На первой стадии реакции происходит нуклеофильное присоединение амина по двойной связи С=О карбонильной группы. Первичным продуктом присоединения является биполярный ион, который стабилизируется в результате внутримолекулярного переноса протона от атома азота к атому кислорода, превращаясь в аминоспирт. Соединения, содержащие электроноакцепторные группы при одном атоме углерода, неустойчивы и стремятся к стабилизации. В данном случае происходит отщепление молекулы воды от молекулы аминоспирта (вторая стадия реакции) и образуется имин (основание Шиффа).
|
|
|

|
|
|


