 |
Строение карбоксильной группы
|
|
|
|
Многие свойства карбоновых кислот обусловлены наличием в их молекулах карбоксильных групп.
Атом кислорода, связанный с углеродом двойной связью, оттягивает электроны в свою сторону. Углерод приобретает некоторый положительный заряд и притягивает электроны второго атома кислорода из группы — ОН, что приводит к сдвигу электронного облака связи О — Н в направлении кислорода. Атом водорода становится подвижным.
Карбоновые кислоты обладают высокими температурами кипения, что связано с образованием водородных связей между молекулами:

Все карбоновые кислоты слабые электролиты, кроме муравьиной кислоты, она электролит средней силы.
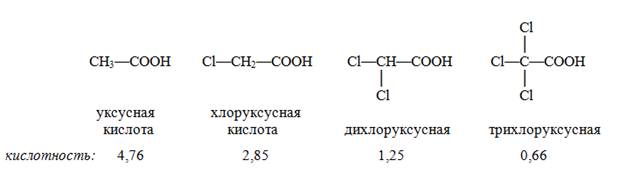
Радикалы, содержащие хлор и бром, влияют на кислотность карбоксильной группы: степень диссоциации хлоруксусной кислоты в 10 раз больше, чем уксусной, а трихлоруксусная кислота по силе близка к соляной или серной.
Кислотные свойства:

- Реакция нуклеофильного замещения:
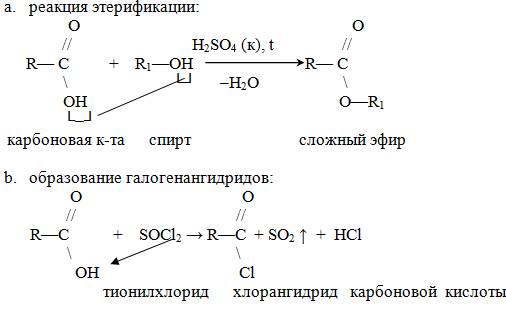
- Образование ангидридов кислот:

Образование амидов:

- Реакция замещения в радикале:

№36.Специфические реакции дикарбоновых кислот. Щавелевая, малоновая, янтарная кислоты. Применение в медицине
Дикарбоновые кислоты – органические кислоты, содержащие 2 карбоксильные группы 
В основе названий – соответствующие предельные углеводороды. В главную цепь включают атомы углерода карбоксильных групп. Наличие двух карбоксильных групп обозначается приставкой – «ди» и суффиксом – «овая».
4. Специфические реакции.
Взаимное расположение карбоксильных групп в дикарбоновых кислотах существенно влияет на их химические свойства. Первые гомологи, в которых СООН-группы сближены,- щавелевая и малоновая кислоты – способны при нагревании отщеплять оксид углерода (IV), в результате чего удаляется карбоксильная группа. Отсюда этот процесс называется декарбоксилированием.
|
|
|
По мере удлинения углеродной цепи и удаления функциональных групп ослабевает их взаимное влияние. Поэтому следующие два члена гомологического ряда – янтарная и глутаровая кислоты – при нагревании не декарбоксилируются, а теряют молекулу воды и образуют циклические ангидриды. Такой ход реакции обусловлен образованием устойчивого пяти- или шестичленного цикла.
а) декарбоксилирование (для щавелевой и малоновой кислот)

б) образование ангидридов (циклических)
т. к. по мере удлинения цепи ослабевает влияние карбоксильных групп друг на друга:

№37.Муравьиная кислота, её отличие от других карбоновых кислот. Уксусная кислота. Применение в медицине.
Муравьиная кислота относится к насыщенным одноосновным карбоновым кислотам. Муравьиная (иначе – метановая) кислота представляет собой неокрашенную жидкость, растворимую в бензоле, ацетоне, глицерине и толуоле.
Применение муравьиная кислота получила в: Медицине, как наружное обезболивающее средство; Сельском хозяйстве, где ее широко используют для заготовки кормов. Она замедляет протекание процессов распада и гниения, что способствует более длительному сохранению сена и силоса; Химической промышленности в качестве растворителя; Текстильной промышленности для окрашивания шерсти; Пищевой промышленности в качестве консерванта; Пчеловодстве, как средство для борьбы с паразитами.
Уксусная кислота – это бесцветная жидкость, обладающая кислым вкусом и резким, характерным для нее запахом. Свойства уксусной кислоты напрямую взаимосвязаны от количества содержащейся в ней воды. 70-80% раствор уксусной кислоты именуют уксусной эссенцией, а 3-9% называют уксусом.
Уксусную кислоту используют для получения душистых и лекарственных веществ, как растворитель.
|
|
|
В медицине уксусная кислота используется как основа для некоторых лекарственных средств: ацетилсалициловая кислота, уксуснокислые соли алюминия и свинца, которые применяются в качестве вяжущих средств и при лечении различных воспалительных заболеваний и процессов.
№38.Функциональные производные карбоновых кислот. Сложные эфиры. Номенклатура. Способы получения. Химические свойства. Кислотный и щелочной гидролиз. Применение в медицине.
 Сложные эфиры – это функциональные производные карбоновых или минеральных кислот, в которых гидроксильная группа заменена остатком спирта или фенола.
Сложные эфиры – это функциональные производные карбоновых или минеральных кислот, в которых гидроксильная группа заменена остатком спирта или фенола.
Реакция образования сложного эфира из кислоты и спирта называется реакцией ЭТЕРИФИКАЦИИ («этер» - эфир).
2. Физические свойства:
Сложные эфиры одноосновных карбоновых кислот – это обычно жидкости с приятным запахом: бутиловый эфир масляной кислоты обладает запахом ананаса, уксусно-изоамиловый эфир имеет запах груш и т.д.Синтетические сложные эфиры в виде фруктовых эссенций используются в производстве фруктовых вод, кондитерских изделий, при изготовлении духов и одеколонов.
3. Получение:
Реакция этерификации:
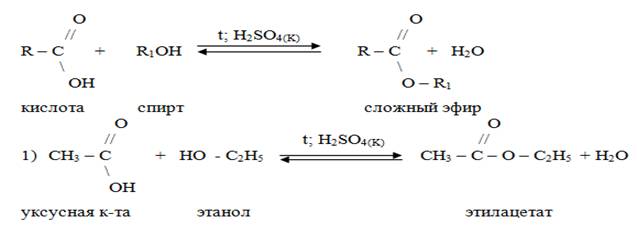
4. Химические свойства:
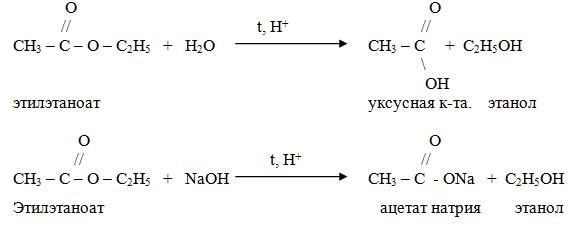
Реакция взаимодействия сложного эфира с водой, приводящая к образованию спирта и кислоты, называется ОМЫЛЕНИЕМ или ГИДРОЛИЗОМ (обратная реакция этерификации.)
№39.Амиды кислот. Номенклатура. Получение. Кислотный и щелочной гидролиз.
Номенклатура.
Важной группой функциональных производных карбоновых кислот являются амиды. Амиды также широко распространены в природе, достаточно сказать, что основа живых организмов – пептидыи белки – содержат многочисленные амидные группировки. Как и сложные эфиры, амиды используются в медицине в качестве лекарственных средств.
Амиды – это функциональные производные карбоновых кислот, в которых гидроксильная группа заменена на аминогруппу.
Существуют также N-замещённые амиды, которые представляют собой N-ацильные производные первичных и вторичных аминов.
В систематических названиях амидов к родоначальной структуре добавляется суффикс – амид. Символ N- в названиях замещённых амидов показывает, что заместитель связан с атомом азота в амидной группе.
|
|
|
CH3CH2CONH2 CH3CH2CH2CONHCH3
Пропанамид N-метилбутанамид
|
|
|


