 |
Классификация хроматографических методов анализа
|
|
|
|
КОНСПЕКТ ЛЕКЦИЙ
по дисциплине
ХРОМАТОГРАФИЯ В ХИМИЧЕСКОЙ ТЕХНОЛОГИИ
Направление подготовки 240100 «Химическая технология»
Преподаватель: Сайфутдинов Б.Р., ассистент кафедры ХТПНГ, к.х.н.
САМАРА 2013 г.
Лекционный курс 18 часов (зачет) – 6 семестр
Лекция 1 (2 часа)
Хроматографический метод: характеристика, цели и задачи
Введение
На протяжении последних 50-ти лет одним из наиболее значительных явлений, определяющих методологию научного исследования во многих естественных дисциплинах, является широкое распространение хроматографических методов разделения и анализа веществ и их смесей.
К середине прошлого века значительных успехов достигли экспериментальные методы идентификации и количественного определения индивидуальных веществ: электрохимические, спектрально-оптические методы, рентгеноструктурный анализ, масс-спектрометрия, ЯМР и др. Однако арсенал классических методов разделения сложных смесей веществ оказался недостаточным для решения сложнейших научных задач, стоящих перед современной аналитической химией.
Устранение такого несоответствия между возможностями изучения индивидуального соединения и возможностями выделения его из сложной смеси связано с развитием хроматографических методов. Первые успешные опыты по хроматографии были проведены еще в начале 20-го века русским ученым Михаилом Семеновичем Цветом [1]. Используя набивную колонку с порошком кальцита, введя в ее верхнюю часть вытяжку из зеленых листьев растений и пропуская через нее петролейный эфир, он получил окрашенные в разные цвета зоны колонки, соответствующие компонентам вытяжки. М.С.Цвет предложил и сам термин «хроматография» (от греческих слов «хрома» – цвет и «графо» – пишу).
|
|
|
В дальнейшем колонки, содержащие различные адсорбенты, ионообменники, жидкие неподвижные фазы, широко использовались для накопления, очистки и разделения тех или иных компонентов смесей. С позиций аналитической химии эти способы имели два существенных недостатка:
1. длительность экспериментов составляла многие часы и сутки,
2. разрешающая способность, или эффективность процесса, была низка.
Революционное значение для появления аналитической хроматографии имело открытие метода газо-жидкостной хроматографии Джеймсом и Мартином в 1952 г. [2] и существенная модернизация метода газо-адсорбционной хроматографии Янаком в 1953 г. [3]. Неспецифичность, чувствительность детектирования и высокая разделяющая способность колонок обеспечили методу газовой хроматографии чрезвычайно широкую область применения при анализе объектов органической природы. Появившийся на рубеже 60-70-х годов метод высокоэффективной жидкостной хроматографии (ВЭЖХ) [4] расширил круг анализируемых органических соединений на полярные и другие труднолетучие вещества. Наконец, с открытием в 1975 г. метода ионной хроматографии [5] появилась возможность экспрессного и высокоинформативного анализа ионных смесей.
Дальнейшее развитие аналитической хроматографии шло в направлениях модернизации аппаратуры (сорбенты, режимы, детекторы), математического моделирования процессов разделения, развития способов получения качественной и количественной информации из данных хроматографического эксперимента и поиска новых областей приложения хроматографии.
Определение аналитической хроматографии
Цель высокоинформативного аналитического метода – распределить компоненты или их характеристики по разным участкам пространства или по шкалам времени, длины волны, потенциала, энергии, температуры, массы и т.п. и по-возможности раздельно определить концентрации аналитов. Первую из перечисленных целей – раздельное распределение компонентов смеси в пространстве – в аналитической химии ставят перед методами хроматографии. Отсюда выводится определение аналитической хроматографии:
|
|
|
аналитическая хроматография – это совокупность методов аналитической химии, селективность которых определяется процессами, приводящими к раздельному распределению компонентов смеси в пространстве, а полнота анализа обеспечивается универсальным детектированием.
Из физической химии известно, что существует два крайних случая пространственного разделения химических веществ: при равновесии, за счет разных термодинамических свойств, и в отсутствие равновесия, за счет разной подвижности. Первый случай реализуется в гетерофазных процессах за счет различия сродства несмешивающихся фаз к разным компонентам. Второй случай обусловлен различной кинетикой компонентов в физических и/или концентрационных полях. Методы аналитической химии, использующие кинетически обусловленное пространственное распределение компонентов (например, гельпроникающая хроматография, электрофорез, изотахофорез и т.п.), не являются сорбционными методами и в настоящем курсе не рассматриваются.
Задачи аналитической хроматографии заключаются в том, чтобы:
· для заданных аналитов подобрать селективные и эффективные фазы (подвижную и неподвижную),
· найти наиболее подходящее аппаратурное оформление,
· выбрать наилучшие режимы разделения,
· определить состав смеси с минимальной ошибкой.
Принципиально методы аналитической хроматографии базируются на физико-химических методах разделения смесей веществ, основой которых, в свою очередь, являются адсорбционные, ионообменные и экстракционные (распределительные) процессы.
Методы разделения смесей веществ
Классификация хроматографических методов анализа
Известны три типа термодинамически устойчивых агрегатных состояния вещества: газообразное, жидкое, твердое. Для распределения вещества между фазами важную роль играет межфазная граница – ее площадь, а также физические и химические свойства. Из всевозможных сочетаний для двухфазных систем, очевидно, следует исключить пары газ-газ и твердое-твердое: в первом случае невозможно разделение на фазы, а во втором – процессы распределения вещества между фазами крайне замедленны и не используются в аналитической химии.
|
|
|
Таким образом, представляют интерес следующие двухфазные системы:
· газ - жидкость,
· газ - твердое тело,
· жидкость - жидкость (для несмешивающихся жидкостей),
· жидкость - твердое тело.
В указанных системах могут происходить следующие процессы:
· испарение (обратный процесс — конденсация),
· растворение (обратный процесс — осаждение),
· адсорбция — явление концентрирования вещества на границе (т.е. поверхности) раздела фаз,
· абсорбция — явление преимущественного распределения вещества в объеме одной из контактирующих фаз (механизм процесса абсорбции называют распределительным),
· экстракция (в узком понимании) — абсорбция с участием реакций образования нейтральных комплексов и ионных ассоциатов,
· ионный обмен — реакция вытеснения ионов, находящихся в фазе ионообменника, эквивалентным количеством ионов того же знака из жидкой фазы.
Первые два процесса (прямые в сочетании с обратными) обычно используются для очистки и выделения одиночных (целевых) компонентов в аппаратах для дистилляции, ректификации и кристаллизации. Процессы адсорбции, экстракции (в широком смысле - абсорбции) и ионного обмена являются более универсальными: они широко используются не только для отделения одного из компонентов от примесей, но и для разделения компонентов между собой. Именно эти процессы в результате многократного повторения приводят к пространственному разнесению зон чистых компонентов, что и используется в хроматографии.
В соответствии с типом подвижной фазы (ПФ) производится классификация видов хроматографии:
· газовая, имеющая два подвида для разных агрегатных состояний неподвижной фазы (НФ): газо-адсорбционная и газо-жидкостная; основные механизмы разделения в газовой хроматографии — адсорбция, распределение;
|
|
|
· жидкостная (высокоэффективная жидкостная хроматография, ВЭЖХ), имеющая два подвида для разных по полярности пар ПФ-НФ: нормально-фазовая (ПФ – неполярная, НФ - полярная) и обращенно-фазовая (ПФ – полярная, НФ - неполярная); основные механизмы разделения в ВЭЖХ — адсорбция, распределение;
· экстракционная, являющаяся случаем жидкостной хроматографии, когда не только ПФ, но и НФ жидкие, а процессом, приводящим к разделению, служит экстракция;
· ионная, являющаяся случаем жидкостной хроматографии, когда процессом, приводящим к разделению, служит ионный обмен.
В приведенную классификацию не вошли (и, соответственно, не будут рассмотрены в настоящем курсе) следующие хроматографические методы:
· молекулярно-ситовая (эксклюзионная, гельпроникающая) хроматография, использующая процесс эксклюзионного разделения молекул разных размеров на молекулярных ситах и гелях – специальных микропористых материалах; эксклюзия – это разная доступность внутреннего объема НФ для молекул разных размеров, формы, полярности и т.п., процесс эксклюзии имеет кинетический характер, его эффективность определяется различием в длине траекторий для компонентов разделяемой смеси;
· критическая хроматография – вариант молекулярно-ситовой хроматографии в условиях перехода «клубок-глобула» для разделяемых полимеров [6];
· сверхкритическая флюидная хроматография – гибридный вариант газовой и жидкостной хроматографии.
По условиям, задаваемым на входе в разделяющую систему, хроматографические процессы подразделяются на следующие (рис. 2.1):
· элютивный (другие названия: элюативный, элюентный, проявительный) процесс, когда ПФ, постоянно пропускаемая через НФ, не содержит аналитов, а определяемая смесь вводится в систему в начальный момент эксперимента кратковременно в виде малой добавки;
· фронтальный процесс, когда ПФ представляет собой разделяемую смесь; начало эксперимента совпадает с началом движения ПФ;
· вытеснительный процесс, когда ПФ представляет собой разделяемую смесь с добавкой элюирующего компонента, наиболее сильно сорбирующегося неподвижной фазой; начало эксперимента совпадает с началом движения ПФ.
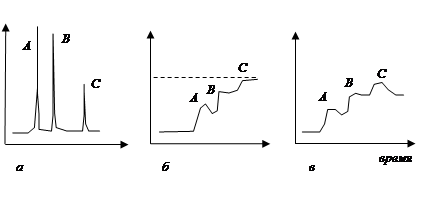
Рис. 2.1. Выходные кривые хроматографических процессов, различающихся условиями на входе: а - элютивный, б - фронтальный, в - вытеснительный процессы. A,B,C – компоненты смеси.
В методах аналитической хроматографии используется, главным образом, элютивный процесс, достоинством которого является четкость проявления зон – в виде пиков, и независимость их положения от концентраций компонентов пробы.
|
|
|
Элютивный процесс в изократическом варианте осуществляется с помощью ПФ постоянного состава и с постоянным расходом. Элютивный процесс в градиентном варианте осуществляется с помощью ПФ переменного состава и/или с переменным расходом. Соответствующие режимы для газовой хроматографии, где главным параметром, определяющим условия разделения, является температура, представляют собой изотермический режим и режим с программированием температуры.
Геометрия разделяющей системы реализуется в двух вариантах: планарная система – используется в тонкослойной и бумажной хроматографии, и колоночная (цилиндрическая) система (насадочные, микронасадочные и капиллярные колонки) – используется в высокоэффективных методах аналитической хроматографии. В настоящем курсе рассмотрены только колоночные виды хроматографии, как наиболее информативные и точные методы анализа.
Размерность хроматографической системы определяется числом разделяющих колонок: хроматография с одной разделяющей колонкой – одномерная, с двумя и более колонками – многомерная.
При всем различии, связанном с видом контактирующих фаз в гетерофазных системах, процессы адсорбции, экстракции и ионного обмена объединяет принцип распределения вещества:
· в адсорбции – между свободной фазой и межфазной границей (последняя является поверхностью адсорбента и, следовательно, принадлежит ему),
· в экстракции (абсорбции) или ионном обмене – между объемами свободной фазы и жидкого экстрагента или твердого ионообменника.
В каждой из перечисленных пар вторая фаза имеет большее сродство к веществу и поэтому является накопителем, или сорбентом. Следовательно, эти процессы можно объединить термином сорбционные процессы, а адсорбент, экстрагент и ионообменник можно обозначить словом сорбенты.
Заметим, что традиционно экстрагенты при использовании их в экстракционных реакторах не называют сорбентами, однако для продукта, полученного путем нанесения экстрагента тонкой пленкой на твердый носитель, название «сорбент» вполне приемлемо. Для простоты изложения там, где это возможно, мы не будем делать различий между сорбентами и экстрагентами, процессами сорбции и экстракции.
|
|
|


