 |
Антиоксиданты и их синергисты
|
|
|
|
А н т и о к с и д а н т ы - это вещества, предотвращающие окислительные процессы в липидах путем блокирования цепной реакции в результате образования стабильных промежуточных продуктов.
С и н е р г и с т ы - это вещества, усиливающие действие анти-оксидантов, но не обладающие антиокислительными свойствами. К синергистам относятся также вещества, которые инактивируют ионы тяжелых металлов, связывая их в комплексные соединения.
Однако в ряде случаев одно и то же вещество может выполнять различные функции, являясь и антиоксидантом, и синергистом.
Применение антиоксидантов в сочетании с синергистами позволяет увеличить продолжительность хранения жиров и жиросодержащих продуктов, максимально сохранить их пищевую ценность и качество.
Механизм действия антиоксидантов основан на прерывании реакции автоокисления липидов. Механизм окислительной порчи жиров подробно изложен в ряде учебников [5, 15, 19], поэтому в этом разделе рассмотрим некоторые особенности действия антиоксидантов и их синергистов. В соответствии с перекисной теорией Баха-Энглера и учением о цепных вырожденно-разветвленных реакциях в процессе окисления липидов образуются свободные радикалы путем отнятия атома водорода от углеводородной цепи свободной или связанной с глицерином жирной кислоты.
Свободный радикал жирной кислоты R присоединяет кислород под действием тепловой или световой энергии и образуется свободный пероксид-радикал.
 R· + О2 RОО· (1)
R· + О2 RОО· (1)
Этот радикал способен к реакции с донатором водорода, при этом образуется первый стабильный промежуточный продукт самоокисления - гидроперекись RООН и вновь свободный радикал жирной кислоты.

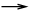 RОО· + RН RООН + R· (2)
RОО· + RН RООН + R· (2)
|
|
|
Эта последовательность реакций зависит от образования радика-лов и протекает вначале медленно.
Однако, когда накапливается достаточно гидроперекисей, они распадаются в ходе бимолекулярной реакции на радикалы, освобождающие высокореакционные фрагменты и создающие таким образом самоускоряющуюся цепную реакцию автоокисления.

 2RООН RОО· + RО· + Н2О (3)
2RООН RОО· + RО· + Н2О (3)
Антиокислители АН вступают в реакцию (2), причем возникающие радикалы А· более стабильны, чем радикалы R· и не ускоряют реакцию (1). Вследствие этого увеличивается период индукции.
 АН + RОО· RООН + А· (4)
АН + RОО· RООН + А· (4)
Синергисты (SН2) могут восстанавливать радикалы А·, но не в состоянии реагировать с RОО· по реакции (4).
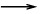 SН2 + 2А· S + 2АН (5)
SН2 + 2А· S + 2АН (5)
Антиокислители способны отщеплять водород и образовывать относительно стабильные радикалы. Синергисты также являются донаторами водорода (5), его акцепторами будут только радикалы А·, но не пероксид-радикалы.
В результате этих реакций замедляется образование продуктов распада перекисей и гидроперекисей (альдегидов, кетонов, эпоксидов, низших жирных кислот), а также продуктов полимеризации и конденсации различного строения, ухудшающих органолептические свойства, пищевую ценность и качество жира.
В пищевой промышленности применяются естественные и синтетические антиоксиданты.
К естественным антиоксидантам относятся: токоферолы (вита-мин Е, флавоны, рутин, кверцетин), эфиры галловой кислоты, гвояковая кислота, препараты из сои, овса, из различных семян и пряностей, госсипол хлопкового масла, сезомол кунжутного масла и другие.
К синтетическим антиоксидантам относятся: бутилоксианизол, бутилокситолуол, орто- и пародифенолы, пропилгаллат, додецилгаллат и другие.
В качестве синергистов чаще всего применяются аскорбиновая кислота и ее производные.
Токоферолы. Жировые продукты содержат определенное количество природных антиоксидантов среди них наибольшее значение имеют токоферолы, которыми особенно богаты растительные масла. В маслах токоферолы представлены смесью нескольких изомеров (a, d, g - изомеры). a-токоферол проявляет большую витаминную активность и меньшую антиокислительную, d-изомер - наоборот. В животных жирах токоферолы встречаются лишь в небольшом количестве (5-30 мг/кг), недостаточном для консервирующего действия. Эффективность их достигается при добавлении в животные жиры или их жировые эмульсии антиоксидантов в количестве более 30 мг/кг. Сильные антиоксидантные свойства проявляются в сочетании с аскорбиновой и лимонной кислотами.
|
|
|
Масла из зародышей пшеницы и маиса содержат много токоферолов и могут использоваться в качестве антиоксидантов.
С токсикологической точки зрения нет отрицательных данных по использованию токоферолов в качестве антиоксидантов.
Аскорбиновая кислота и ее производные. К ним относятся L- и D-формы аскорбиновой кислоты, их пальмитаты, стеараты и миристаты, а также D-изоаскорбиновая кислота, эриторбовая кислота и ее натриевые соли. Они чаще применяются как синергисты.
Аскорбинпальмитаты широко применяются для растительных масел, маргаринов, сливочного масла и майонезов. L-аскорбиновая кислота добавляется в сухое молоко. Большое значение имеет добавление аскорбиновой кислоты в пищевые продукты растительного происхождения, приобретающие темную окраску вследствие ферментативных процессов. Добавление аскорбиновой кислоты в количестве 1-2 г/кг продукта позволяет сохранить цвет и запах многих консервированных фруктов.
Применение аскорбиновой кислоты сокращает использование нитритов при производстве мясных продуктов. Она предотвращает образование нитрозаминов.
В большинстве стран разрешается применять аскорбиновую кислоту и ее соли.
Препараты из сои. В сое содержатся токоферолы, поэтому препараты на основе сои можно использовать в качестве антиоксидантов. Соя содержит лецитин, поэтому применяется как эмульгатор. Экстракты из соевой муки хорошо сохраняют каротиноиды.
Препараты из овса. Беззародышевые зерна овса тормозят окисление жиров и жиросодержащих выпечных изделий, а также применяются для стабилизации аскорбиновой кислоты. Механизм действия изучается.
|
|
|
Производные флавона. К ним относятся кверцетин, кверцитрин и рутин. Антиокислительное действие их сильнее, чем галлатов. В качестве синергистов кверцетина применяется лимонная и аскорбиновая кислоты. Эти соединения не токсичны и ограничений на их применение нет.
Гваяковая смола. Это нерастворимая в воде аморфная масса, состоящая из a- и d-гваяковых кислот. Добывается из тропических деревьев семейства гваяковых. Применяется для животных жиров в концентрациях 1-2 г/кг.
Эфиры галловой кислоты (галлаты). К наиболее распространенным эфирам галловой кислоты относятся пропилгаллат, октилгаллат, додецилгаллат и лаурилгаллат. В воде они не растворимы, в жирах хорошо растворяются лишь октил- и додецилгаллат.
Галлаты - очень эффективные антиоксиданты, они применяются для сохранения жиров, масел и эмульсий в количестве 50-200 мг/кг. Их действие усиливается добавлением синергистов - лецитина или лимон- ной кислоты. Галлаты добавляют в сухое молоко, картофельные чипсы, сельдь жирную, а также для стабилизации витамина А.
Пропилгаллат используют при производстве бульонных куриных и мясных кубиков.
Однако галлаты способны образовывать с ионами тяжелых металлов, особенно с ионами железа (Fе3+), интенсивно окрашенные соединения, что может ухудшить окраску жиров. Допустимое содержание галлатов в продуктах 0,2%.
К антиоксидантам естественного происхождения относятся экс- тракты из семян редиса, рапса, томатов, различных пряностей (анис, кардамон, кориандр, укроп, горчица, имбирь, красный перец, шалфей, розмарин), а также препараты из шелухи какао.
Из синтетических антиоксидантов широко в мире применяются бутилоксианизол (БОА) и бутилокситолуол (БОТ). Они имеют идентичный механизм антиокислительного действия и эффективно подавляют автоокисление липидов в концентрациях 20-200 мг/кг продукта.
Этими веществами также можно пропитывать упаковочный материал для жиров и изделий, содержащих значительное количество жира.
|
|
|
В РФ допущены: аскорбиновая кислота (ПДК не лимитируется) - для задержки окисления маргарина; БОА и БОТ (ионол) - для животных топленых жиров и шпика соленого (ПДК - 200 мг/кг); додецилгаллат - для жиров пищевых концентратов (ПДК - 100 мг/кг). БОТ применяется для пропитки упаковочных материалов, используемых для кексов, шоколадных изделий, крупяных и других продуктов из расчета 0,5 г на один килограмм упаковочного материала.
Активность этих окислителей повышается в присутствии других фенольных антиокислителей или синергистов. Они не вызывают изменения органолептических свойств пищевых продуктов.
Ферментные препараты
Для производства многих видов пищевых продуктов требуется длительное время.
Определенное место в совершенствовании технологических процессов, ускорении производства различных продуктов питания отводится ферментным препаратам. Ферменты, добавляемые к продуктам питания, позволяют ускорить процессы созревания мяса и рыбы, выход сока из плодов и овощей, брожение крахмала, теста и т.д. Это дает возможность снизить себестоимость продукции, ускорить сроки ее изготовления, улучшить качество пищевых продуктов. Ферментные препараты в настоящее время широко применяются при производстве пива, спирта, консервов, в хлебопекарной, рыбо- и мясоперерабатывающей промышленности. Чаще всего ферментные препараты применяются при производстве плодовых и овощных соков, для увеличения выхода сока, его осветления [28].
Все ферментные препараты (ФП) тщательно изучаются в гигиеническом отношении, так как среди продуцентов ФП грибного или бактериального происхождения могут быть токсикогенные штаммы микроорганизмов.
ФП, используемые при обработке пищевых продуктов с целью токсикологической оценки, подразделяются на 5 классов:
1. Ферменты, полученные из тканей животных, обычно используемых в пищу. Они рассматриваются как пищевые продукты и считаются допустимыми при условии, что для них могут быть разработаны удовлетворительные химические и микробиологические спецификации;
2. Ферменты, полученные из частей растений, используемых в пи- щу. Они также рассматриваются как пищевые продукты и считаются допустимыми при условии, если для них могут быть разработаны удовлетворительные химические и микробиологические спецификации;
3. Ферменты, полученные из микроорганизмов, традиционно ис- пользуемых в приготовлении пищи. Эти препараты также рассматриваются как продукты питания и считаются допустимыми при условии, что они снабжены микробиологическими и химическими спецификациями;
4. Ферменты, полученные из непатогенных микроорганизмов, яв- ляющихся контаминантами пищи. Эти препараты не считаются продуктами питания. Для них необходимо разработать спецификации, проводя краткосрочные токсикологические исследования. Оценка этих ферментов в каждом случае производится индивидуально, после чего устанавливается величина допустимого суточного потребления.
|
|
|
5. Ферменты, получаемые из малоизвестных микроорганизмов. Эти препараты требуют химических и микробиологических спецификаций и более подробного токсикологического изучения.
Оценка безопасности ферментов не зависит от того, добавляются ли ферменты непосредственно в пищу или используются в иммобилизованной форме. Особенно важна токсикологическая оценка ферментов, относящихся к 4-му и 5-му классам.
При этом необходимо учитывать следующее:
- ферментные препараты добавляют непосредственно в пищевой продукт и не удаляют из него;
- ферментные препараты добавляют в пищевой продукт, но удаляют из конечного продукта в соответствии с технологией;
- иммобилизованные ферментные препараты находятся в контакте с продуктами питания только в процессе обработки.
Наименование препаратов, согласно принятой в России и СНГ номенклатуре, указывает на вид ферментной активности (протеолитическая и др.), продуцент и метод культивирования (поверхностный - П, глубинный - Г), а также степень концентрирования ферментов по сравнению с исходной культурой продуцента. Так, например, из названия "Протосубтилин Г10х" следует, что фермент протеолитический, получен из В.Subtilis глубинным методом и концентрирован десятикратно.
Ферментные препараты широко применяются при производстве соков. Так, для увеличения выхода сока используются ферментные комплексы, содержащие: протеолитические, пектолитические, гемицеллюлазные и целлюлазные составляющие; в некоторых случаях содержатся амилазные, если в сырье содержится крахмал.
В настоящее время принята следующая номенклатура пектолитических ферментов.
Пектинэстераза (ПЭ) гидролизует эфирные связи метилового спирта, и последний выделяется в свободном состоянии.
Эндополиметилгалактуроназа (эндо-ПМГ) разрывает цепь пектина произвольно по длине, причем соседние галактуроназные остатки должны быть метилированными.
Экзополиметилгалактуроназа (экзо-ПМГ) разрывает крайние a-1® 4-связи, т. е. отщепляет только крайние галактозные кольца, что способствует образованию свободного сахара (глюкозы).
Эндополигалактуроназа (эндо-ПГ) фрагментирует полигалактуроновую (пектовую) кислоту и слабо этерифицированную полигалактуроновую кислоту, называемую еще пектиновой кислотой.
Экзополигалактуроназа (экзо-ПГ) осахаривает крайние галактоз- ные кольца, если они неэтерифицированы.
Трансэлиминазы разрывают негидролитическим путем пектиновые вещества с образованием двойной связи в галактуроновом остатке между четвертым и пятым атомами углерода.
По субстратной специфичности трансэлиминазы делятся на эндопектинтрансэлиминазу (эндо-ПТЭ), экзопектинтрансэлиминазу (экзо-ПТЭ), эндополигалактуроназотрансэлиминазу (эндо-ПГТЭ) и экзополигалактуроназотрансэлиминазу (экзо-ПГТЭ), аналогично делятся полигалактуроназа и полиметилгалактуроназа.
Ферментативный препарат (комплекс) подбирается в зависимости от химического состава плодов и цвета.
Для слабоокрашенных (яблоки, груши, белый виноград, айва и т.п.) комплекс ферментов должен содержать пектинэстеразу, эндополи- галактуроназу, эндополиметилгалактуроназу. Желательно содержание протеиназы, экзополигалактуроназы, гемицеллюлазы и целлюлазы. Нежелательно наличие пектинтрансэлиминазы, аскорбатоксидазы, антоцианоксидазы. Недопустимо наличие пероксидазы, фенолоксидазы, каталазы.
Для сильноокрашенных красных плодов (вишня, малина, клубника, смородина и др.) ферментный препарат должен содержать: пектинэстеразу, эндополигалактуроназу и пектинтрансэлиминазу. Желательно содержание аналогичных ферментов, нужных для светлых плодов. Нежелательно наличие пероксидазы, полифенолоксидазы и каталазы. Недопустимо присутствие антоцианоксидазы и аскорбиназы.
Чем объяснить, что одни ферменты нужны, другие не нужны? При получении осветленного сока из светлых плодов образуется мезга, которую необходимо обработать. Под действием эндополигалактуроназы (эндо-ПГ), экзо-ПМГ и пектинэстеразы резко снижается вязкость полученного сока. Протеиназа, экзо-ПГ, целлюлаза и гемицеллюлаза повышают проницаемость клеточных стенок, способствуя увеличению выхода сока. Наличие пектинтрансэлиминазы нежелательно, потому что она катализирует разложение нерастворимого пектина и активизирует мацерацию плодовой ткани; это ухудшает дренажные свойства плодовой мезги. Окислительные ферменты ухудшают цвет.
При производстве соков с мякотью (нектаров), наоборот, желательно наличие мацерирующих ферментов, но нежелательно присутствие эндополигалактуроназы, которая понижает вязкость жидкой фазы и ускоряет расслоение нектара. При производстве этих соков определяющую роль играют пектинтрансэлиминаза, гемицеллюлаза и целлюлаза. Пектинтрансэлиминаза способствует превращению протопектина в пектин, а целлюлаза и гемицеллюлаза улучшают консистенцию сока. Полигалактуроназа и особенно эндополигалактуроназа нежелательны, потому что уменьшают вязкость и гомогенность.
Максимальная сокоотдача и хорошее осветление, а также наиболее низкая вязкость отжатого после прессования сока получаются под действием эндо-ПГ и эндо-ПМГ, т.е. двух ферментов. Чем выше степень этерификации пектина, тем больше вязкость сока и тем слабее будет эффективность эндо-ПГ, а выше эффективность эндо-ПМГ.
Обычно трансэлиминазы имеют оптимум действия в нейтральном рН, поэтому в нормальных условиях мало эффективны, но все-таки способствуют мацерации тканей плодов и овощей.
Дубильные вещества отрицательно влияют на пектолитические ферменты, но и сами изменяются под действием ферментов. Ингибирующий эффект на них оказывает лимонная кислота, а полигалактуроназа чувствительна к фенольным соединениям и особенно к окисленным лейкоантоцианам и катехинам.
Выпускаемые в настоящее время пектолитические препараты обычно являются полиферментами и их ферментный состав зависит от продуцента (микроорганизма) и условий получения. Поэтому для каждого препарата необходимо предварительно установить оптимальные условия его использования для данного сырья. Кроме того, следует иметь в виду, что сырье тоже содержит пектолитические ферменты.
Расщепление пектиновых веществ происходит под действием двух групп пектолитических ферментов - гидролитических (эндо-ПГ, экзо-ПГ, эндо-ПМГ) и ферментов липазного типа, разрывающих a-1®4-связи и образующих ненасыщенные мономерные остатки галактуроновой кислоты (эндо-ПТЭ, экзо-ПТЭ, эндо-ПГТЭ и экзо-ПГТЭ).
У яблок, груш и айвы под влиянием пектинэстеразы и полигалак- туроназы разрушается растворимый пектин, вязкость клеточного сока понижается, выход сока увеличивается.
Если ферментный препарат содержит пектинтрансамилазу и другие мацерирующие ферменты, то часть нерастворимых пектиновых веществ переходит в растворимые формы. Это приводит к повышению вязкости клеточного сока и соответствующему понижению выхода сока.
Для нежных плодов - земляники, малины, смородины под влиянием пектолитических ферментов быстро нарастает проницаемость клеточных мембран, нарушается целостность самих клеток, вязкость сока падает, а выход увеличивается на 20%.
Для черешни, вишни и винограда, у которых окрашена лишь кожица, обработка ферментами должна обеспечить мацерацию не только мякоти, но и кожицы, для того чтобы могли экстрагироваться и антоцианы, содержащиеся в них. Это достигается примерно за три часа. Выход сока повышается на 5-7%.
Для некоторых косточковых плодов (созревших слив, абрикосов, персиков и др.), обработка ферментами обязательна в целях понижения вязкости сока. При этом выход сока повышается на 12-20%, достигая 50-55%.
Для предотвращения ухудшения цвета под действием окислительных ферментов, рекомендуется бланшировать сливы, черные сорта винограда и другие плоды. Термическая обработка яблок, айвы, белых сортов винограда исключена. Вместо нее используется обработка химическими препаратами, которые, однако, не должны мешать гидролитическим процессам. Применяют SО2, сорбиновую кислоту, бензоат натрия, аскорбиновую кислоту и др.
В противном случае в течение трех - четырех часов обработки ферментами окислительные ферменты сильно ухудшают качество полученного сока.
К сокам и компотам перед герметизацией банок прибавляют глюкозидазу и каталазу с целью понижения окислительных реакций.
Глюкозидаза окисляет глюкозу до глюконовой кислоты, и выделяется пероксид водорода, который разлагается каталазой.
Протеолитические ферментные препараты понижают содержание белков в осветленных соках и этим предотвращают их помутнение на белковой основе.
При производстве соков из цитрусовых плодов добавляют фермент нарингиназу с целью разрушения нарингина (7-рамнозидо- b-глюкозидо-4,5,7-тригидроксифлавонон), придающего соку горький вкус. Пектолитические препараты также гидролизуют нарингин с образованием прунина и нарингинина, которые не имеют горького вкуса. Но этот процесс протекает намного медленнее.
Ферментные препараты нашли широкое применение не только при производстве соков, но и в других отраслях пищевой промышленности.
Так, ферментные препараты из грибов Aspergillus terricola, штамм 3374 и As.oryzae, штамм КС ускоряют созревание соленой сель- ди, а также разрешены в качестве размягчителей полуфабрикатов из грубых сортов мяса.
Фицин - растительный фермент, получаемый из сока инжира, применяют для обработки мяса перед приготовлением вторых блюд. Под влиянием ферментного препарата мясо приобретает нежную, мягкую консистенцию и приятный вкус, что объясняется гидролитическим изменением белка.
ФП липооризин ГЗХ, выделяемый Rhizopus cryzae, может использоваться для структурированных рыбных продуктов.
Иммобилизованные ферменты. Ферменты могут использоваться "однократно" и "многократно". При классических методах ферментативной обработки сырья ферменты остаются в продукте или инактивируются при однократном использовании.
Созданы новые формы ферментных препаратов, используемых многократно. Их называют иммобилизованными связанными, фиксированными, матрицированными, но чаще употребляется термин "им-мобилизованные". Для иммобилизирования ферментов используют разнообразные носители неорганического и органического происхождения.
Органические носители - полимеры природного и синтетического характера. К полимерам природного происхождения относятся полисахариды и белковые носители в качестве остатков целлюлозы, декстрина, крахмала (амилозы и амилопектина), агарозы.
В качестве синтетических полимерных носителей используются полиметиленовые, полиамидные и полиэфирные соединения.
Наиболее перспективными неорганическими носителями являются микропористые силикагели, пористые стекла, аэросилогели и др.
К носителям предъявляются определенные требования: они не должны растворяться в среде, которая будет обрабатываться ферментом, вызывать конформационные изменения в молекулах белков ферментов и других белков, содержащихся в обрабатываемом продукте, и должны отличаться по электрическому заряду от заряда фермента, обладать высокой химической, биологической и механической устойчивостью, иметь высокую гидрофильность, легко поддаваться гранулированию и активизации. Носители могут выпускаться в форме зерна, волокон, колец, трубочек и т.д.
Все способы связывания ферментов с носителями делятся на две группы: без образования ковалентных связей между белком и матрицей (физические методы иммобилизации) и с образованием ковалентных связей (химические методы иммобилизации). В настоящее время химические методы являются основными. Полученные посредством этого метода препараты являются стабильными, ферменты "не отмываются" от носителя, понижая отрицательное действие матрицы на сам фермент. Существенным недостатком является частичная инактивация фермента, который иммобилизован.
Современное направление - иммобилизация целых микробных клеток и их использование для определения соответствующих ферментных реакций.
Иммобилизованные ферменты отличаются по свойствам от нативных ферментов, так как несколько изменяется пространственная структура ферментной белковой молекулы, поэтому иммобилизация понижает активность ферментов. Однако иммобилизация приводит к расширению границ температуры и рН, более эффективному действию ферментов, что является преимуществом. Кроме того, активизация ферментативных реакций сохраняется и снижается отрицательное влияние ингибиторов.
|
|
|


