 |
Основные типы реакций радикалов
|
|
|
|
Реакции замещения (отрыв атома водорода).
Для реакций замещения характерно вовлечение в цепь органического вещества за счет бимолекулярной реакции его со свободными радикалами, которые всегда атакуют периферийные атомы молекулы, обычно атомы водорода. Поэтому большинство этих реакций состоит в замещении водорода органических веществ на те или иные функциональные группы.

Общее правило радикального замещения: преимущественно замещаются те атомы водорода, при отрыве которых образуются наиболее стабильные радикалы (третичный > вторичный > первичный), или те, для которых энергия связи наименьшая. Отсюда следует малая вероятность радикальных реакций по связям О - Н или N - Н, энергия разрыва которых превышает 400 кДж/моль. С другой стороны, вещества, имеющие в молекуле разные атомы водорода, обычно образуют смеси изомеров.
В процессах галогенирования разные атомы галогенов проявляют разную избирательность при атаке атомов водорода, зависящую от активности галогена; чем реакционноспособнее атом галогена, тем менее избирательно он атакует те или иные положения молекулы (наименьшую избирательность реакции с активным фтором и наибольшую - с бромом).
Сложнее протекают процессы окисления. Например, образование гидропероксидов состоит из двух элементарных стадий:

из которых лимитирующая - вторая, в связи с чем пероксидный радикал ROO× обычно преобладает в смеси, и обрыв цепи происходит на нем. Пероксидный радикал менее реакционноспособен по сравнению с атомом хлора, что обусловливает большую избирательность окисления по сравнению с хлорированием. Из гидропероксидов получают спирты и кетоны.
Для ускорения процессов жидкофазного окисления используют каталитические добавки солей или комплексов металлов переменной валентности (Со, Мn, Сu и др.), роль которых заключается в образовании свободных радикалов.
|
|
|
Реакции расщепления.
Акт расщепления всегда происходит с образованием свободных радикалов и ненасыщенных молекул органического вещества.






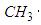
Реакции присоединения.
Реакции присоединения к связи С=С образуют наиболее важную группу реакций с участием радикалов.
Присоединение радикалов происходит по кратной связи.
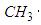



В случае несимметричного олефина радикал, первично атакующий ненасыщенный атом углерода, присоединяется таким образом, что промежуточно образуется наиболее стабильный из возможных радикалов (третичный > вторичный > первичный). Это правило радикального присоединения аналогично сформулированному ранее для радикального замещения.
Особое значение имеют также реакции присоединения галогенов и галогеноводородов. При радикально-цепном гидробромировании пропилена первично присоединяется по двойной связи не водород, а бром:

Следовательно, НВr присоединяется против правила Марковникова, образуя н-пропилбромид. Подобно этому к олефинам присоединяется сероводород, дающий первичные меркаптаны:

В большинстве реакций радикального присоединения из двух стадий продолжения цепи лимитирующей является вторая, так как энергетически она наименее выгодна. Это означает, что концентрация участвующего в ней радикала больше, чем концентрация второго, и обрыв цепи происходит именнона нем. От этого зависит и реакционная способность олефинов при радикальном присоединении. Действительно, при наличии в олефине электронодонорных заместителей промежуточный радикал стабилизируется ими и оказывается менее реакционноспособным при второй, лимитирующей стадии продолжения цепи. Так особенно медленно реагируют по радикальному механизму изоолефины и стирол, промежуточныерадикалы которых сильно стабилизованы за счет эффектов сопряжения и сверхсопряжения.
|
|
|
Особое внимание привлекает винильная полимеризация.
Эта реакция была предметом многих теоретических исследований и изучения механизма главным образом вследствие технического значения тех полимеров, которые образуются в ходе полимеризации. Подобно другим рассмотренным выше радикальным реакциям, она включает три стадии: инициирование, рост цепи и прекращение реакции (обрыв цепи).
Инициирование:
(1) Образование инициатора Ra∙, например, из пероксидов.

Рост цепи:

Обрыв цепи:

Рост цепи обычно идет очень быстро. Мономерные алканы могут реагировать с кислородом воздуха с образованием пероксидов, которые легко распадаются до соответствующих радикалов, вызывающих автоинициирование и называемых инициаторами. Поэтому для стабилизации мономера при хранении к нему добавляют небольшое количество ингибитора, например хинона. Для последующей полимеризации необходимо добавить достаточное количество радикального инициатора, чтобы «насытить» ингибитор, перед тем как начнется полимеризация. Именно этим объясняется наличие индукционного периода, часто наблюдаемого при проведении процесса полимеризации.
Радикальные инициаторы не являются, строго говоря, катализаторами (хотя их часто именно так и называют), поскольку каждый радикал, инициирующий рост полимерной цепи, необратимо связывается с ней, и в ряде случаев его удается обнаружить в полученном полимере. Эффективность некоторых инициаторов настолько велика, что после определенного индукционного периода каждый радикал вызывает образование полимерной цепи.
Обрыв растущей цепи может произойти вследствие ее столкновения как с инициатором, так и с другой растущей цепью, причем вторая реакция более важна; большая часть инициирующих радикалов расходуется для зарождения цепей. Обрыв цепи может происходить также в результате реакции диспропорционирования между растущими цепями. Отрыв атома водорода возможен при атаке растущей цепью уже сформированного полимера, что приводит к появлению новой точки роста, а, следовательно, к образованию разветвленного продукта:
|
|
|

Степень разветвления оказывает глубокое влияние на физические и механические свойства образующегося полимера.
Свойства полимера в значительной степени зависят также от его средней молекулярной массы, т. е. от средней длины полимерных молекул, которая может варьировать от нескольких мономерных единиц до многих тысяч. Кроме того, важное значение имеет фактический диапазон отклонений длин молекул полимеров от среднего значения. Например, свойства двух полимеров с примерно равной средней молекулярной массой различны, если один из них состоит из молекул, большая часть которых имеет одну и ту же длину, в то время как другой содержит как очень длинные, так и очень короткие молекулы. Длину цепи образующегося полимера можно контролировать. Так, увеличение концентрации инициатора по отношению к концентрации алкена будет приводить к образованию более коротких цепей, так как число растущих цепей увеличится и, следовательно, их обрыв станет более возможным, чем рост цепи.
Инициируемая радикалами полимеризация простейших алкенов, например этена и пропена, идет только в жестких условиях, в том числе при очень высоком давлении, однако многие замещенные алкены мономера полимеризуются легко. К ним относятся, например, СН2=СНСl [полимер – поливинилхлорид (ПВХ) – используют для изготовления водопроводных труб и др.], СН2 = СМеСО2Ме (полимер – полиметилметакрилат, органическое стекло); PhCH=CH2 (полимер – полистирол – используют для изготовления изоляционных материалов), CF2= =CF2 (полимер – тефлон, обладающий чрезвычайно низким коэффициентом трения, высокой химической инертностью и высокой температурой плавления). Свойства полимера можно изменять в чрезвычайно широких пределах путем сополимеризации двух различных мономеров, в ходе которой оба мономера включаются в молекулы полимера поровну или в иных пропорциях; например, многие синтетические каучуки являются сополимерами стирола и бутадиена.
|
|
|
|
|
|


