 |
Модель длинной связи между молекулами воды.
|
|
|
|
НОВЫЙ ВЗГЛЯД НА СТРУКТУРУ И АНОМАЛЬНЫЕ СВОЙСТВА ВОДЫ
А.А.Гришаев, независимый исследователь
Введение.
Считается, что аномальные свойства воды – повышенные температуры плавления и кипения, большая диэлектрическая проницаемость, способность к образованию ассоциатов, и др. – обусловлены наличием т.н. водородных связей между молекулами воды [1-3]. Но что такое водородная связь? Полагают, что атом водорода в молекуле воды, оставаясь химически присоединён к своему атому кислорода, способен образовать слабую связь с атомом кислорода другой молекулы воды. Схематически, такой водородный мостик обозначают
О – Н ××× О,
где штрих означает химическую связь, а троеточие – слабую. Структура льда [1-3], как полагают, построена на таких водородных мостиках. В обычном гексагональном льду (лёд I, при атмосферном давлении) элементарная кристаллическая ячейка имеет тетрагональную симметрию: центральная молекула воды окружена четырьмя соседними молекулами, которые находятся в вершинах тетраэдра. Считается, что на центральную молекулу приходится четыре водородные связи, две из которых порождаются двумя «своими» атомами водорода, а две других – двумя «чужими». Малая плотность льда обусловлена большой длиной водородных мостиков: расстояния между ядрами кислорода составляют 2.76 Ангстрем при длине ОН-связи 0.96 Ангстрем [1].
Разумного объяснения феномена водородной связи не дают ни «электростатическая» модель Полинга, ни метод молекулярных орбиталей (см., например, [4,5]). Объяснение межатомных связей с позиций электростатики нелепо [6] – в согласии с теоремой Ирншоу: «устойчивая статическая конфигурация электрических зарядов невозможна» [7]. Действие этой теоремы распространяется, очевидно, и на совокупности атомов или молекул, в которых электроны представляют размазанными по т.н. электронным облакам. Что же касается метода молекулярных орбиталей, то он ровным счётом ничего не объясняет: он лишь описывает молекулярные соединения – причём, не только существующие, но, с неменьшим успехом, и «не существующие» [8].
|
|
|
Таким образом, в рамках традиционных представлений не находит объяснения феномен длинных связей между молекулами воды – а ведь этими длинными связями во многом определяются аномальные свойства воды, и, практически, полностью определяется структура льда. В данной статье мы предлагаем физическую модель, которая, на наш взгляд, приоткрывает тайну этих длинных связей.
Необходимые предварительные замечания.
Как мы излагали ранее [9], каждый атомарный электрон связан лишь с одним соответствующим ему протоном ядра. Причём, кулоновское взаимодействие не играет здесь никакой роли: атомарная связка «протон-электрон» формируется благодаря попеременным прерываниям квантовых пульсаций на электронной частоте [10] у электрона и протона – из-за чего они вынуждены находиться на определённом расстоянии друг от друга [11]. Поскольку их заряды при этом оказываются в бытии попеременно, то отпадает необходимость в механизме, препятствующем их кулоновскому притяжению – и атомарный электрон не обязан пребывать в орбитальном или ином движении для того, чтобы атомная структура была устойчивой.
Поэтому мы не разделяем ни резерфордовский подход, согласно которому атомарные электроны обращаются вокруг ядра, ни квантово-механический подход, согласно которому они размазаны по электронным облакам. Мы полагаем, что каждый атомарный электрон пребывает в индивидуальной области удержания, в которой на него действует связующий алгоритм. Эта область удержания имеет, по-видимому, шаровую форму и размер, на порядок меньший расстояния от ядра. Мы привели свидетельства [12] о том, что расстояние между электроном и протоном в атомарной связке не увеличивается при появлении у этой связки энергии возбуждения. Т.е., атомный радиус не зависит от того, возбуждён атом или нет – будучи всегда таковым, каков он в основном состоянии.
|
|
|
Химическая же связь, как мы излагали ранее [6], возможна при перекрытии областей удержания двух валентных электронов [9], принадлежащих тому и другому связуемым атомам. Химическая связь представляет собой циклический процесс [6], при котором каждый из этих электронов переключается из состава одного атома в состав другого.
По логике нашей модели химической связи, атом кислорода, имеющий два валентных электрона, может химически присоединить не более двух атомов водорода – причём, в направлениях двух задействованных валентностей кислорода, на периферии получившейся молекулы воды будут находиться два «голых» протона.
Модель длинной связи между молекулами воды.
Длина ОН-связи, т.е. расстояние между ядром кислорода и «голым» протоном, в молекуле водяного пара составляет 0.96 Ангстрем [1]. Эта величина, практически, равна сумме атомных радиусов кислорода и водорода. Длина же водородных связей во льду, т.е. расстояние между ядрами кислорода, составляет 2.76 Ангстрем [1] – что, практически, втрое (!) больше длины ОН-связи. Эта троекратность и подсказала нам версию механизма длинных связей между молекулами воды.
Такая связь, на наш взгляд, осуществляется не через одну группу ОН, как это принято считать, а через две, принадлежащие той и другой связуемым молекулам воды – как это схематически показано на Рис.1. При такой конфигурации существует возможность связки двух молекул воды, если расстояние между «голыми» протонами из задействованных групп ОН как раз равно длине ОН-связи.
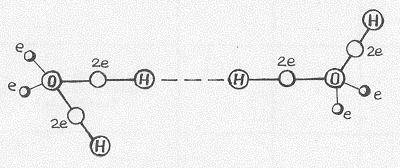
Рис.1
Действительно, в нашей модели химической связи [6], встречные переключения валентных электронов – из состава одного атома в состав другого – упорядочиваются циклическими перебросами кванта возбуждения из одного атома в другой. В условиях теплового равновесия, наиболее вероятная энергия этого кванта соответствует максимуму равновесного спектра, т.е. составляет 5 kT, где k – постоянная Больцмана, T – абсолютная температура. Перебросы кванта возбуждения автоматически управляются Навигатором квантовых перебросов энергии [13]. Роль Навигатора при формировании химической связи подробно описана в [6]. По логике «цифрового» физического мира [14], Навигатор сканирует пространство вокруг возбуждённого атома в поисках атома-адресата, которому может быть переброшена энергия возбуждения: от ядра возбуждённого атома начинает расходиться сферическая «поисковая» волна. У первого же атома, который накрывает эта волна, появляется шанс стать получателем энергии возбуждения. При обычной химической связи, таким получателем оказывается – с вероятностью, близкой к единице – ближайший сосед, поэтому квант возбуждения может неограниченно долго перебрасываться из одного из связуемых атомов в другой, и обратно. Ситуация же, изображённая на Рис.1, несколько иная. Когда в задействованной группе ОН возбуждён атом водорода, то поисковая волна, расходящаяся от его ядра, т.е. от протона, практически одновременно накрывает как ядро атома кислорода из своей группы ОН, так и ядро атома водорода из чужой группы ОН. Поэтому вероятности переброса кванта возбуждения как своему атому кислорода, так и чужому атому водорода – практически одинаковы.Таким образом, существует реальная возможность переброса кванта из одной группы ОН в другую – и поэтому весьма вероятен процесс циклических перемещений кванта «туда-сюда» вдоль всей цепочки О–Н…Н–О. Этот процесс, способный длиться неопределённо долго, и порождает, на наш взгляд, длинную связь между молекулами воды.
|
|
|
Может показаться непривычным, что сам по себе циклический обмен квантом возбуждения у пары атомных групп способен оказывать на эту пару механически стабилизирующее действие. Наверное, особенно непривычно это покажется тем теоретикам, для которых вполне привычна ковалентная связь «на обменной энергии» - т.е. на чисто математическом трюкачестве [6]. Но о том, что вышеизложенная модель длинной связи физична, и что повторяющиеся перебросы кванта возбуждения могут оказывать механическое связующее действие на молекулы, свидетельствует известный эффектный опыт. В кювету с оптически нелинейной жидкостью, например, с нитробензолом, направляют лазерный луч – так, чтобы он проходил параллельно поверхности жидкости на небольшой глубине. Интенсивность лазерного луча должна быть такой, чтобы произошла нелинейная канализация энергии, т.е. чтобы образовался «световод» в жидкости. После этого, с помощью вентилятора обдувают поверхность жидкости, пуская по ней волну. И эта волна заставляет волнообразно изгибаться «световод», по которому идёт лазерный луч!
|
|
|
Не будем упускать из виду, что модель длинной связи кардинально расходится с моделью водородной связи в вопросе о структуре связующего мостика. Согласно модели водородной связи, «на каждой линии кислород-кислород находится только один атом водорода» [1], тогда как модель длинной связи говорит о двух атомах водорода между двумя связуемыми атомами кислорода (см. Рис.1). Какая из этих моделей лучше согласуется с экспериментом, т.е. с результатами структурных исследований?
|
|
|


