 |
Категория «Теоретические основы объемных методов анализа»
|
|
|
|
:: 001:: В 100 мл крови человека содержится примерно 55, 8 мг железа. Сколько это составляет атомов железа?
а) 6 ∙ 1026;
б) 6 ∙ 1017;
в) 10-3;
г) 6 ∙ 1020
:: 002:: Какое значение может принимать фактор эквивалентности HNO3 в кислотно-основных реакциях ионного обмена?
а) ½;
б) 1/5;
в) 1;
г) 1/3.
:: 003:: Какое количество эквивалентов составляют 98 г фосфорной кислоты в реакции образования средней соли?
а) 3;
б) 2;
в) ½;
г) 1.
:: 004:: В какой из приведенных ниже реакций фактор эквивалентности H2SО4 равен 1/8?
а) Н2SО4 + 2КОН = K2SО4 + 2Н2О;
б) H2SО4 + КОН = KHSО4 + Н2О;
в) H2SО4 + Cu = CuSО4 + SO2 + Н2О;
г) H2SО4 + НI = I2 + H2S + Н2О.
:: 005:: Массовая доля NaCI в физиологическом растворе равна 0, 85%. Какую массу NаС1 нужно взять для приготовления 1 кг физиологического раствора?
а) 85 г;
б) 8, 5 г;
в) 0, 85 г;
г) 85 мг.
:: 006:: В качестве первичного стандарта в титриметрическом анализе может быть использовано следующее вещество:
а) КМnО4;
б) Na2B4О7 ∙ 10H2О;
в) I2;
г) NaОН.
:: 007:: Сколько миллилитров 0, 1 М раствора AgNО3 израсходуется на титрование 5мл 0, 2 М раствора NaCL?
а) 5мл;
б) 2, 5мл;
в) 10мл;
г) 100мл.
:: 008:: В методе кислотно-основного титрования стандартными растворами могут быть растворы:
а) NH4ОH;
б) H2SO3;
в) Н3ВО3;
г) NaOH.
:: 009:: В качестве первичных стандартов в методе кислотно-основного титрования используются следующие вещества:
а) Н2С2О3 ∙ 2Н2О;
б) Na2CО3 ∙ 10Н2О;
в) Na2B4О7 ∙ 10Н2О;
г) Na2SО4 ∙ 10H2О.
:: 010:: Из указанных ниже навесок веществ (или объема газа) приготовлено 4 водных раствора объемом 1 л. В каких случаях молярная концентрация эквивалента полученного раствора равна 0, 1 моль/л?
а) 8, 0 г NaOH;
б) 2, 24 л НС1 (н. у. )
в) 5, 9 г H2SО4 (fэкв= 1/2).
г) 6, 6 г КОН.
|
|
|
:: 011:: Концентрацию растворов или количество каких веществ в смеси можно определить методом кислотно-основного титрования?
а) NaCl;
б) Na2CО3;
в) К2Сr2О7;
г) НС1.
:: 012:: Какие факторы определяют выбор индикатора при кислотно-основном титровании?
а) интервал перехода окраски индикатора;
б) зона скачка рН на кривой титрования;
в) рН в точке эквивалентности;
г) объем титруемого раствора.
:: 013:: С какими индикаторами можно титровать раствор аммиака стандартным раствором HNO3?
а) бромфеноловый синий, Δ рН = 3, 0... 4, 6;
б) нейтральный красный, Δ рН = 6, 8... 8, 0;
в) метилоранж, Δ рН = 3, 1... 4, 4;
г) фенолфталеин, Δ рН = 8, 2... 10, 0.
:: 014:: В водных растворах каких солей лакмус (рТ= 7) окрасится в синий цвет?
а) CaCL2;
б) Al2(SО4)3;
в) NaNО3;
г) Na2CО3.
:: 015:: На титрование 10, 0 мл раствора NaOH пошло 12, 0 мл 0, 1000 М раствора НС1. Какие из нижеследующих цифр соответствуют составу исследуемого раствора щелочи?
а) 0, 004800 г/мл;
б) 7, 2 · 1022 молекул NaOH/л;
в) 0, 12 моль/л.
г) 12 г/л.
:: 016:: На титрование 10, 0 мл раствора Н3РО4 в присутствии метилоранжа пошло 5, 0 мл 0, 2 М раствора NaOH. Каковы масса и количество Н3РО4 в 1 л анализируемого раствора?
а) 4, 9 г;
б) 9, 8 г;
в) 0, 05 моль;
г) 0, 1 моль.
:: 017:: В 1 л воды растворили 22, 4 мл газообразного НС1 (н. у. ). Чему равны рН и рОН полученного раствора?
а) рН = 3;
б) рН = 1;
в) рОН = 12;
г) рОН = 13.
:: 018:: Чему равен фактор эквивалентности окислителя в следующих превращениях:
1. Cr2O  → 2Cr3+
2. NO → 2Cr3+
2. NO 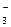 → NO → NO  3. MnО
3. MnО 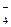 → MnO2
4. BrO → MnO2
4. BrO 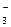 → Br - → Br -
| а) 1/6; б) ½; в) 1/3; г) 1/5. |
:: 019:: Какие исходные вещества используются для стандартизации следующих титрантов:
| 1. KMnO4 2. NaOH 3. Na2S2O3 4. H2SO4 | а) H2C2O4 ∙ 2H2O б) MgSO4 в) K2Cr2O7 г) Na2CO3 |
:: 020:: Какие титранты необходимы для следующих веществ методом прямого титрования:
| 1. Na2C2O4 2. NaCL 3. Na2CO3 ∙ 10H2O 4. Na2S2O3 ∙ 5H2O | а) KMnO4 б) AgNO3 в) HCL г) I2 |
:: 021:: Какие пары титрантов следует использовать при определении следующих веществ методом обратного титрования:
|
|
|
| 1. СаСО3 2. К2Cr2O7 3. Na2SO3 4. NH4CL | а) HCL и NaOH б)I2 и Na2S2O3 в) KMnO4 и FeSO4 г) CH3COH и NH2OH |
:: 022:: Какой индикатор следует использовать для фиксирования точки эквивалентности при титровании:
| 1. Н2О2 раствором KMnO4 в среде H2SO4 2. CH3COOH раствором КОН 3. Йода раствором Na2S2O3 4. Раствора аммиака раствором Н2SO4 | а) индикатор не нужен б) фенолфталеин (рТ 9) в) крахмал г) метилоранж (рТ 4) |
|
|
|


