 |
Адсорбция на границе раздела твердое тело/жидкость
|
|
|
|
Типичные ПАВ имеют асимметрично построенные молекулы, состоящие из двух частей: активной полярной группы, хорошо взаимодействующей с молекулами воды, типа —ОН, —СООН, —NH2, —NO2, —SO3H, —SO3Na, —COONa и др., и неполярной гидрофобной группы – углеводородного радикала.
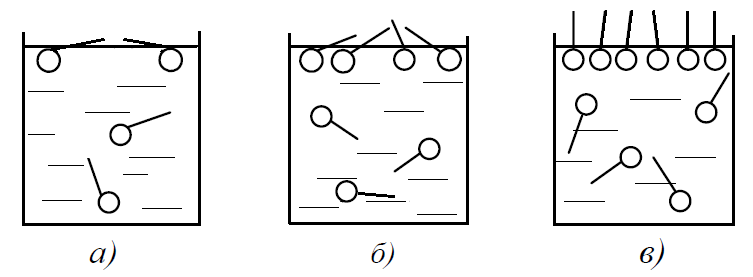
Такие дифильные молекулы, способные взаимодействовать одновременно с полярными и неполярными средами, самопроизвольно концентрируются на границах раздела фаз, снижая энергию Гиббса поверхности и образуя адсорбционный слой определенной структуры. В адсорбционных слоях молекулы ПАВ ориентируются полярными группами в сторону полярной среды (воды), а гидрофобной неполярной частью – в сторону менее полярной фазы (воздуха, углеводородной жидкости, рисунок 8.1). По мере заполнения поверхности раздела вода/воздух молекулами ПАВ поверхностное натяжение на этой границе резко снижается. В разреженных адсорбционных слоях молекулы ПАВ располагаются вдоль поверхности (рисунок 8.1 а, б). Такое расположение молекул ПАВ приводит к наибольшему экранированию молекул воды и обеспечивает минимальное поверхностное натяжение раствора.
С ростом концентрации раствора число молекул ПАВ в адсорбционном слое увеличивается. При некоторой концентрации раствора может образоваться предельно насыщенный адсорбционный слой, так называемый «частокол Лэнгмюра» (рисунок 8.1 в). В этом случае на границе раздела фаз между водным раствором ПАВ и воздухом образуется мономолекулярный адсорбционный слой и поверхность воды оказывается сплошь покрытой углеводородными радикалами молекул ПАВ. Поверхностное натяжение растворов при этих концентрациях приближается к значению поверхностного натяжения индивидуальных ПАВ на границе с воздухом.
|
|
|
|
| Рисунок 8.1 –Схема адсорбции ПАВ на границе раздела раствор/воздух с ростом концентрации ПАВ в растворе |
При введении адсорбентов в водные растворы ПАВ молекулы ПАВ адсорбируются на границе вода/твердая поверхность. Согласно правилу выравнивания полярностей П.А. Ребиндера, при адсорбции ПАВ разность полярностей между адсорбентом и растворителем уменьшается. Все полярные гидрофильные поверхности адсорбируют ПАВ из неполярных и слабополярных жидкостей. Неполярные сорбенты, такие, как уголь или некоторые полимерные материалы, наоборот, хорошо адсорбируют ПАВ из полярных жидкостей.
На адсорбцию ПАВ из растворов оказывает влияние и пористость адсорбента. Влияние пористости определяется соотношением размеров пор и молекул ПАВ. С уменьшением размеров пор адсорбция небольших молекул ПАВ, как правило, возрастает. Это наблюдается в тех случаях, когда молекулы ПАВ имеют размеры, позволяющие проникнуть в поры адсорбента.
По истечении определенного времени в системе адсорбент/водный раствор ПАВ устанавливается равновесие между количествоммолекул ПАВ, перешедших на поверхность сорбента, и их объемной равновесной концентрацией C. Это равновесие может быть описано уравнением Лэнгмюра, при этом емкость монослоя G¥отвечает предельной адсорбции. Для определения величины G¥ лучше использовать уравнение Лэнгмюра в линейной форме:
 . (8.1)
. (8.1)
Графически зависимость 1/G= f (1/ C) выражается прямой, пересекающей ось ординат. Отрезок, отсекаемый от оси ординат, определяет величину, обратную емкости монослоя 1/G∞. Тангенс угла наклона прямой позволяет найти константу адсорбционного равновесия B.
Величину гиббсовской адсорбции Gдля ПАВ обычно рассчитывают, определяя концентрацию раствора до и после адсорбции:
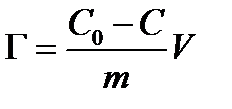 , (8.2)
, (8.2)
где C 0, C — начальная и равновесная концентрации ПАВ в растворе; т. – масса адсорбента; V – объем раствора ПАВ, в который введен адсорбент; G–гиббсовская адсорбция, т.е. избыток вещества в поверхностном слое определенной толщины по сравнению с его количеством в таком же слое в объеме фазы. Этот избыток обычно относят к единице площади поверхности (или к единице массы адсорбента)
|
|
|
Разность концентраций поверхностно-активного вещества (C 0 – C) удобно определять по изменению поверхностного натяжения раствора.
Определив экспериментально емкость монослоя G¥по формуле (8.1), можно рассчитать удельную поверхность адсорбента S yд., т.е. поверхность, приходящуюся на единицу массы адсорбента. Для этого необходимо знать площадь s 0, занимаемую одной молекулой адсорбата в насыщенном адсорбционном слое на границе раздела фаз. Согласно исследованиям Лэнгмюра и Гаркинса, площадь, занимаемая одной молекулой большинства одноосновных жирных кислот и спиртов, составляет 0,2¸0,3 нм 2.
Лабораторная работа 8.1
|
|
|


