 |
На фарм предпр для изготовления таблеток поступили ЛС(изониазид, фтивазид)
|
|
|
|
Примесь изониазида есть. Примесь определяют растворением в воде. Изониазид растворим, фтивазид – нет. К получ воде +NaNO2 = азид
KI + NaNO2 = нет окраски – примесь есть
Примеси нет – есть окрашивание
пр-е пиридина, изоникотиновой к-ты.
Isoniasidum -гидразид изоникотиновой к-ты, Противотуберкул ср-во. Таб, р-р для инъекций. Бел крист пор б/з, горьк вкуса, Тпл 170-174, легко р в воде,к-тах, щел, умер в этаноле.
Phthivazidum - 3-метокси-4-оксибензилиденгидразид изоникотиновой к-ты.
Гидразид – продукт вз-я гидразина с к-ми. Желт крист пор со слаб зап ванилина, б/в, оч мало р в воде, легко в р-рах к-т и щел с усил окраш-я. (неск ат N облад осн св-вами). Обладают способ к таутомерии. УФ изон 266 и 234.
Общие реакции
-пиролиз с карбонатом натрия- обр пиридин (неприят запах).
-цветн р-я с крист лимон к-той и укс ангидр –при нагр обр вишневое окраш
- р-я Цинке-обр-е полиметиновых касителей производных глутаконового альдегида. Фтивазид-желто-бурое окраш, изон – буро-красное окраш.
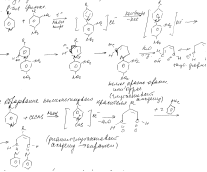
- Как соед-я с третич ат N р-ии с общеалк осадит р-вами.(осадок в цвет реактива)
Изониазид

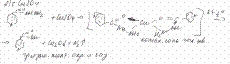
Колич.определение

Р-ль лед укс к-та с добавлением укс аегидридадля ацетилирования препарата.
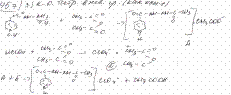
Фтивазид


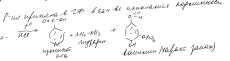

2. Используются ли данные ЛС при скрининге новых ЛВ .
Таргетный скрининг – позв в соотв с выбором гена вести отбор БАВ, в частности АБ с заплан мех-мом д-я в отличие от традиц метода, когда поиск ведется «от клетки к гену». 1 этап скрининга – выделение гена из генома. 2 этап – исп-ся ПЦР для амплифицирования гена (созд-ся вирусный вектор, кот вводится в плазмиду). 3 – кол-во копий гена умножается. 4 –конструируются: а) бесклеточная с-ма, где наработ матрица служит для получения РНК, специфичной для гена; б) бесклеточная рибосомная с-ма, где эта иРНК служит для наработки белк. продукта, кодируемого данным геном.
|
|
|
Для позитивного контроля при скрининге новых ЛС лучше использовать изо-
ниазид, т.к. он действует на все формы микобактерий туберкулеза, проникает
через клеточные мембраны, оказывает терапевтическое действие в кислой среде
и более активен, чем фтивазид. В качестве позитивного контроля можно ис-
пользовать изониазид для характеристики эффективности антимикробных пре-
паратов, сходных по механизму действия с этим веществом.
3. Проанализировав основныве группы вспомогат в-тв укажите их влияние Наполнители – это вещества, используемые для придания таблетке определенной массы в тех случаях, когда лекарственное вещество входит в ее состав в небольшой дозировке (0,01 – 0,001г), обычно сильнодействующее вещество. В качестве наполнителей применяют сахарозу, лактозу, глюкозы, натрия хлорид, крахмал, натрия гидрокарбонат и др. Наполнители, обладающие хорошей сыпучестью и прессуемостью, используются для прямого прессования. Они не являются инертными формообразователями, а в значительной степени определяют скорость высвобождения, скорость и полноту всасывания лекарственного вещества, а также его стабильность.
Разрыхлители – вводят в состав таблетируемых масс с целью обеспечения их быстрого механического разрушения в жидкой среде (воде или желудочном соке), что необходимо для высвобождения и последующего всасывания лекарственного вещества. По механизму действия их можно подразделить на следующие группы: а) вещества, разрывающие таблетку после набухания при контакте с жидкостью; б) улучшающие смачиваемость и водопроницаемость таблетки и способствующие ее распадению и растворению; в) обеспечивающие разрушение таблетки в жидкой среде в результате газообразования.
К веществам, обладающим способностью к набуханию в жидкой среде, относятся кислота альгиновая (ПС из бурых морских водорослей) и натриевая соль ее, амилопектин, МЦ, натриевая соль карбоксиметилцеллюлозы, агар-агар (ПС из багряных морских водорослей), трагакант, ПВП.
|
|
|
К веществам, улучшающим смачиваемость, относятся неионогенные поверхностно-активные вещества – твины. Твины способствуют образованию гидрофильных пор в таблетке, по которым вода или пищеварительные соки проникают внутрь таблетки. Твин-80 обладает резко выраженной гидрофильностью и добавленный в небольшом количестве (0,2% от общей массы таблетки) приводит к уменьшению времени распадаемости и ускорению, всасывания некоторых лекарственных веществ. К этой же группе разрыхляющих веществ относят крахмал, действие которых обусловлено не столько набуханием зерен, сколько увеличением пористости таблеток и созданием условий для проникновения в них жидкости.
Связывающие вещества вводятся в сухом виде или в гранулирующем растворе в состав масс для таблетирования при гранулировании для обеспечения прочности гранул и таблеток. С увеличением концентрации раствора связывающих веществ ухудшается распадаемость таблеток и скорость высвобождения лекарственного вещества. Это относится к крахмальный клейстер, Na КМЦ, полиэтиленоксид и желатин. Увеличение ПВП, альгинат натрия количества улучшает высвобождение лекарственного вещества.
Вещества, способствующие скольжению. По своей природе скользящие вещества можно разбить на две группы: а) жиры и жироподобные вещества; б) порошковидные вещества. По своим функциям скользящие вещества делятся на 3 группы: обеспечивающие скольжение, смазывающие и препятствующие прилипанию. Они обеспечивают равномерное истечение таблетируемых масс из бункера в матрицу, что гарантирует точность и постоянство дозировки лекарственного вещества. Смазывающие вещества способствуют облегченному выталкиванию таблеток из матрицы, предотвращая образование царапин на их гранях. Противоприлипающие вещества предотвращают налипание массы на стенки пуансонов и матриц, а также слипание частичек друг с другом.
Поскольку тальк и стеараты являются гидрофобными скользящими веществами, то они затрудняют проникновение пищеварительных жидкостей в пористую структуру таблетки, что ухудшает ее распадаемость. Для таблеток не пролонгированного действия это нежелательно, т.к. при терапевтической дозировке лекарственных веществ медленное высвобождение последних не обеспечит терапевтическую концентрацию их в крови, поэтому снижение содержания скользящих веществ за счет повышения их дисперсности позволяет улучшить качество готовой продукции.
|
|
|
Красители добавляют для улучшения внешнего вида таблеток.
Необходимо: понять и оценить роль особенностей технологии производства, качественного и количественного состава вспомогательных веществ лекарственной формы и многих других факторов в действии лекарственных средств.в большинстве случаев терапевтическая неэквивалентность препаратов, содержащих одни и те же лекарственные вещества, зависит от различий в их биодоступности. Биодоступность -часть от введенной дозы, достигшая системного кровотока без изменения. Абсолютная биодоступность — часть лекарственного препарата, которая достигла системного кровотока вычисляемая как отношение "площади под кривой концентрация препарата–время" (AUC) после введения данным методом к AUC после внутривенного введения. Выражается в процентах. Относительная биодоступность — это величина, определяющая относительную степень всасываниялекарственного вещества из испытуемого препарата по отношению к всасыванию лекарственного вещества из препаратов сравнения. Факторы, влияющие на биодоступность:
-физические свойства лекарственного средства, в частности, гидрофобность, степень диссоциации на ионы, растворимость),-лекарственные формы препарата (немедленное высвобождение, применение вспомогательных веществ, методы производства, измененное — замедленное, удлиненное или длительное высвобождение,-введено ли лекарственное средство натощак или после приема пищи,-различия в течение суток,-скорость опорожнения желудка,-индуцирование/ингибирование другими лекарственными средствами или пищей
|
|
|
-взаимодействие с другими лекарствами (антацидами, алкоголем, никотином),
-взаимодействие с отдельными продуктами питания (грейпфрутовый сок, помело, клюквенный сок).-белки-переносчики, субстрат для белка-переносчика (напр., P-гликопротеин).-состояние желудочно-кишечного тракта, его функция и морфология. Для изучения биодоступности лекарственных средств используют различные методы. Чаще всего проводят сравнительное изучение изменений концентраций лекарственного вещества в исследуемой и стандартной лекарственных формах в плазме крови и/или в моче. Если в качестве стандартной лекарственной формы взять раствор для внутривенного введения (которые обеспечивает 100% биодоступность), то можно определить абсолютную биодоступность.
4. В аптеку обратился педиатр с вопросом о возм изгот ЖЛФ для реб 1 года
ГФ XI. Прик 214, 305, 308
Прописано вво с нерезко выраж гидрофоб св-вами в конц до 3%, поэт готовим сусп в массо-объемн конц-ии. Стабил-т МЦ 1:1. мех-м стабил-го д-я – обр-т мономолекулярный слой, снижает пов натяж на границе раздела фаз. Диполи воды ориентируются вокруг стаб-х ч-ц. суспензию готовят дисперсионным м-дом с использованием прав Дерягина (вва измельч с ж-ю, кот сост ½ от их массы). Этим достигается расклинивающее д-е. прием взмучивания не исп, т.к. он не эффективен. Масса фталазола (1-100, х-120 -àх=1.2 г.)
В ступку отвеш 1,2 фталазола и тщат измельч. Доб 1,2 МЦ (непонятно почему берут равное кол-во, а не в 2 раза меньше по правилу дерягина) изм и смеш. Далее в ступку доб прим 1 мл воды и смеш до обр-я пульпы. Пульпу смывают в отп флакон в неск приемов. Флакон с готовой суспензией укупоривают полиэтиленовой пробкой и закрывают навинчивающейся крышкой. Флакон снабжают основной этикеткой «Внутреннее» и предупредительными надписями: «Перед употреблением взбалтывать», «Беречь от детей», «Сохранять в прохладном месте» и отдельным рецептурным номером.
5. Акцентируйте внимание на организ-экономич аспектах.
Фтивазид и изониазид относятся к ЛС специфического действия (противотуберкулезные). Методич прием расчета- экономико-математический.
1. Определить количество больных туберкулезом,потребляющих эти препараты, по формуле: К = Численность населения * % больных туберкулезом / 100
2. Определить потребность аптеки в препарате за год по формуле:
П = Ср.год.потребность в препарате на 1 больного * К
3.Определить потреб аптеке в препарате за мес. П = Потребность за год / 12
Изониазид входит в список ЖНВЛС
Отпуск по рецептам Бланк №107 дейст 2 мес, не хранят
ФОРМА N 148-1/у-04 (лN 148-1/у-06 (л) ЛС, отпускаемые БЕСПЛАТНО и на ЛЬГОТНЫХ условиях (действ до 1 (3) мес, хранятся 5 лет).
|
|
|
Рецепты на бесплатный и льготный отпуск таксируются по полной стоимости, несмотря на то, что больной ничего не платит за препарат или оплачивает только 50% его стоимости. После таксировки рецепт оплачивается больным и регистрируется провизором-технологом в рецептурном журнале. Рецепты хранятся в отдельном шкафу в специально выделенной комнате в подшитом и сгруппированном по датам, месяцам и годам виде. Здесь же хранятся сводные ведомости льготных рецептов, по которым были отпущены ЛС, по группам населения и категориям заболевания
6.На фарм предпр поступило сырье Листья брусники для изгот мочег сбора. Брусника – Vaccinum vitis idaea. Folia Vitis idaea. Vaccinaceae – брусничные. Мочегонное ср-во. Исп водные отвары при мочекам б-ни, подагре, сбор Бруснивер. Мочег сбор.
Гр фенол соед и их гликозидов. Хим сост арбутин, гидрохинон, галловая, эллаг к-та -дуб в-ва, флав, урсоловая к-та.
 Качественные реакции:
Качественные реакции:
0,5 г сырья + 10мл воды кипятят, охлаждают, фильтруют.
А). Извлечение + железоаммонийные квасцы --- зеленовато-черное окраш (дубил в-ва)Б). 1мл фильтрата + 4мл аммиака + 10% 1мл натрия фосфорно-молибденового кислого + 10% HCl --- синяя окраска.(арбутин)
Хроматографирование в уксусной кислоте 5%. Хроматограмму обрабатывают реактивом Паули --- арбутин в виде красного пятна.
Количественное определение
Арбутина-Иодометрическое титрование
| Подготовка | измельчение ЛРС, взятие точной навески | для лучшей экстракции арбутина |
| Экстракция | водой при нагревании | хорошо р-м в воде |
| Очистка | (CH3COO) 2Pb | ↓ дуб.в-в и отделение осадка |
| КО | H2SO4+ Zn пыль титр-е J2 с крахмалом до синего цвета | окисление арбутина |
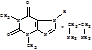 (эуфиллин)
На воздухе поглощает углекислоту, при этом растворимость уменьшается
Произв пурина (пиримидин+имидазол), соль теофиллина с этилендиамином. Теоф – 1,3-диметилксантин. Euphillinum. Спазмолитик и диуретик. Порошок, таб, р-р д/инъ. Бел крист пор со слаб аммиачным зап. Хар Тпл, Спектры УФ и ИК. Раств в воде. Раств в разв р-рах к-т и щел. Водн р-ры имеют щел р-ю.
Подлинность: Мурексидная проба. Окислительно-гидролитич разлож-е до пр-х пиримидина. Разруш молек пурина при нагр с ок-лем (Н2О2 и аммиак) до обр-я смеси метилированных пр-х аллоксана и диалуровой к-ты. Вз-я м/у собой, они образ-т метилир-е пр-е аллоксантина, кот под д-м изб р-ра аммиака приобр пурпурно-красное окраш-е, исчез при доб неск кап NaOH.
Мурексидная проба (окисление в кислой среде с разрушением имидазольного цикла):
(эуфиллин)
На воздухе поглощает углекислоту, при этом растворимость уменьшается
Произв пурина (пиримидин+имидазол), соль теофиллина с этилендиамином. Теоф – 1,3-диметилксантин. Euphillinum. Спазмолитик и диуретик. Порошок, таб, р-р д/инъ. Бел крист пор со слаб аммиачным зап. Хар Тпл, Спектры УФ и ИК. Раств в воде. Раств в разв р-рах к-т и щел. Водн р-ры имеют щел р-ю.
Подлинность: Мурексидная проба. Окислительно-гидролитич разлож-е до пр-х пиримидина. Разруш молек пурина при нагр с ок-лем (Н2О2 и аммиак) до обр-я смеси метилированных пр-х аллоксана и диалуровой к-ты. Вз-я м/у собой, они образ-т метилир-е пр-е аллоксантина, кот под д-м изб р-ра аммиака приобр пурпурно-красное окраш-е, исчез при доб неск кап NaOH.
Мурексидная проба (окисление в кислой среде с разрушением имидазольного цикла):
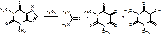
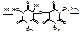
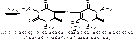 пурпурно-красное окрашивание
-tпл осадка теофиллина
пурпурно-красное окрашивание
-tпл осадка теофиллина
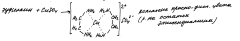 Количественное определение:
КО этилендиамина
1. Ацидиметрия
ЭДА + 2HCl = ЭДА •2HCl
f=1/2, индикатор МО
КО теофиллина
2. Косвенная нейтрализация.
Количественное определение:
КО этилендиамина
1. Ацидиметрия
ЭДА + 2HCl = ЭДА •2HCl
f=1/2, индикатор МО
КО теофиллина
2. Косвенная нейтрализация.
 HNO3+NaON=NaNO3+H2O
3. КО титрование в неводной среде. Протофильный растворитель-диметилформамид HCON (CH3)2. Титрант метилат натрия.
3. Иногда, при проведении курса терапии, некоторые ЛС требуют проведения мониторинга.
4. В таблет цеху на подгот этапе порошок ЛС подвергали измельчению
HNO3+NaON=NaNO3+H2O
3. КО титрование в неводной среде. Протофильный растворитель-диметилформамид HCON (CH3)2. Титрант метилат натрия.
3. Иногда, при проведении курса терапии, некоторые ЛС требуют проведения мониторинга.
4. В таблет цеху на подгот этапе порошок ЛС подвергали измельчению





 5. В аптеку часто поступ рец на изгот порошков
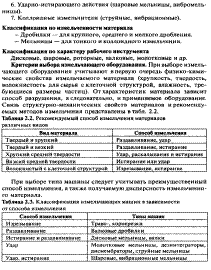
Euphyllinum
ЛС должно изготавл в асептич условиях.
Порошок эуфиллина с сахаром готовят в асептич условиях в соотв с требованием ГФ. При этом замена сахара в порошках на глюкозу запрещено. Это связано с тем, что пор эуфилина с глюкозой не подлежат длит хран-ю, отсыревание нач-ся ч/з 2-6 дней и сопровожд пожелтением порошков. ВАЗ можно по прописи 173 приказ 214.
ВАЗ должна пройти полный качественный и количественный анализ, изготовл в асептических условиях.
6. Акцентируйте внимание на организ-эконом аспектах.
Документ оформление ВАЗ: 1.ЖУРНАЛ РЕГИСТРАЦИИ РЕЗУЛЬТАТОВ ОРГАНОЛЕПТИЧЕСКОГО, ФИЗИЧЕСКОГО И ХИМИЧЕСКОГО КОНТРОЛЯ ВНУТРИАПТЕЧНОЙ ЗАГОТОВКИ, ЛЕКАРСТВЕННЫХ ФОРМ, ИЗГОТОВЛЕННЫХ ПО ИНДИВИДУАЛЬНЫМ РЕЦЕПТАМ (ТРЕБОВАНИЯМ ЛЕЧЕБНЫХ УЧРЕЖДЕНИЙ), КОНЦЕНТРАТОВ, ПОЛУФАБРИКАТОВ, ТРИТУРАЦИЙ, СПИРТА ЭТИЛОВОГО И ФАСОВКИ
2. Журнал учета лабораторных и фасовочных работ.
Формирование розничной цены:
1 ЭТАП. Определить стоимость выданного в работу товара (ЛС + посуда) по формуле: С = Розничная цена (ЛС,посуды) * Количество (ЛС,посуды)
1.1.Для ингредиента
1.2. Для посуды
1.3. Итого стоимость выданного в работу товара(ингредиенты+посуда)
Ст = С1 + С2 +... + Сn
2 ЭТАП. Определить цену единицы готовой продукции(округление до 0.01 руб.)
2.1. Без учета тарифа за изготовление: Ц1 = Ст / Кол-во ед.фасовки
2.2. С учетом тарифа за изготовление: Ц2 = Ц1 + Т1 + Т2, где
Т1 - тариф за изготовление единицы ВАЗ с 1-3 ингредиентами,
Т2 - тариф за каждый последующий ингредиент (после 3-х),
3 ЭТАП. Определить общую стоимость готовой продукции по формуле:
С = Ц2 * Кол-во ед.готовой продукции
4 ЭТАП. Определить сумму дооценки (уценки) при лабораторно-фасовочных работах по формуле: Д = С - Ст
РЦ= Стоим лек ингрид+Стоим аптеч пос, стоим вспомогат мат+ тарифа на изгот+сумма налога на доб стоим, рассчитан от налоговой базы
Суммарная разница в стоимости продукции до оценка (если продажная стоимость изготовленной продукции выше продажной стоимости использованного сырья) или уценка (если продажная стоимость изготовленной продукции ниже использованных субстанций) отражается в «Справке о дооценке и уценке по лабораторным и фасовочным работам»
Дооценка возникает за счет округления цены гот прод в сторону увелич стоимости
Стоимость дооценки в конце меяца отраж в приходной части ТО, а уценка – в расходной. Дооценка относится к приходным товарным операциям. Уценка относится к прочему докум расходу товаров.
Каждая серия ВАЗ подвергается качественному и количеств анализу (полный хим контроль)
5. В аптеку часто поступ рец на изгот порошков
Euphyllinum
ЛС должно изготавл в асептич условиях.
Порошок эуфиллина с сахаром готовят в асептич условиях в соотв с требованием ГФ. При этом замена сахара в порошках на глюкозу запрещено. Это связано с тем, что пор эуфилина с глюкозой не подлежат длит хран-ю, отсыревание нач-ся ч/з 2-6 дней и сопровожд пожелтением порошков. ВАЗ можно по прописи 173 приказ 214.
ВАЗ должна пройти полный качественный и количественный анализ, изготовл в асептических условиях.
6. Акцентируйте внимание на организ-эконом аспектах.
Документ оформление ВАЗ: 1.ЖУРНАЛ РЕГИСТРАЦИИ РЕЗУЛЬТАТОВ ОРГАНОЛЕПТИЧЕСКОГО, ФИЗИЧЕСКОГО И ХИМИЧЕСКОГО КОНТРОЛЯ ВНУТРИАПТЕЧНОЙ ЗАГОТОВКИ, ЛЕКАРСТВЕННЫХ ФОРМ, ИЗГОТОВЛЕННЫХ ПО ИНДИВИДУАЛЬНЫМ РЕЦЕПТАМ (ТРЕБОВАНИЯМ ЛЕЧЕБНЫХ УЧРЕЖДЕНИЙ), КОНЦЕНТРАТОВ, ПОЛУФАБРИКАТОВ, ТРИТУРАЦИЙ, СПИРТА ЭТИЛОВОГО И ФАСОВКИ
2. Журнал учета лабораторных и фасовочных работ.
Формирование розничной цены:
1 ЭТАП. Определить стоимость выданного в работу товара (ЛС + посуда) по формуле: С = Розничная цена (ЛС,посуды) * Количество (ЛС,посуды)
1.1.Для ингредиента
1.2. Для посуды
1.3. Итого стоимость выданного в работу товара(ингредиенты+посуда)
Ст = С1 + С2 +... + Сn
2 ЭТАП. Определить цену единицы готовой продукции(округление до 0.01 руб.)
2.1. Без учета тарифа за изготовление: Ц1 = Ст / Кол-во ед.фасовки
2.2. С учетом тарифа за изготовление: Ц2 = Ц1 + Т1 + Т2, где
Т1 - тариф за изготовление единицы ВАЗ с 1-3 ингредиентами,
Т2 - тариф за каждый последующий ингредиент (после 3-х),
3 ЭТАП. Определить общую стоимость готовой продукции по формуле:
С = Ц2 * Кол-во ед.готовой продукции
4 ЭТАП. Определить сумму дооценки (уценки) при лабораторно-фасовочных работах по формуле: Д = С - Ст
РЦ= Стоим лек ингрид+Стоим аптеч пос, стоим вспомогат мат+ тарифа на изгот+сумма налога на доб стоим, рассчитан от налоговой базы
Суммарная разница в стоимости продукции до оценка (если продажная стоимость изготовленной продукции выше продажной стоимости использованного сырья) или уценка (если продажная стоимость изготовленной продукции ниже использованных субстанций) отражается в «Справке о дооценке и уценке по лабораторным и фасовочным работам»
Дооценка возникает за счет округления цены гот прод в сторону увелич стоимости
Стоимость дооценки в конце меяца отраж в приходной части ТО, а уценка – в расходной. Дооценка относится к приходным товарным операциям. Уценка относится к прочему докум расходу товаров.
Каждая серия ВАЗ подвергается качественному и количеств анализу (полный хим контроль)
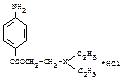 (новокаин)
Novocainum, β-диэтиламиноэтилового эфира п-аминобензойной к-ты гидрохлорид. Местноанестезир ср-во. Прим для спинно-мозговой и инфильтрац анестезии в виде 0,25-0,5 % р-ров, порош.
Произв ароматич к-т.Соль органич осн-я и мин к-ты. Б/ц крист или бел крист пор б/з, горького вкуса. Вызыв на языке чувство онемения. Характ спектр УФ, ИК. Оч легко р в воде, легко р в спирте, мало в хлороф.
Основн св-ва. Р-я на незам первич аром аминогр – обр-е азокрасителя (действуем NaNO2 в кисл среде----соль диахзония, а потом доб щелочной в-нафтол).
Р-я среды солиновокаина кислая, а при д-и щел выдел орг осн-е новокаина, нераств в воде (б/ц маслянистые капли) и NaCl+H2O
Обр соли с общеалк осадит реакт: к-та пикр, к-та фосфорно-вольфрамовая
При д-ии на р-р Новок р-р перманг калия обесцвеч-ся. (новокаин окисляется)
(новокаин)
Novocainum, β-диэтиламиноэтилового эфира п-аминобензойной к-ты гидрохлорид. Местноанестезир ср-во. Прим для спинно-мозговой и инфильтрац анестезии в виде 0,25-0,5 % р-ров, порош.
Произв ароматич к-т.Соль органич осн-я и мин к-ты. Б/ц крист или бел крист пор б/з, горького вкуса. Вызыв на языке чувство онемения. Характ спектр УФ, ИК. Оч легко р в воде, легко р в спирте, мало в хлороф.
Основн св-ва. Р-я на незам первич аром аминогр – обр-е азокрасителя (действуем NaNO2 в кисл среде----соль диахзония, а потом доб щелочной в-нафтол).
Р-я среды солиновокаина кислая, а при д-и щел выдел орг осн-е новокаина, нераств в воде (б/ц маслянистые капли) и NaCl+H2O
Обр соли с общеалк осадит реакт: к-та пикр, к-та фосфорно-вольфрамовая
При д-ии на р-р Новок р-р перманг калия обесцвеч-ся. (новокаин окисляется)
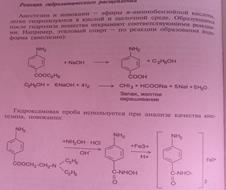 КО нитритометрия по первич аминогр.
Т-натрия нитрит, титруют медл, т к обр-е соли диазония идет во времени. В реакц среду для стабил доб KBr, так как хлориды менее устойчивы. Инд тропеолин ОО или йодкрахм бум, либо потенциометрически.
В ТЭ на йодкрахм бум выд йод, кот кот окраш крахм в син цвет.
2KJ+2NaNO2+2H2SO4=>J2+2NO+K2SO4 +Na2SO4+2H2O
М опред м-дом нейтрал по связ HCl. Возможно аргентометрич опр по хлорид-иону.
2-3. Дайте хар-ку разл видам стабилизации растворов для иньекций.
Теория ОВ процессов: прикладная теория Баха и Энглера. Первичный процесс окисления:
Факторы, влияющие на устойчивость ЛС:
- физико-хим св-ва ЛВ
-чистота ЛВ и растворителей
-значение рн водного р-ра
-температура
-наличие тяж.Ме
-наличие кислорода(в возд над раствором и в самом растворе)
-надлежащие условия хранения и упаковка
- класс и марка стекла флакона.
Инъ р-ры д облад стабил-ю. Это обусл тем, что в проц изгот инъ р-ров, особ при термич стерил-ии) и послед хран возм разлож нек ЛВ. Это вызывает необх стабил-ии инъ р-ров. Если р-ры не стабил, то в них м появ муть, осадок, изм цв.
Соль гидролиз-ся с обр-м слабодисс осн-я и сильнодисс к-ты, т е образ ионы гидросония ОН3+. Это усил-ся при стерил-ии. Прибавление к этим р-рам своб к-ты пониж степень диссоц-ии воды и одавл-т гидролиз, вызывая сдвиг равновесия влево. Нагрев-е р-ра во время стерил-ии увел степ диссоц воды и повыш рН р-ра за счет выщелач-я стекла, вызыв в значит степ усил-е гидролиза соли, что приводит к накопл в р-ре труднораств азотистого осн-я. Новокаин сод сложноэф группы, при нагр происх омыление слож эфира, сопров измен фармакол д-я. После стерил-ии р-ра Новок появл своб ПАБК, благ чему рН р-ра смещ в кисл стор.
Для высококонц р-ров Новок (5,10,20%) доб HCl оказ недост, т.к. в проц стерил-ии происх интенс ок-е Новок-на. Поэт исп антиоксиданты (Na, К метабисульфит, к-та лимонная. рН р-ра 3,8-4.5. хр 30 дней.
СХЕМА ГИДРОЛИЗА СОЛИ СЛАБОГО ОСНОВАНИЯ И СИЛЬНОЙ КИСЛОТЫ
Схема гидролиза
ВА+ HOH ↔ВOH + Н+ +А-
где: ВА – гидролизующееся вещество;
ВOH – слабодиссоциируемое основание.
Растворы новокаина стабилизируют 0,1 М раствором кислоты хлористоводородной для создания рН 3,8– 4,5 (ГФ Х), количество которой зависит от концентрации новокаина в растворе.
4.Акцентируйте внимание на организационно-экономических аспектах.
При обнаружении боя, порчи товара, в присутствии представителя поставщика составляется акт об установлении расхождения по количеству и качеству при приемке товарно-материальных ценностей. Акт подписывается представителями с обеих сторон. На основании этого акта аптека списывает товар в своей программе. Также составл рекламация в электронном виде. В товарной накладной при приемке товара необходимо также пометить, какое количество товара испорчено.
Учет движения товаров (включая рецептурную и материальную посуду, коробки) осуществляется в аптеке только в стоимостном выражении по продажной стоимости. Медикаменты ПКУ учитываются обособленно в количественном выражении в журнале учета ядовитых, наркотических,дефицитных медикаментов и этилового спирта по форме N 10-АП.
Зав.аптекой ведет учет товаров в регистре (ведомости), который является одновременно и товарным отчетом по форме N 25-АП.Отчет составляется в 2 экземплярах. Основным документом, служащим основанием для записей в приходной части отчета, является счет или накладная поставщика, по которым товары и другие ценности поступили в аптеку и приняты Аптекой.Все графы приходной части отчета заполняются по каждому счету, накладной в отдельности.
5. Назовите факторы влияющие на кач-во высушенного ЛРС.
Лекарственное растительное сырье должно храниться в сухом, хорошо вентилируемом помещении в плотно закрытой таре: в аптеках — стеклянной, металлической посуде, в ящиках с крышкой, на складах — в тюках или закрытых ящиках на стеллажах. Резаное сырье хранят в тканевых мешках, порошки — в двойных мешках (внутренний должен быть бумажным, многослойным, наружный — тканевым; возможна картонная упаковка.
В зависимости от физико-химических свойств лекарственного растительного сырья допускается упаковка из полимерных материалов.
Лекарственное растительное сырье, содержащее эфирные масла, хранят изолированно в хорошо укупоренной таре.
Некоторые гигроскопические травы, листья и плоды необходимо хранить в стеклянной или металлической таре хорошо укупоренными (например, листья наперстянки, почечный чай и др.).
При хранении высушенных сочных плодов для предотвращения порчи их амбарными вредителями рекомендуется помещать в ящики с плодами флакон с хлороформом, в пробку которого вставлена трубочка для выхода паров хлороформа. Хлороформ добавляют по мере его улетучивания.
Готовые лекарственные растительные сборы хранят в аптеках и на аптечных складах с соблюдением вышеуказанных общих правил.
Лекарственное растительное сырье должно подвергаться периодическому контролю в соответствии с требованиями ГФ. Трава, корни, корневища, семена, плоды, утратившие нормальную окраску, запах и требуемое количество действующих веществ, а также пораженные плесенью, амбарными вредителями в зависимости от степени поражения либо бракуют, либо после переработки и дополнительного контроля используют.
Особое внимание при хранении следует уделить лекарственному растительному сырью, содержащему сердечные гликозиды.
Для них ГФ установлены более строгие сроки хранения и повторного контроля на содержание биологической активности.
Ядовитое и сильнодействующее лекарственное растительное сырье хранят в отдельном помещении или отдельном шкафу, сейфе под замком.На окнах д б метал решетки, двери также обивают Ме.
Основные факт, влия на ЛРС – внешние: гигиенические (влажность, Т, свет) и природно-климат(время года, зональность); внутренние – физ-хим процессы, протекающ в ЛРС.
Влажность – повыш: самонагревание, заплесневение, слеживание, гниение, сниж сод ДВ, особ для гигроскоп видов (боярышник, белены, крас)
Растения
1)эфирные масла-мята перечная Mentha piperita L.,Folia Menthae piperitae,Lamiaceae(Яснотковые).Хим состав:ментол,ментон,каротин, флавоноиды, урсоловая и олеаноловая кислоты, каротин, гесперидин, бетаин, стеролы. Выделены также азулены, полифенолы, антоцианы и лейкоантоцианы, микроэлементы (медь, марганец, стронций и др.).Препараты- Лист мяты перечной, настои, сборы, мятное масло, ароматная мятная вода, настойка, комплексные препараты ("Валидол", "Корвалол", капли Зеленина, "Валокордин"), ментол, брикеты, мятные таблетки и др Применение-спазмолитическое.улучшает пищеварение,в составе серд-сосуд препаратов,каплях от насморка.
2)Серд.гликозиды- Н. крупноцв – D. grandiflora, Сем-во норичниковые – Scrophulariaceae. Листья наперстянки – Folia Digitalis.ХС: карденолиды. Первичные гликозиды-пурпуреагликозиды А,В и глюкогиталоксин.Препараты-Порошок листьев.сух.эктракт,настой,дигитоксин.кордигит.Кардиотоническое действие
3) Белена чёрная – Hyoscyamus Niger.Семейство паслёновые – Solanaceae.
Лист белены – Folium Hyoscyami. Алкалоиды тропанового ряда, гиосциамин, скополамин; + в-ва гликозидной природы – гиосципикрин, тиосперин, гиоспирезин. Семена содержат жирное масло.
4) Шиповник собачий – Rosa Canina L.Шиповник майский – Rosa Majalis Herrm.
Шиповник иглистый – Rosa acicularis Семейство розоцветные – Rosaceae.
Плоды шиповника – Fructus Rosae. Витамины: аскорбиновая кислота (2-10%), каротин, филлохинон, флавоноиды (витамин Р), рибофлавин, токоферолы, жирное масло, сахара, пектиновые и др. в-ва.
6.Сегодня уже существует и работает система поиска антимикробных агентов
Таргетный скрининг позволяет в соответствии с выбором гена отбирать биологически активные вещества с запланированным механизмом действия (в отличие от традиционного метода, когда поиск ведется «от клетки к гену»).
Первый этап таргетного скрининга - это выделение данного гена (соответствующего фрагмента ДНК) из генома. Затем фрагмент ДНК амплифицируется (создается вирусный вектор, который вводится в плазмиду) -количество копий гена умножается. Затем конструируются:
- бесклеточная система, где наработанная матрица служит для получения информационной РНК, специфичной для гена;
- бесклеточная рибосомная система, где эта информационная РНК служит для наработки белкового продукта, кодируемого данным геном.
Бесклеточная система, используемая для первичного отбора и оценки активности потенциальных лекарственных веществ - ингибиторов фермента (продукта изучаемого гена), содержит фермент и его субстрат. Когда наработан белок, возникает вопрос: как узнать функцию этого белка? Существует несколько способов:
- если наработанный белок схож с белком из «модельного» организма, то подобрать бесклеточную систему несложно;
- если сходство есть, но не очень близкое, то прибегают к анализу «мотивов» - коротких участков аминокислотной последовательности, которые распределены по всей длине белковой цепи и могут оказаться сходными у двух белков;
- если сходства не существует, то устанавливают, с какими белками он (наработанный белок) контранскрибируется (переписывается в последовательность матричной информационной РНК).
Таким образом можно проводить серийные испытания потенциальных ингибиторов функций почти любого из тысяч генов, составляющих геном патогенна и обнаруживать все новые «уязвимые точки» микробной клетки.
.
КО нитритометрия по первич аминогр.
Т-натрия нитрит, титруют медл, т к обр-е соли диазония идет во времени. В реакц среду для стабил доб KBr, так как хлориды менее устойчивы. Инд тропеолин ОО или йодкрахм бум, либо потенциометрически.
В ТЭ на йодкрахм бум выд йод, кот кот окраш крахм в син цвет.
2KJ+2NaNO2+2H2SO4=>J2+2NO+K2SO4 +Na2SO4+2H2O
М опред м-дом нейтрал по связ HCl. Возможно аргентометрич опр по хлорид-иону.
2-3. Дайте хар-ку разл видам стабилизации растворов для иньекций.
Теория ОВ процессов: прикладная теория Баха и Энглера. Первичный процесс окисления:
Факторы, влияющие на устойчивость ЛС:
- физико-хим св-ва ЛВ
-чистота ЛВ и растворителей
-значение рн водного р-ра
-температура
-наличие тяж.Ме
-наличие кислорода(в возд над раствором и в самом растворе)
-надлежащие условия хранения и упаковка
- класс и марка стекла флакона.
Инъ р-ры д облад стабил-ю. Это обусл тем, что в проц изгот инъ р-ров, особ при термич стерил-ии) и послед хран возм разлож нек ЛВ. Это вызывает необх стабил-ии инъ р-ров. Если р-ры не стабил, то в них м появ муть, осадок, изм цв.
Соль гидролиз-ся с обр-м слабодисс осн-я и сильнодисс к-ты, т е образ ионы гидросония ОН3+. Это усил-ся при стерил-ии. Прибавление к этим р-рам своб к-ты пониж степень диссоц-ии воды и одавл-т гидролиз, вызывая сдвиг равновесия влево. Нагрев-е р-ра во время стерил-ии увел степ диссоц воды и повыш рН р-ра за счет выщелач-я стекла, вызыв в значит степ усил-е гидролиза соли, что приводит к накопл в р-ре труднораств азотистого осн-я. Новокаин сод сложноэф группы, при нагр происх омыление слож эфира, сопров измен фармакол д-я. После стерил-ии р-ра Новок появл своб ПАБК, благ чему рН р-ра смещ в кисл стор.
Для высококонц р-ров Новок (5,10,20%) доб HCl оказ недост, т.к. в проц стерил-ии происх интенс ок-е Новок-на. Поэт исп антиоксиданты (Na, К метабисульфит, к-та лимонная. рН р-ра 3,8-4.5. хр 30 дней.
СХЕМА ГИДРОЛИЗА СОЛИ СЛАБОГО ОСНОВАНИЯ И СИЛЬНОЙ КИСЛОТЫ
Схема гидролиза
ВА+ HOH ↔ВOH + Н+ +А-
где: ВА – гидролизующееся вещество;
ВOH – слабодиссоциируемое основание.
Растворы новокаина стабилизируют 0,1 М раствором кислоты хлористоводородной для создания рН 3,8– 4,5 (ГФ Х), количество которой зависит от концентрации новокаина в растворе.
4.Акцентируйте внимание на организационно-экономических аспектах.
При обнаружении боя, порчи товара, в присутствии представителя поставщика составляется акт об установлении расхождения по количеству и качеству при приемке товарно-материальных ценностей. Акт подписывается представителями с обеих сторон. На основании этого акта аптека списывает товар в своей программе. Также составл рекламация в электронном виде. В товарной накладной при приемке товара необходимо также пометить, какое количество товара испорчено.
Учет движения товаров (включая рецептурную и материальную посуду, коробки) осуществляется в аптеке только в стоимостном выражении по продажной стоимости. Медикаменты ПКУ учитываются обособленно в количественном выражении в журнале учета ядовитых, наркотических,дефицитных медикаментов и этилового спирта по форме N 10-АП.
Зав.аптекой ведет учет товаров в регистре (ведомости), который является одновременно и товарным отчетом по форме N 25-АП.Отчет составляется в 2 экземплярах. Основным документом, служащим основанием для записей в приходной части отчета, является счет или накладная поставщика, по которым товары и другие ценности поступили в аптеку и приняты Аптекой.Все графы приходной части отчета заполняются по каждому счету, накладной в отдельности.
5. Назовите факторы влияющие на кач-во высушенного ЛРС.
Лекарственное растительное сырье должно храниться в сухом, хорошо вентилируемом помещении в плотно закрытой таре: в аптеках — стеклянной, металлической посуде, в ящиках с крышкой, на складах — в тюках или закрытых ящиках на стеллажах. Резаное сырье хранят в тканевых мешках, порошки — в двойных мешках (внутренний должен быть бумажным, многослойным, наружный — тканевым; возможна картонная упаковка.
В зависимости от физико-химических свойств лекарственного растительного сырья допускается упаковка из полимерных материалов.
Лекарственное растительное сырье, содержащее эфирные масла, хранят изолированно в хорошо укупоренной таре.
Некоторые гигроскопические травы, листья и плоды необходимо хранить в стеклянной или металлической таре хорошо укупоренными (например, листья наперстянки, почечный чай и др.).
При хранении высушенных сочных плодов для предотвращения порчи их амбарными вредителями рекомендуется помещать в ящики с плодами флакон с хлороформом, в пробку которого вставлена трубочка для выхода паров хлороформа. Хлороформ добавляют по мере его улетучивания.
Готовые лекарственные растительные сборы хранят в аптеках и на аптечных складах с соблюдением вышеуказанных общих правил.
Лекарственное растительное сырье должно подвергаться периодическому контролю в соответствии с требованиями ГФ. Трава, корни, корневища, семена, плоды, утратившие нормальную окраску, запах и требуемое количество действующих веществ, а также пораженные плесенью, амбарными вредителями в зависимости от степени поражения либо бракуют, либо после переработки и дополнительного контроля используют.
Особое внимание при хранении следует уделить лекарственному растительному сырью, содержащему сердечные гликозиды.
Для них ГФ установлены более строгие сроки хранения и повторного контроля на содержание биологической активности.
Ядовитое и сильнодействующее лекарственное растительное сырье хранят в отдельном помещении или отдельном шкафу, сейфе под замком.На окнах д б метал решетки, двери также обивают Ме.
Основные факт, влия на ЛРС – внешние: гигиенические (влажность, Т, свет) и природно-климат(время года, зональность); внутренние – физ-хим процессы, протекающ в ЛРС.
Влажность – повыш: самонагревание, заплесневение, слеживание, гниение, сниж сод ДВ, особ для гигроскоп видов (боярышник, белены, крас)
Растения
1)эфирные масла-мята перечная Mentha piperita L.,Folia Menthae piperitae,Lamiaceae(Яснотковые).Хим состав:ментол,ментон,каротин, флавоноиды, урсоловая и олеаноловая кислоты, каротин, гесперидин, бетаин, стеролы. Выделены также азулены, полифенолы, антоцианы и лейкоантоцианы, микроэлементы (медь, марганец, стронций и др.).Препараты- Лист мяты перечной, настои, сборы, мятное масло, ароматная мятная вода, настойка, комплексные препараты ("Валидол", "Корвалол", капли Зеленина, "Валокордин"), ментол, брикеты, мятные таблетки и др Применение-спазмолитическое.улучшает пищеварение,в составе серд-сосуд препаратов,каплях от насморка.
2)Серд.гликозиды- Н. крупноцв – D. grandiflora, Сем-во норичниковые – Scrophulariaceae. Листья наперстянки – Folia Digitalis.ХС: карденолиды. Первичные гликозиды-пурпуреагликозиды А,В и глюкогиталоксин.Препараты-Порошок листьев.сух.эктракт,настой,дигитоксин.кордигит.Кардиотоническое действие
3) Белена чёрная – Hyoscyamus Niger.Семейство паслёновые – Solanaceae.
Лист белены – Folium Hyoscyami. Алкалоиды тропанового ряда, гиосциамин, скополамин; + в-ва гликозидной природы – гиосципикрин, тиосперин, гиоспирезин. Семена содержат жирное масло.
4) Шиповник собачий – Rosa Canina L.Шиповник майский – Rosa Majalis Herrm.
Шиповник иглистый – Rosa acicularis Семейство розоцветные – Rosaceae.
Плоды шиповника – Fructus Rosae. Витамины: аскорбиновая кислота (2-10%), каротин, филлохинон, флавоноиды (витамин Р), рибофлавин, токоферолы, жирное масло, сахара, пектиновые и др. в-ва.
6.Сегодня уже существует и работает система поиска антимикробных агентов
Таргетный скрининг позволяет в соответствии с выбором гена отбирать биологически активные вещества с запланированным механизмом действия (в отличие от традиционного метода, когда поиск ведется «от клетки к гену»).
Первый этап таргетного скрининга - это выделение данного гена (соответствующего фрагмента ДНК) из генома. Затем фрагмент ДНК амплифицируется (создается вирусный вектор, который вводится в плазмиду) -количество копий гена умножается. Затем конструируются:
- бесклеточная система, где наработанная матрица служит для получения информационной РНК, специфичной для гена;
- бесклеточная рибосомная система, где эта информационная РНК служит для наработки белкового продукта, кодируемого данным геном.
Бесклеточная система, используемая для первичного отбора и оценки активности потенциальных лекарственных веществ - ингибиторов фермента (продукта изучаемого гена), содержит фермент и его субстрат. Когда наработан белок, возникает вопрос: как узнать функцию этого белка? Существует несколько способов:
- если наработанный белок схож с белком из «модельного» организма, то подобрать бесклеточную систему несложно;
- если сходство есть, но не очень близкое, то прибегают к анализу «мотивов» - коротких участков аминокислотной последовательности, которые распределены по всей длине белковой цепи и могут оказаться сходными у двух белков;
- если сходства не существует, то устанавливают, с какими белками он (наработанный белок) контранскрибируется (переписывается в последовательность матричной информационной РНК).
Таким образом можно проводить серийные испытания потенциальных ингибиторов функций почти любого из тысяч генов, составляющих геном патогенна и обнаруживать все новые «уязвимые точки» микробной клетки.
.
|
|
|


