 |
Анализ и Подведение итогов занятия.
|
|
|
|
1.5. Место и время занятия: учебная комната, 2 акад. часа.
1.6. Оснащение занятия: микроскопы, микропрепараты, таблицы.
занятие 2
Представители типа Sarcomastigophora –
паразиты человека. Класс Zoomastigophora
1.1. Значение темы. Знание строения, циклов развития, методов лабораторной диагностики паразитических представителей класса жгутиковых необходимо при выработке оптимальной тактики для профилактики и эффективного лечения заболеваний, которые они вызывают.
1.2. Цель занятия. Общая - изучить особенности строения паразитических жгутиковых, получить представление о циклах развития и характере заболеваний, которые они вызывают.
1.3. Конкретные цели:
1.3.1.Уметь находить на препаратах простейших – лямблию, трипаносому, лейшманию, трихомонаду.
1.3.2.Знать систематику и отличительные черты морфологии у изучаемых паразитических жгутиковых.
1.3.3.Представлять механизм заражения и меры профилактики заболеваний, вызываемых паразитическими жгутиковыми.
1.3.4.Уметь решать задачи КРОК 1.
Основные теоретические сведения
Подцарство - Protozoa (одноклеточные).
Класс – Zoomastigophora (Flagellata - жгутиковые).
Отряд – Protomonadina (Первично-жгутиковые).
Вид – Trypanosoma brucei gambiense, T. Cruzi (трипаносомы),
Leishmania tropica, L. Donovani (Лейшмании).
Отряд – Polimastigina (Многожгутиковые).
Вид – Lamblia intestinalis или Giardia intestinalis (лямблия),
Trichomonas vaginalis, T. hominis, T. buccalis, Т. tenax (трихомонады)
Trypanosoma brucei gambiense (Трипаносома) — паразитическое простейшее, которое имеет вытянутую, плоскую форму, заостренную с двух концов, длина колеблется в пределах 15—30 мкм. В передней части тела начинается короткий жгутик, проходящий вдоль всей клетки, формируя ундулирующую мембрану. В заднем конце клетки жгутик входит в цитоплазму и заканчивается у специфического органоида кинетопласта. Ядро расположено асимметрично (рис. 4 и II Пр).
|
|
|
 Трипаносомы – возбудители африканского трипаносомоза проходят две стадии развития: стадию трипомастиготы и стадию эпимастиготы (рис. 4). У возбудителя американского трипаносомоза описаны еще две стадии – стадия промастиготы и стадия амастиготы (рис. 4 и II Пр).
Трипаносомы – возбудители африканского трипаносомоза проходят две стадии развития: стадию трипомастиготы и стадию эпимастиготы (рис. 4). У возбудителя американского трипаносомоза описаны еще две стадии – стадия промастиготы и стадия амастиготы (рис. 4 и II Пр).


Рис. 325. Trypanosoma brucei: I - начальная форма из крови; II, III - стадии деления. 1 - ядро, 2 -блефаропласт, 3 - базальное зерно жгутика, 4 - ундулирующая мембрана, 5 - жгутик.
 Trypanosoma brucei gambiense и T. b. rhodesiense паразитирует в крови, лимфе, ликворе и тканях спинного мозга. Трипаносомоз природно-очаговое и трансмиссивное заболевание. Природным резервуаром возбудителя являются антилопы, в крови которых обитают трипаносомы, не вызывая при этом болезни (рис. 5). Специфический переносчик возбудителя — кровососущая муха це-це ( Glossina palpalis ) – крупное насекомое, размерами до 14 мм (рис. Х Пр). Поэтому распространение болезни ограничено ареалом ее обитания, то есть районами Африки южнее Сахары.
Trypanosoma brucei gambiense и T. b. rhodesiense паразитирует в крови, лимфе, ликворе и тканях спинного мозга. Трипаносомоз природно-очаговое и трансмиссивное заболевание. Природным резервуаром возбудителя являются антилопы, в крови которых обитают трипаносомы, не вызывая при этом болезни (рис. 5). Специфический переносчик возбудителя — кровососущая муха це-це ( Glossina palpalis ) – крупное насекомое, размерами до 14 мм (рис. Х Пр). Поэтому распространение болезни ограничено ареалом ее обитания, то есть районами Африки южнее Сахары.
В кишках мухи цеце трипаносомы интенсив-но размножаются, мигрируют в слюнные железы, образуя инвазион-ные (метациклические) формы.
 При укусе человека трипаносомы вводятся со слюной мухи в кровь, затем – во внутренние органы и центральную нервную систему, где размножаются, вызывая развитие сонной болезни (трипаносомоз), длительно протекающего тяжелого заболевания человека. Инкубационный период длится 2 - 3 недели, а болезнь протекает в течение 4 -7 недель. На ранних стадиях болезни трипаносомы размножаются в крови и лимфе, проникают в лимфатические узлы, которые увеличиваются.
При укусе человека трипаносомы вводятся со слюной мухи в кровь, затем – во внутренние органы и центральную нервную систему, где размножаются, вызывая развитие сонной болезни (трипаносомоз), длительно протекающего тяжелого заболевания человека. Инкубационный период длится 2 - 3 недели, а болезнь протекает в течение 4 -7 недель. На ранних стадиях болезни трипаносомы размножаются в крови и лимфе, проникают в лимфатические узлы, которые увеличиваются.
На более поздних стадиях трипаносомы попадают в спинномозговую жидкость, спинной и головной мозг. Возникают тяжелые нарушения центральной нервной системы, развивается мышечная слабость, сонливость, депрессия и болезнь очень часто заканчивается смертью.
|
|
|
При сонной болезни поражается ЦНС, развивается менингоэнцефалит, который может привести к гибели по истечении нескольких месяцев или лет.

Рис. 324. Муха це - це Gloccina palpalis (вверху). Больной сонной болезнью на последних стадиях заболевания (внизу).
ПРОФИЛАКТИКА. Раннее выявление, изоляция и лечение больных,а также предупреждение нападения на человека мух цеце и уничтожение их.
Trypanosoma Cruzi является возбудителем тяжелой болезни (трипаносомоз американский или болезнь Чагаса), распространенной в Южной Америке (Бразилия). Возбудитель болезни живет в организме человека в двух стадиях: трипаносомной - в крови и лейшманоподобной - в клетках мышц, сердца, ЦНС. Переносчиком этого возбудителя является «поцелуйный клоп» Triatoma megistus, который живет в стенах жилищ. «Поцелуйным» он называется потому, что, нападая на спящих людей, кусает преимущественно в губы на месте перехода кожи в слизистую оболочку (рис. X Пр). Триатомовые клопы активны ночью. Они кусают человека в область губ и глаз. Во время сосания крови клопы оставляют фекалии и находящиеся на них трипаносомы попадают в ранку. Трипа - носомы проникают с кровью в клетки различных органов. Там они превращаются в безжгутиковую лейшманиальную форму и интенсивно делятся. Затем они превращаются в критидиальную и трипа -носомальную форму. Проникая в кровь, трипаносомы попадают в новые клетки. Часто поражается сердечная мышца, нервная система, поперечно - полосатые мышцы, эндокринная система.
Болезнь Чагаса – тяжелое заболевание, поражающее внутренние органы, сердечную мышцу, головной мозг. Инкубационный период длится от 3 до 7 дней. Часто болеют дети. В некоторых случаях смерть наступает через 2 - 4 недели.
Иногда болезнь может протекать хронически, в зависимости от поражения систем органов. Такое течение болезни длится до 12 лет
Лабораторная диагностика основана на нахождении возбудителя в мазках крови, спинномозговой жидкости больного, а также в пунктатах лимфатических узлов, селезенке, костного мозга. По сравнению с африканской формой болезни число трипаносом в периферической крови значительно меньше, поэтому требуется просматривать большее число препаратов. Также используют серологические реакции: реакции связывания комплемента, агглютинации, флюоресцирующих антител.
|
|
|
А  Б
Б 
 В
В 
ПРОФИЛАКТИКА. Раннее выявление, изоляция и лечение больных. Уничтожение клопов-переносчиков, улучшение санитарно-бытовых условий, способствующих исключению возможности нападения на человека триатомовых клопов.
Leishmania (Лейшмании). Существует несколько видов и подвидов простейших возбудителей кожного лейшманиоза — Leishmaniatropica и висцерального лейшманиоза — Leishmania donovani (в настоящее время выделяют две формы висцерального лейшманиоза: индийский кала-азар и средиземноморский). В жизненном цикле лейшманий различают следующие стадии: безжгутиковая — амастигота и жгутиковая — промастигота (рис. 6 и III Пр).
 Амастигота — это внутриклеточный паразит человека и позвоночных животных, в связи с чем размеры ее очень малы (2,0—5,5 мкм). В клетке содержится относительно крупное ядро, имеется палочковидный кинетопласт, цитоплазма часто вакуолизирована. При кровососании москита амастиготы попадают в кишки насекомого и быстро, в течение нескольких часов, превращаются в промастиготы.
Амастигота — это внутриклеточный паразит человека и позвоночных животных, в связи с чем размеры ее очень малы (2,0—5,5 мкм). В клетке содержится относительно крупное ядро, имеется палочковидный кинетопласт, цитоплазма часто вакуолизирована. При кровососании москита амастиготы попадают в кишки насекомого и быстро, в течение нескольких часов, превращаются в промастиготы.
 Промастигота — более крупная стадия. Клетка имеет веретеновидную форму, ее длина 12—20 мкм, ширина — 1,5—3,5 мкм. Ядро расположено в центре, а кинетопласт в передней части тела. От базального тельца, лежащего вблизи кинетопласта, начинается жгутик, обеспечивающий высокую подвижность. Тело промастиготы ограничивает хорошо развитая трехслойная мембрана.
Промастигота — более крупная стадия. Клетка имеет веретеновидную форму, ее длина 12—20 мкм, ширина — 1,5—3,5 мкм. Ядро расположено в центре, а кинетопласт в передней части тела. От базального тельца, лежащего вблизи кинетопласта, начинается жгутик, обеспечивающий высокую подвижность. Тело промастиготы ограничивает хорошо развитая трехслойная мембрана.
| Рис. 319. Язвы, вызываемые Leishmania tropica (пендинская язва). |
Внутриклеточная форма не имеет жгутиков и называется лейшманиальной. Жгутиковая стадия проходит в организме насекомых (москитов), которые являются переносчиками лейшманий. Заболевания, вызываемые различными видами лейшманий называют лейшманиозами и относят к трансмиссивным с природной очаговостью. Эта группа заболеваний, которые связаны с определенным комплексом природных условий и могут существовать в природе независимо от человека. Наличие очагов этих заболеваний связано с тремя группами организмов:
|
|
|
1) возбудителей заболеваний;
2) хозяев возбудителей (представляющих естественный резервуар
возбудителей заболеваний);
3) переносчиков возбудителей заболеваний.
У человека встречается кожный, висцеральный и кожно-слизистый
лейшманиоз.
 Возбудитель кожного лейшманиоза (Leishmania tropica) был открыт русским ученым П.Д.Боровским в 1898 г. в Ташкенте. Лейшмании очень малы (2 - 8 мкм). Паразитируют в клетках кожи человека, в результате чего образуются длительно не заживающие язвы. Заражение происходит при укусе человека москитом (рис. 320), в слюнных железах которого находятся жгутиковые формы паразита, имеющие удлиненное тело и один жгутик на переднем конце (лептомонадная форма). На поверхности кожи (на открытых частях тела в местах укуса), через 3 - 8 месяцев появляется небольшой бугорок буровато - красного цвета. В это период паразит интенсивно размножается и имеет округлую безжгутиковую форму. На месте бугорка через 3 - 6 месяцев образуется сухая корка, прикрывающая небольшую язву. Заболевание длится около года, после чего язва начинает рубцеваться. Рубцы остаются на всю жизнь, возникает иммунитет к лейшманиозу (рис. 319).
Возбудитель кожного лейшманиоза (Leishmania tropica) был открыт русским ученым П.Д.Боровским в 1898 г. в Ташкенте. Лейшмании очень малы (2 - 8 мкм). Паразитируют в клетках кожи человека, в результате чего образуются длительно не заживающие язвы. Заражение происходит при укусе человека москитом (рис. 320), в слюнных железах которого находятся жгутиковые формы паразита, имеющие удлиненное тело и один жгутик на переднем конце (лептомонадная форма). На поверхности кожи (на открытых частях тела в местах укуса), через 3 - 8 месяцев появляется небольшой бугорок буровато - красного цвета. В это период паразит интенсивно размножается и имеет округлую безжгутиковую форму. На месте бугорка через 3 - 6 месяцев образуется сухая корка, прикрывающая небольшую язву. Заболевание длится около года, после чего язва начинает рубцеваться. Рубцы остаются на всю жизнь, возникает иммунитет к лейшманиозу (рис. 319).
 Рис. 320. Москит Phlebotomw. papatasii (no Смарту).
Рис. 320. Москит Phlebotomw. papatasii (no Смарту).
Заражение москита лейшманиями происходит при питании на больных животных (резервуарных хозяевах - больших песчанках) или человеке. Вместе с кровью лейшмании попадают в пищеварительный тракт москита, где превращаются в жгутиковую форму размножаются и передвигаются в передние отделы пищеварительной системы а далее в хоботок. После этого москит снова способен передать возбудителя незараженным хозяевам (рис 321) 
Рис. 321. Жизненный цикл Leishmania tropica.
Заболевание распространено в Европе, Африке, Азии, Америке, а также в районах Средней Азии и Закавказья. Кожный лейшманиоз называют также болезнью Боровского, пендинской язвой.
Диагноз кожного лейшманиоза ставят при нахождении паразитов в клетках крови, взятых из язвы.
 Б
Б 
Рис. III. Leishmania tropica: А – амастигота, Б – промастигота..
Профилактика связана с защитой от укусов москитов и борьбой с ними и резервуарными хозяевами. Рекомендуют делать прививки.
Возбудители висцерального лейшманиоза (Leishmania donovam) (внутреннего или кала-азар) имеют размеры 2 - 4 мкм (рис 322 ). Резервуарными хозяевами могут быть собаки, волки шакалы. Заражение человека происходит при укусе москита, являющегося переносчиком возбудителя лейшманиоза. Инкубационный период длится от 3 до 5 месяцев. Лейшмании, паразитируя в клетках внутренних органов - в печени, селезенке, костном мозге лимфатических узлах, стенках кишечника -интенсивно в них размножаются. Заболевание сопровождается лихорадкой, анемией, увеличением печени, селезенки, истощением организма. Часто болеют дети. При правильном лечении выздоровление наступает через 2 - 3 месяца. При отсутствии лечения наблюдается высокий процент смертельных исходов (рис. 322)
|
|
|
. 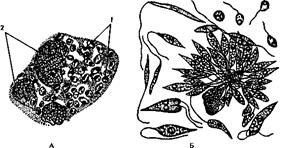
Рис. 322. Leishmania donouani. A - паразиты в клетке хозяина (по Майеру). Б - жгутиковые формы лейшманий в культуре (по Веньону): 1 - лейшмании, 2 - ядро клетки хозяина.
Для постановки диагноза делают пункцию селезенки, лимфатических желез, грудины, биопсию печени.
Висцеральный лейшманиоз распространен в странах Азии, тропической Африки, Португалии, Испании, Италии, а также Средней Азии и Закавказья.
 Профилактика направлена на выявление, лечение и уничтожение животных, больных лейшманиозом, борьбу с москитами и защиту человека от укусов москитов.
Профилактика направлена на выявление, лечение и уничтожение животных, больных лейшманиозом, борьбу с москитами и защиту человека от укусов москитов.
Лабораторная диагностика состоит в микроскопическом изучении отделяемого из язв с целью выявления возбудителя. Кожный лейшманиоз распространен в странах субтропического климата — юг Европы, страны Азии и Центральной Америки.
Природным резервуаром возбудителей висцерального лейш-маниоза (кала-азар или черная болезнь) являются больные люди, а также грызуны и различные представители семейства собачьих, переносчики — москиты. При этой форме поражаются органы ретикулоэндотелиальной системы — селезенка, печень.
Лабораторная диагностика основана на нахождении паразита в крови, мазках-пунктатах из лимфатических узлов и грудины (красный костный мозг), используется также метод культивирования паразита на искусственных средах. Заболевание характерно для жарких стран — Индии, Азии, Африки, Южной Америки, встречается в странах Средиземноморья.
ПРОФИЛАКТИКА сводится к уничтожению бродячих собак, грызунов и переносчиков возбудителя болезни - москитов.
Lamblia intestinalis (Лямблия) — часто встречающийся простейший жгутиковый паразит, обитает в желчном пузыре, желчных ходах и кишечнике человека, вызывая заболевание лямблиоз.
Жизненный цикл лямблии включает:
А) вегетативную стадию — трофозоит и
Б) покоящуюся стадию — цисту (рис. 8 и IV Пр).

 Трофозоит лямблии имеет расширенную кпереди и суженную кзади форму, тело уплощено в дорзо-вентральном направлении, размеры 9—16 мкм. Клетка двусторонне-симметрична. вдоль нее проходят две опорные нити (аксостиль), которые делят цитоплазму на зеркальные половины (все органоиды и ядра у лямблий парные). Функцию движения выполняют четыре пары жгутиков. С помощью электронной микроскопии установлено, что жгутики начинаются внутри цитоплазмы в виде аксонем (внутриклеточные отрезки жгутиков). Основание жгутика крепится к базальному зерну - блефаропласту. Органом фиксации служит присоска, расположенная на вентральной поверхности паразита. Вегетативные формы (трофозоиты) обнаруживаются в содержимом тонкой кишки (рис. IV Пр).
Трофозоит лямблии имеет расширенную кпереди и суженную кзади форму, тело уплощено в дорзо-вентральном направлении, размеры 9—16 мкм. Клетка двусторонне-симметрична. вдоль нее проходят две опорные нити (аксостиль), которые делят цитоплазму на зеркальные половины (все органоиды и ядра у лямблий парные). Функцию движения выполняют четыре пары жгутиков. С помощью электронной микроскопии установлено, что жгутики начинаются внутри цитоплазмы в виде аксонем (внутриклеточные отрезки жгутиков). Основание жгутика крепится к базальному зерну - блефаропласту. Органом фиксации служит присоска, расположенная на вентральной поверхности паразита. Вегетативные формы (трофозоиты) обнаруживаются в содержимом тонкой кишки (рис. IV Пр).
 Б
Б 
Рис. IV. Lamblia intestinalis: А – вегетативная форма, Б – циста.
Цисты лямблий овальной формы, 10—14 мкм в диаметре, имеют 2 или 4 ядра, расположенных у переднего полюса, оболочка хорошо выражена. Инцистирование протекает наиболее интенсивно в нижних отделах кишок. Цисты с испражнениями выделяются в окружающую среду.
Размножаются лямблии в местах наибольшего их скопления путем парного деления. По данным М. М. Соловьева (1963 г.) процесс деления занимает 15 - 20 минут, что способствует интенсивному заселению кишечника простейшими. Во внешнюю среду выделяются с фекалиями в основном в виде цист. Трофозоиты можно обнаружить лишь в жидких фекалиях не более чем у 5% инвазированных лямблиями лиц.
Место паразитирования лямблий - верхние отделы тонкой кишки. К слизистой оболочке лямблия прикрепляется передней частью тела, а задний конец свободный. На одном месте трофозоиты остаются фиксированными непродолжительное время. Они часто открепляются от ворсинок и снова прикрепляются к ним, но уже в другом месте или переходят в свободное состояние. При интенсивной инвазии могут проникать в ткани ворсинок.
Периодически открепляющиеся от слизистой оболочки трофозоиты инцистируются или дегенерируют. Экспериментальными исследованиями на собаках установлено, что через 10 - 15 дней после заражения основная масса трофозоитов локализуется в тощей кишке и изредка в двенадцатиперстной. В дальнейшем популяция лямблий перемещается из проксимальных в средние или в средние и дистальные отделы тонкой кишки. Образование цист (инцистирование) в первые 10-15 дней происходит в тощей кишке, редко - в двенадцатиперстной, а в более поздние сроки - в среднем и дистальном отделах тонкой кишки. Это зависит от численности популяции лямблий, выраженности патологических сдвигов в месте паразитирования и давности инвазионного процесса. Цистовыделение при лямблиозе носит прерывистый характер.
В 1959 г. А. Е. Карапетян получил культуру лямблий in vitro, что позволило более детально изучить особенности биологии простейших. В частности, был установлен характер симбиотический характер взаимоотношений лямблий с грибками рода Candida, что нашло отражение в подходах к лечебной тактике.
Было также установлено, что культура лямблий выдерживает кратковременное замораживание, не теряя способности делиться. В то же время температура воды выше + 50° С вызывает моментальную гибель простейших.
Лямблии относятся к наиболее распространенным паразитам человека, обитающим в верхних отделах тонких кишок. Современные данные о морфологических и биологических особенностях лямблий свидетельствуют об их исключительной приспособленности к обитанию именно в этом участке желудочно-кишечного тракта.
Безуспешные попытки экспериментального заражения животных введением лямблий непосредственно в желчный пузырь (Винников М. Э., 1943 г.; Гнездилов В. Г., 1953 г.; Карапетян А. Е., 1960 г.) и данные о токсичности для лямблий неразведенной желчи (Карапетян А. Е., 1964 г.) убедительно свидетельствуют о невозможности обитания лямблий в желчном пузыре и печени.
Веские доказательства чрезвычайной приспособленности лямблии к обитанию на щеточной кайме эпителия тонких кишок приведены М. М. Соловьевым (1968 г.).
Лямблии обитают на поверхности эпителия. Занос единичных экземпляров в строму ворсинок, установленный Дехкан-Ходжаевой (1960 г.), возможен только при интенсивном заселении лямблиями кишечника. Такие показатели, как отсутствие признаков размножения вегетативных лямблий внутри ворсинки, резких нарушений их структуры и отсутствие реакции окружающей ткани отрицают возможность приспособления этих простейших к внутритканевому паразитированию.
лямблиоз. Лямблиями человек заражается при проглатывании цист вместе с загрязненными продуктами, водой.

Цикл развития лямблий.
Лямблиоз распространен повсеместно. При этом могут возникать нерезкие боли в животе, расстройство стула, снижение аппетита, боли в правом подреберье. Для подтверждения диагноза необходима лабораторная диагностика.Больные жалуются на разлитую болезненность в правой половине подложечной области. Отмечаются резкие приступы болей, сопровождающиеся тошнотой. Частыми являются жалобы на снижение аппетита, отрыжки, изжоги, неустойчивый стул, поносы, сменяющиеся запорами.
Постоянные умеренные боли в области пупка, чаще всего не связанные с едой, чувство переполнения желудка, вздутие живота, жидкий, иногда пенистый стул, до 3 - 5 раз в сутки, стеаторея характерны для энтерита. При осмотре больного - живот умеренно вздут, при глубокой пальпации болезнен в области пупка.
У лиц, инфицированных лямблиями, нередко выявляется гепатобилиарная патология, чаще всего выраженная симптомами холецистита.
Дискинезия желчевыводящих путей, реактивный панкреатит, изменения в печени, желудке, червеобразном отростке имеют рефлекторное происхождение, отягощенное присоединением вторичной инфекции.
Механическое повреждение слизистой оболочки тонкого кишечника и разрушение гликокаликса лямблиями способствует инокуляции условно-патогенной и патогенной микрофлоры с развитием дисбактериоза. Последний проявляется многообразием видового состава микрофлоры и увеличением числа микробных ассоциаций.
Продукты метаболизма и гибели лямблий всасываются из кишечника, вызывают сенсибилизацию организма человека, которая может проявляться различными формами аллергической реакции. Только у 40 - 50% больных лямблиозом отмечается повышенное содержание эозинофилов в крови.
Паразитирование лямблий отягощает течение сопутствующих инфекционных болезней: вирусных гепатитов, брюшного тифа, дизентериии, способствует появлению не свойственных им симптомов и переходу в затяжные формы.
Колонизация слизистой тонкой кишки лямблиями сопровождается выработкой иммунного ответа (AT, комплемента, сенсибилизация иммунокомпетентных клеток), с помощью которого может осуществляться нейтрализация и выведение паразитов из организма. Большую роль в защите хозяина играет местный иммунный ответ, характеризующийся образованием специфических s-IgA. Специфические к антигенам лямблий антитела обнаруживаются также в сыворотках крови инвазированных людей и животных. В настоящее время изучено и охарактеризовано уже более 20 белков лямблий, часть из которых является иммунодоминантными антигенами лямблий. Иммунитет после перенесенного лямблиоза ненапряженный и нестойкий.
Несмотря на активное изучение патогенеза лямблиоза, в научных публикациях все же по-прежнему дискутируется вопрос о патогенности лямблий.
В ряде случаев патогенность лямблий сомнений не вызывает, когда их обнаружение подкрепляется определенной клинической картиной, которая не подтверждается другими причинами.
Доказанной является и патогенная роль лямблий при других заболеваниях желудочно-кишечного тракта, течение которых отягощается при сопутствующем лямблиозе.
Однако регистрируются случаи выявления лямблий при отсутствии патологического процесса, в этих случаях их расценивают как условно-патогенные организмы, степень патогенности которых зависит от ряда факторов, при наличии которых бессимптомное носительство может перейти в болезнь - лямблиоз. К факторам, определяющим возможность такого перехода, относят прежде всего наличие сопутствующих заболеваний, ослабляющих организм носителя, сниженная иммунореактивность, состав паразитоценоза кишечника хозяина, витаминная недостаточность, характер питания, а также массивность заражения лямблиями, а может, и вирулентность простейших (последнее не доказано). Частота манифестного лямблиоза составляет 13 - 43%, субклинического - 49%, бессимптомного - 25 - 28% от числа инвазированных лямблиями.
Лабораторная диагностика. Классическим методом лабораторной диагностики лямблиоза являются протозоологические исследования. Проводится микроскопическое исследование нативных и окрашенных раствором Люголя мазков из свежевыделенных фекалий. Учитывая циклическое выделение цист и трофозоитов с фекалиями, незначительные сроки жизни вегетативных форм во внешней среде, необходимо примененять консервирующие жидкости длясохранения паразита в фекалиях (Сафаралиева, Турдыева, Барроу) и проводить многократные исследования (от 2 - 3 до 6 - 7 раз с интервалами 1-2 дня), а также использовать метод формалин-эфирного обогащения, метод всплывания. В большинстве случаев цисты лямблий в кале обнаруживаются уже при первом исследовании. Отрицательные периоды в выделении лямблий могут колебаться от 2 - 3 суток до 2 - 3 недель. Поэтому при подозрении на лямблиоз можно также рекомендовать проводить протозоологическое исследование кала в течение 4-5 недель с интервалом в одну неделю.
В дуоденальном содержимом трофозоиты лямблий обнаруживаются с большим постоянством, чем в фекалиях. Однако при паразитировании лямблий в средних и дистальных отделах тонкой кишки результаты исследования дуоденального содержимого могут быть отрицательными, поэтому необходимо проводить исследование кала. Исследование секрета двенадцатиперстной кишки, полученного с помощью трехканального зонда в условиях вакуума, более эффективно для обнаружения паразита, чем микроскопия дуоденального содержимого, полученного с помощью обычных зондов.
В последнее время для лабораторного подтвеждения лямблиоза применяют иммунологические методы исследования, основанные на выявлении АГ возбудителя в фекалиях или специфических AT в сыворотке крови. При размножении L. intestinalis в кишечнике в большом количестве продуцируется специфический АГ GSA 65. В фекалиях его определяют методом моноклональных AT. Специфические AT класса IgM можно выявлять в сыворотке крови больного методом ИФА уже на 10 - 14 день от начала инвазии, их наличие в диагностических титрах свидетельствует об остром лямблиозе. Использование ПЦР для обнаружения ДНК лямблий в биологических субстратах является высоко эффективным методом диагностики, но применяется в основном для проведения научных исследований.
ПРОФИЛАКТИКА: выявление больных и их лечение; соблюдение санитарно-гигиенических правил; защита пищевых продуктов от загрязнения; уничтожение мух и других бытовых членистоногих как возможных механических переносчиков цист лямблий.
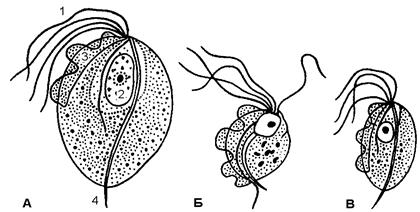 Трихомонады. У человека обитают три вида трихомонад: Trichomonas vaginalis – влагалищная, паразитирующая в мочеполовых путях, Trichomonas hominis – кишечная (в толстом кишечнике)и Trichomonas tenax – ротовая, обитающая в полости рта (рис.9 и V Пр).
Трихомонады. У человека обитают три вида трихомонад: Trichomonas vaginalis – влагалищная, паразитирующая в мочеполовых путях, Trichomonas hominis – кишечная (в толстом кишечнике)и Trichomonas tenax – ротовая, обитающая в полости рта (рис.9 и V Пр).
 Trichomonas vaginalis (Влагалищная трихомонада) — жгутиковое простейшее, возбудитель урогенитального трихомонадоза. Влагалищная трихомонада имеет грушевидное тело длиной 14—30 мкм. На переднем конце тело имеет 4 жгутика и ундулирующую мембрану, доходящую только до середины тела. Ближе к переднему концу располагается ядро (рис. 9 и V Пр). Сквозь все тело проходит осевая нить (аксостиль), выступающая на заднем конце в виде шипика. Цитоплазма содержит вакуоли. Цист не образует, во внешней среде быстро погибает. Играет заметную роль в патологии мочеполовой системы, особенно у женщин.
Trichomonas vaginalis (Влагалищная трихомонада) — жгутиковое простейшее, возбудитель урогенитального трихомонадоза. Влагалищная трихомонада имеет грушевидное тело длиной 14—30 мкм. На переднем конце тело имеет 4 жгутика и ундулирующую мембрану, доходящую только до середины тела. Ближе к переднему концу располагается ядро (рис. 9 и V Пр). Сквозь все тело проходит осевая нить (аксостиль), выступающая на заднем конце в виде шипика. Цитоплазма содержит вакуоли. Цист не образует, во внешней среде быстро погибает. Играет заметную роль в патологии мочеполовой системы, особенно у женщин.
Трихомонады этого вида передаются половым путем, а также при пользовании общей постелью, бельем и предметами личной гигиены. Отсюда вытекают соответствующие профилактические мероприятия. Иногда высказываемое мнение о том, что трихомонады могут переселиться во влагалище из кишечника, неверно, так как кишечная и влагалищная трихомонады — это разные виды с различными требованиями к условиям среды обитания.
При урогенитальном трихомонадозе возбудитель болезни внедряется в слизистые оболочки мочеполовых путей, повреждая эпителиальные клетки и способствуя развитию воспалительного процесса. Основными симптомами при мочеполовом трихомонозе являются зуд, боль, жжение в мочеполовых путях, серозно-гнойные выделения (бели). Наблюдается и длительное бессимптомное носительство, чаще у мужчин. Заболевание встречается повсеместно.
Trichomonas hominis ( Кишечная трихомонада) имеет грушевидное тело длиной 8—20 мкм. От переднего конца тела отходят обычно 5 жгутиков (рис. 9). С одной стороны тела по всей его длине расположена волнообразная перепонка (ундулирующая мембрана), по наружному краю которой проходит тонкая нить, выступающая своим свободным концом в виде жгутика. В цитоплазме при окраске видны ядро и осевая нить, или аксостиль.
Движение трихомонады активное, беспорядочное, «суетливое». Наряду с поступательным движением трихомонады вращаотея вокруг продольной оси. Мембрану удается заметить только при замедлении движения трихомонады или при ее остановке в виде периодически пробегающих волн по одной из сторон тела. Размножается делением. Цист не образует. Обитает в толстом кишечнике человека. В жидких испражнениях может обнаруживаться в очень больших количествах. В ряде случаев играет определенную роль в развитии или ухудшении течения заболеваний толстого кишечника, особенно у детей раннего возраста.Кишечные трихомонады существуют только в виде вегетативных форм, которые локализуются в толстой кишке человека. Их размножение усиливается при диете богатой клетчаткой и другими углеводами, а также при различных заболеваниях, сопровождающихся разжижением содержимого толстой кишки. Являясь условно-патогенными организмами, кишечные трихомонады под действием ряда факторов могут приобретать патогенные свойства и вызывать кишечный трихомониаз, который протекает в форме колитов и энтероколитов. Возникают поносы от одного до 8 раз в сутки. Испражнения жидкие, водянистые или кашицеобразные, часто с примесью слизи, но без крови. Нередко отмечаются боли в животе различного характера. При ректороманоскопии слизистая оболочка прямой и сигмовидной кишок чрезмерно влажная в результате усиленной эксудации, блестящая, не гиперемированная, без слизи, эрозий и язв, как бы обмытая очистительной клизмой.
Усиленное размножение трихомонад в вызванных дизентерийными бактериями и амебами изъязвлениях замедляет их заживление. Трихомонады обнаруживались также в тканях кишечной стенки, в гнойном содержимом абсцессов печени и других органов.
Диагноз кишечного трихомониаза, при наличии соответствующей клинической картины, устанавливается в случае обнаружения трихомонад в испражнениях методом нативного мазка. При этом надо дифференцировать их от нередко совместно с ними встречающихся хиломастиксов (Chilomastix mesnili) и энтеромонад (Enteromonas hominis).
Trichomonas tenax ( Ротовая трихомонада) по строению похожа на кишечную форму, ее длина 6—13 мкм, ундулируюшая мембрана не достигает конца тела (рис. 9). Цист не образует.
Патогенное значение не доказано, хотя и имеются данные о значительно более частой встречаемости у лиц с различными заболеваниями полости рта и зубов (гингивит, пародонтоз, кариес зубов) и о неблагоприятной роли этих простейших в поддержании патологического процесса. Некоторые исследователи обнаруживали трихомонад в мокроте больных легочными заболеваниями, а также в удаленных хирургическим путем бронхоэктазах и абсцессах легких. Все это заставляет обратить внимание на необходимость более широкого применения лабораторных методов исследования с целью выявления ротовых трихомонад в стоматологических и терапевтических медицинских учреждениях.
Лабораторная диагностика. Трихомонад обнаруживают при микроскопии нативных или окрашенных мазков из соскоба ротовой полости (с зубов, десен, из очагов воспаления и нагноения), в бронхиальной слизи и мокроте. Диагностика урогенитального трихомониаза основывается на выявлении клинических признаков заболевания и обнаружении в исследуемом материале Trichomonas vaginalis.
Основными методами лабораторной диагностики трихомониаза являются:
- микроскопический;
- культуральный;
· полимеразная цепная реакция (ПЦР);
Серологические методы используются как вспомогательные, поскольку антитрихомонадные антитела могут циркулировать в сыворотке крови в течение длительного времени после лечения, что затрудняет дифференцирование текущей и перенесенной в прошлом трихомонадной инфекции.
Чувствительность метода микроскопии по различным данным варьирует от 38% до 82%. Несмотря на то, что этот метод среди диагностических тестов является определённо экономически наиболее целесообразным и простым, он имеет низкую чувствительность и специфичность. Это может быть обусловлено, в первую очередь, потерей трихомонадами характерной подвижности после того, как простейшее уже извлечено из среды человеческого организма. Особенно большая доля субъективизма проявляется в случае препаратов с низким титром или препаратов, содержащих огромное количество клеток эпителия, лейкоцитов и различного деструктивного материала из очага поражения. В очаге поражения влагалищная трихомонада часто представлена округлыми формами, напоминающими полиморфоядерные лейкоциты, и естественно, типичные морфологические признаки теряются во время фиксации и окрашивания, создавая трудность для этиологической идентификации.

Мазок Папаниколау, показывающий инвазию простейшими Trichomonas vaginalis
А  Б
Б 
Рис. V. Trichomonas vaginalis (1): А – мазок со слизистой влагалища, Б – трихомонада, выделенная из культуры.
|
|
|


