 |
Основные теоретические положения
|
|
|
|
Из трех агрегатных состояний (жидкого, твердого и газообразного), в которых может находиться всякое вещество, наиболее простым является газообразное. В газах среднее расстояние между молекулами во много раз больше размеров самих молекул. Межмолекулярные силы взаимодействия на таких расстояниях слабы, и молекулы движутся почти независимо друг от друга, меняя направление движения при столкновениях между собой или со стенками сосуда. В молекулярной физике широко используется модель идеального газа, в рамках которой считается, что межмолекулярные силы не просто малы, а полностью отсутствуют; размерами молекул можно пренебречь. Газ, обладающий такими же свойствами, как и совокупность невзаимодействующих материальных точек, называется идеальным газом.
Состояние газа характеризуется совокупностью величин, которые называются параметрами состояния. Такими параметрами состояния являются: давление p, под которым находится газ, его абсолютная температура T и объем V, занимаемый определенной массой газа M. Под объемом газа понимают тот объем, в котором молекулы газа движутся свободно (свободный объем). Для идеального газа свободный объем совпадает с геометрическим объемом сосуда, в котором находится газ. Параметры состояния газа не являются независимыми. Каждый из них является функцией двух других. Уравнение, связывающее все три величины p, T и V для данной массы газа M называется уравнением состояния и может быть в общем виде записано так:  . (5.1)
. (5.1)
При изучении различных процессов в газах удобно пользоваться их графическим представлением – изображаются кривые зависимости одних параметров от других.
Рассмотрим результаты экспериментальной проверки законов, управляющих поведением газов. Одним из них является Закон Бойля-Мариотта. Произведение давления газа на его объем при постоянной температуре есть величина постоянная:
|
|
|
 . (5.2)
. (5.2)
Процессы, идущие в газах, при постоянной температуре и неизменной массе газа называются изотермическими. Кривые, изображающие зависимость между физическими величинами, которые характеризуют свойства вещества при постоянной температуре, называется изотермами.
 Изотермы, определяющие зависимость
Изотермы, определяющие зависимость  от V газа, который подчиняется закону Бойля-Мариотта, представляют собой гиперболы, располагающиеся на графике тем выше, чем выше температура. На рис. 5.1 закон Бойля-Мариотта изображен графически для нескольких температур. По оси абсцисс отложен объем
от V газа, который подчиняется закону Бойля-Мариотта, представляют собой гиперболы, располагающиеся на графике тем выше, чем выше температура. На рис. 5.1 закон Бойля-Мариотта изображен графически для нескольких температур. По оси абсцисс отложен объем  , а по оси ординат – давление
, а по оси ординат – давление  .
.
Рис. 5.1. Графики изотермического
процесса при различных температурах
Реальные газы не строго подчиняются закону Бойля-Мариотта. Это проявляется в том, что кривые, изображающие зависимость давления газа от объема при постоянной температуре, отличаются от гипербол. Если отклонения не велики, то отличие трудно заметить. Легче обнаружить отклонения от закона Бойля-Мариотта, если воспользоваться иным представлением зависимости давления газа от объема, а именно, откладывать по оси абсцисс давление, а по оси ординат величину отношения  , где
, где  – количество молей газа (
– количество молей газа ( , здесь
, здесь  – молярная масса).
– молярная масса).
Молем какого-либо вещества называется количество этого вещества, содержащее столько же структурных элементов (молекул, атомов), сколько атомов содержится в 0,012 кг изотопа углерода 12С. Молярной массой называется масса одного моля вещества. В СИ эта величина измеряется в кг/моль.
Такие графики, полученные экспериментально для  киломолей водорода, азота и кислорода, приведены на рис. 5.2 для трех значений абсолютной температуры.
киломолей водорода, азота и кислорода, приведены на рис. 5.2 для трех значений абсолютной температуры.

Рис. 5.2. Экспериментальная зависимость  от давления [4]
от давления [4]
|
|
|
Из рис. 5.2 видно, что для всех трех газов получаются прямые линии, но при температуре 373,15 К (температура кипения воды при нормальном атмосферном давлении) только для кислорода прямая 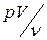 приблизительно параллельна оси
приблизительно параллельна оси  . Таким образом, при этой температуре закон Бойля-Мариотта справедлив только для кислорода, тогда как для водорода и азота наблюдаются отклонения от этого закона.
. Таким образом, при этой температуре закон Бойля-Мариотта справедлив только для кислорода, тогда как для водорода и азота наблюдаются отклонения от этого закона.
При температуре 273,16 К почти горизонтально идет линия азота, тогда как линия кислорода наклонна. Таким образом, при этой температуре закон Бойля-Мариотта справедлив для азота и не выполняется для кислорода.
Сравнение графиков, приведенных на рис. 5.2, показывает, что для одного и того же газа, например для кислорода, величина отношения  может при повышении давления возрастать, уменьшаться или оставаться постоянной в зависимости от температуры. Обсудим причины отклонения поведения реальных газов от закона Бойля-Мариотта.
может при повышении давления возрастать, уменьшаться или оставаться постоянной в зависимости от температуры. Обсудим причины отклонения поведения реальных газов от закона Бойля-Мариотта.
Объясним сначала, почему при повышении давления  может расти произведение
может расти произведение 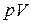 . Согласно закону Бойля-Мариотта, при повышении давления объем газа уменьшается во столько раз, во сколько повышается давление. Если при повышении давления
. Согласно закону Бойля-Мариотта, при повышении давления объем газа уменьшается во столько раз, во сколько повышается давление. Если при повышении давления  произведение
произведение 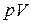 растет, то объем при этом уменьшается в меньшее число раз, чем повышается давление. Это легко объяснить, если допустить, что сами молекулы имеют некоторый объем. Обозначим через
растет, то объем при этом уменьшается в меньшее число раз, чем повышается давление. Это легко объяснить, если допустить, что сами молекулы имеют некоторый объем. Обозначим через 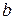 величину, связанную с собственным объемом молекул, на которую уменьшается предоставленный молекулам объем. Тогда разность
величину, связанную с собственным объемом молекул, на которую уменьшается предоставленный молекулам объем. Тогда разность  есть свободный объем, а связь между давлением и объемом газа можно выразить следующим уравнением:
есть свободный объем, а связь между давлением и объемом газа можно выразить следующим уравнением:
 (при Т=const).
(при Т=const).
Рассмотрим теперь, как объяснить уменьшение 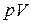 с возрастанием давления. Такое уменьшение
с возрастанием давления. Такое уменьшение 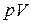 возможно, если объем V уменьшается в большей степени, чем повышается давление
возможно, если объем V уменьшается в большей степени, чем повышается давление  . Это становится понятным, если допустить, что объем газа уменьшается не только под действием внешнего давления
. Это становится понятным, если допустить, что объем газа уменьшается не только под действием внешнего давления  , но также под действием внутреннего давления
, но также под действием внутреннего давления 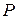 , обусловленного силами взаимного притяжения между молекулами. В этом случае, если пренебречь объемом молекул, вместо уравнения (5.1) получим:
, обусловленного силами взаимного притяжения между молекулами. В этом случае, если пренебречь объемом молекул, вместо уравнения (5.1) получим:  (при Т=const)
(при Т=const)
или  .
.
Из последнего уравнения следует, что наличие сил взаимного притяжения между молекулами приводит к уменьшению произведения 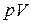 при повышении
при повышении  .
.
|
|
|
Таким образом, пойдет изотерма с повышением давления вниз или вверх, решается в зависимости от того, что будет преобладать: влияние сил притяжения или влияние объема молекул. Из того, что при малых давлениях изотермы располагаются ниже прямой  , а при больших – выше этой прямой, можно сделать вывод, что при малых плотностях газа большее значение имеют силы межмолекулярного притяжения, а при больших плотностях – собственный объем молекул.
, а при больших – выше этой прямой, можно сделать вывод, что при малых плотностях газа большее значение имеют силы межмолекулярного притяжения, а при больших плотностях – собственный объем молекул.
Из экспериментальных данных, представленных на рис. 5.2, следует важный результат: линии, изображающие зависимость  от давления
от давления  при постоянной температуре, сходятся в одной точке, лежащей на оси
при постоянной температуре, сходятся в одной точке, лежащей на оси  (если их продолжить в область низких давлений). Это означает, что при бесконечном увеличении объема, и следовательно,
(если их продолжить в область низких давлений). Это означает, что при бесконечном увеличении объема, и следовательно,  , произведение давления одного киломоля газа на объем стремится к постоянной величине. Как видно из графиков на рис. 5.2, эта постоянная зависит от температуры. Однако, если предельные значения
, произведение давления одного киломоля газа на объем стремится к постоянной величине. Как видно из графиков на рис. 5.2, эта постоянная зависит от температуры. Однако, если предельные значения  разделить на соответствующую абсолютную температуру, получатся равные числа:
разделить на соответствующую абсолютную температуру, получатся равные числа:
 . (5.3)
. (5.3)
Число R, равное 8,31 Дж/моль, называется универсальной газовой постоянной..
При исследовании газовых законов результаты экспериментов были представлены также в виде графиков зависимости  от температуры (рис. 5.3). В верхней части для всех идеальных газов на этом графике получились прямые линии; наклон этих прямых меняется от газа к газу, но продолжения их пересекаются с осью абсцисс в одной и той же точке, а именно, при -273˚С.
от температуры (рис. 5.3). В верхней части для всех идеальных газов на этом графике получились прямые линии; наклон этих прямых меняется от газа к газу, но продолжения их пересекаются с осью абсцисс в одной и той же точке, а именно, при -273˚С.
В нижней части рис. 5.3 представлена зависимость  от температуры, что привело к значительному упрощению: теперь наклон прямых оказывается для всех идеальных газов одинаков; через точки, полученные путем измерения с различными газами, можно теперь провести только одну общую прямую. Наклон этой прямой определяется отношением (5.3). Ее точка пересечения с осью абсцисс остается прежней: -273˚ С. Этот экспериментальный факт дает возможность определить «абсолютную шкалу» температур, т.е. шкалу без отрицательных значений и практически не зависящую от свойств вещества (шкала Кельвина).
от температуры, что привело к значительному упрощению: теперь наклон прямых оказывается для всех идеальных газов одинаков; через точки, полученные путем измерения с различными газами, можно теперь провести только одну общую прямую. Наклон этой прямой определяется отношением (5.3). Ее точка пересечения с осью абсцисс остается прежней: -273˚ С. Этот экспериментальный факт дает возможность определить «абсолютную шкалу» температур, т.е. шкалу без отрицательных значений и практически не зависящую от свойств вещества (шкала Кельвина).
|
|
|
На рис. 5.3 точку прямых, для которых величина  измерена в окружении тающего льда, обозначают на оси абсцисс значением 273 К. Важной особенностью шкалы температур Кельвина является то, что градусы шкалы Кельвина совпадают по размерам с градусами шкалы Цельсия. Между обеими шкалами температур имеет место простое соотношение:
измерена в окружении тающего льда, обозначают на оси абсцисс значением 273 К. Важной особенностью шкалы температур Кельвина является то, что градусы шкалы Кельвина совпадают по размерам с градусами шкалы Цельсия. Между обеими шкалами температур имеет место простое соотношение:
 .
.
Шкала Кельвина, которая также называется абсолютной шкалой температур, нанесена на рис. 5.3.

Рис. 5.3. Экспериментальные графики процессов в нескольких газах [6]
Таким образом, обе серии экспериментов по изучению свойств газов приводят к результату (5.3). Уравнение (5.3) называют уравнением Клапейрона-Менделеева и записывают в виде:
 . (5.4)
. (5.4)
Газ, подчиняющийся уравнению Клапейрона-Менделеева, называется идеальным. Идеальный газ есть предельный случай реального при  . Уравнение Клапейрона-Менделеева является обобщенной формой законов Бойля-Мариотта, Гей-Люссака и Шарля. Все эти законы являются законами идеального газа; выражающие их уравнения выводятся как частные случаи из уравнения Клапейрона-Менделеева.
. Уравнение Клапейрона-Менделеева является обобщенной формой законов Бойля-Мариотта, Гей-Люссака и Шарля. Все эти законы являются законами идеального газа; выражающие их уравнения выводятся как частные случаи из уравнения Клапейрона-Менделеева.
При Т=const уравнение (5.4) преобразуется в уравнение Бойля-Мариотта:  (
( ). (5.5)
). (5.5)
Процессы в газе, идущие при постоянном давлении  и неизменной массе газа, называются изобарными. Для изобарных процессов из уравнения состояния (5.4) получаем закон Гей-Люссака:
и неизменной массе газа, называются изобарными. Для изобарных процессов из уравнения состояния (5.4) получаем закон Гей-Люссака:
 (
( ) (5.6)
) (5.6)
- при постоянном давлении отношение объема газа к абсолютной температуре есть величина постоянная.
Процессы в газе, идущие при постоянном объеме  и неизменной массе газа, называются изохорными. Для них из уравнения (5.4) получаем закон Шарля:
и неизменной массе газа, называются изохорными. Для них из уравнения (5.4) получаем закон Шарля:
 (
( ) (5.7)
) (5.7)
- при постоянном объеме отношение давления газа к абсолютной температуре есть величина постоянная.
К законам идеального газа относится и закон Авогадро: в равных объемах газов при одинаковых давлениях и температурах содержится одинаковое число молекул.
В уравнении Клапейрона-Менделеева R есть величина постоянная для всех газов. В одном киломоле газа содержится одно и то же число молекул – число Авогадро NA. Можно определить газовую постоянную, отнесенную к одной молекуле:  . Это – постоянная Больцмана. Если ввести постоянную Больцмана в уравнение Клапейрона-Менделеева, то его можно преобразовать к новому виду:
. Это – постоянная Больцмана. Если ввести постоянную Больцмана в уравнение Клапейрона-Менделеева, то его можно преобразовать к новому виду:
 , (5.8.)
, (5.8.)
где 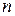 есть число молекул в единичном объеме.
есть число молекул в единичном объеме.
Из уравнения (5.8) следует, что давление идеального газа при данной температуре определяется только числом молекул в единице объема и не зависит от рода молекул.
|
|
|


