 |
Адсорбция на поверхности твердых тел.
|
|
|
|
Адсорбция газов. Твердые вещества адсорбируют молекулы из окружающей среды. Чем больше поверхность твердого тела, тем больше газа он может поглотить. Сильно развитой поверхностью обладают вещества имеющие пористую структуру или в состоянии тонкого измельчения (коллоиды).
Лучшие адсорбенты: уголь (древесный и костный), силикагель, кварцевый песок, каолин, и некоторые алюмосиликаты и т.д.
Абсолютное количество адсорбированного вещества определяют по разности между первичным количеством адсорбтива и оставшегося свободным после установления равновесия.
Количество поглощенного вещества (х), на 1 см2 адсорбирующей поверхности, называется удельной адсорбцией.
 .
.
У пористых адсорбентов поверхность измерить трудно, поэтому удельную адсорбцию выражают в этом случае в молях на 1 г. адсорбента, Гуд=  ,
,
где m – масса адсорбента.
Для каждого адсорбента установлена максимальная величина его насыщения (Г∞ при определенных условиях).

Количество вещества адсорбированного 1 см2 поверхности адсорбента зависит:
- от химической природы адсорбента и адсорбтива;
- от состояния поверхности;
- от концентрации адсорбтива;
- от температуры.
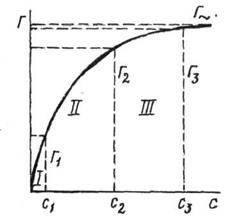
При постоянной температуре адсорбированное количество (Г) зависит только от равновесной концентрации (С) адсорбтива. Рассмотрим изотерму адсорбции (рисунок 8).
|
Рис. 8. Изотерма адсорбции.
Из рисунка видно, что при повышении концентрации возрастает и Г, приближаясь к своему предельному значению Г∞. Однако, зависимость не везде одинакова.
1. Область 1 (низкие концентрации) величина Г прямопропорциональна С.
2. В области 2 увеличение концентрации увеличивает Г в меньшей степени.
|
|
|
3. В области 3 при больших концентрациях кривая стремится к прямой параллельной оси абсцисс. Это говорит о достижении полного насыщения поверхности адсорбента.
Изотерма адсорбция справедлива для газообразных и растворенных веществ.
Применение адсорбции.
1. При гетерогенном катализе с твердым катализатором.
2. Очистка газов и растворов от примесей (активированный уголь в противогазах, процессы осветления и обесцвечивания).
3. Экстракция ценных продуктов (извлечение фенолов из воды активированным углем, силикагелем). Затем методы десорбции.
4. В процессе биологической очистки СВ (адсорбция загрязнений активным илом, биопленкой).
5. Умягчение и обессоливание воды методом ионного обмена (полярная адсорбция).
Коллоидные системы
Классификация золей
Дисперсная система с размером частиц от 1 до 100 нм, распределённых в той или иной среде, называются коллоидным раствором или золем. Коллоидные системы являются гетерогенными системами, состоящими из двух или более фаз.
Характеристикой коллоидного раствора является величина свободной межфазной энергии. Величина эта зависит от:
- удельной поверхности частиц S0;
S0= 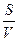 ,
,
где S - суммарная поверхность;
V - объём дисперсной фазы;
-степени дисперсности D;
D= 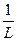 ,
,
где L – размер частиц.
Существует несколько классификаций коллоидных систем:
- классификация по агрегатному состоянию дисперсионной среды:
1. Аэрозоли - дисперсионная среда газообразная (дым, туман и т.д.).
2. Лиозоли – дисперсионная среда жидкость (гидрозоли).
3. Солиозоли – дисперсионная среда твёрдая (сплавы).
4. Пены – дисперсия газа в жидкости;
- классификация по межфазному взаимодействию:
1. Лиофильные – характеризуются сильным межмолекулярным взаимодействием между веществом дисперсной фазы со средой.
2. Лиофобные – слабое взаимодействие;
- классификация по внутренней структуре частиц:
|
|
|
1. Суспензоиды – высокодисперсные гетерогенные системы (лиофильные и лиофобные) неустойчивые и необратимые.
От суспензий они отличаются размерами частиц. Они не могут длительно существовать в отсутствии стабилизатора дисперсности (как и суспензии). Необратимые, т.к. осадки суспензоидов остающиеся при выпаривании таких коллоидов не образуют вновь золя при контакте с дисперсионной средой. К ним относятся золи металлов, их оксидов, гидроксидов, различных неорганических солей.
Свойства суспензоидов определяются очень сильной поверхностной энергией, это приводит к неустойчивости их без стабилизатора.
Высокомолекулярные соединения (белки, полипептиды, поливиниловый спирт и др.), добавляемые для стабилизации дисперсных систем называются защитными коллоидами.
Адсорбируясь на границе раздела фаз, они образуют в поверхностном слое структуры, создающие барьер, препятствующий объединению частиц дисперсной фазы.
2. Молекулярные коллоиды – гомогенные системы, устойчивые и обратимые. К ним относятся высокомолекулярные вещества с молекулярной массой от десяти тысяч до нескольких миллионов. Молекулы этих веществ имеют размеры коллоидных частиц, поэтому такие молекулы называются макромолекулами. Образование молекулярных коллоидных систем происходит в процессе набухания.
При неограниченном набухании полимер переходит в растворимое состояние с образованием гомогенной системы. Растворы молекулярных коллоидов легко превращаются в гетерогенные системы при незначительном изменении состава среды (белок, растворённый в воде, при добавлении спирта переходит в лиофобный золь).
3. Мицеллярные коллоиды (полуколлоиды). Коллоиднодисперсные частицы этого типа возникают при высокой концентрации дифильных молекул низкомолекулярных веществ путем их ассоциации в агрегаты молекул (мицеллы) сферической или пластинчатой формы.
Дифильные молекулы состоят из углеводородного радикала, имеющего сродство к неполярным растворителям, и гидрофильной группы, имеющей сродство к воде.

Рис. 9. Образование мицелл из дифильных молекул
Мицеллы представляют собой скопление правильно расположенных молекул, удерживаемых дисперсионными силами. Образование мицелл характерно для водных растворов моющих веществ (мыла), некоторых органических красителей и т.д.
|
|
|
|
|
|


