 |
Получение монокристаллов из раствора
|
|
|
|
Кристаллизацией из раствора получают более чистые и совершенные по структуре монокристаллы, так как процесс происходит при более низких температурах, чем кристаллизация из расплавов. Раствор – гомогенная (однородная) смесь, образованная двумя и более компонентами, один из которых растворитель, другой – растворимое вещество. Компоненты распределены в виде молекул, атомов или ионов. Растворители – вода, многокомпонентные водные и неводные растворы, расплавы химических соединений.
Процесс роста состоит из следующих стадий: 1) растворение компонентов; 2) диффузия компонентов через жидкую фазу к фронту кристаллизации; 3) осаждение и диффузия в кристалле; 4) отвод теплоты кристаллизации. При выращивании кристаллов из расплава лимитирующей стадией является отвод теплоты, при выращивании из раствора – диффузия компонентов. Вследствие этого скорость роста кристаллов из раствора на 2–3 порядка меньше скорости роста из расплавов.
В зависимости от температуры процесса и химической природы растворителя различают процессы выращивания из низкотемпературных растворов (температуры не выше 80–90 °С), перегретых растворов (гидротермальный метод, температуры до 800 °С), солевых расплавов (кристаллизация из раствора в расплаве, температуры до 1500 °С).
Низкотемпературный кристаллизатор (см. рис. 2.12). Растворители – вода, спирты, кислоты и др. Необходимое для начала кристаллизации пересыщение раствора достигается при постепенном понижении температуры в объеме кристаллизатора, либо при создании в кристаллизаторе двух зон с различными температурами.
Методом снижения температуры раствора выращивают кристаллы сегнетовой соли, квасцов и т. д. В методе температурного перепада в кристаллизаторе создают две области с разными температурами. В нижней части высокого сосуда происходит растворение твердого вещества, в верхней подвешивается затравка. В результате конвекции раствора обеспечивается постоянный перенос вещества снизу вверх, в зону роста. Этим методом выращивают кристаллы дигидрофосфатов калия и 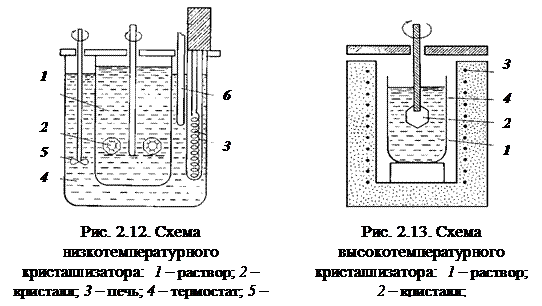 аммония (KDP и ADP). Скорость роста составляет около 1 мм в сутки. Кристаллы весом 400 г растут 1,5–2 месяца.
аммония (KDP и ADP). Скорость роста составляет около 1 мм в сутки. Кристаллы весом 400 г растут 1,5–2 месяца.
|
|
|
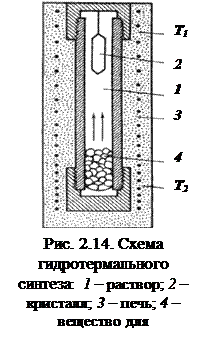 Высокотемпературный кристаллизатор (рис. 2.13) имеет тигель с растворителем и кристаллизуемым соединением, помещенный в печь. Растворители – расплавленные соли и др. Кристалл растет при медленном снижении температуры (раствор-расплавная кристаллизация). Метод применяется для получения кристаллов железоиттриевых гранатов, слюды, полупроводниковых пленок.
Высокотемпературный кристаллизатор (рис. 2.13) имеет тигель с растворителем и кристаллизуемым соединением, помещенный в печь. Растворители – расплавленные соли и др. Кристалл растет при медленном снижении температуры (раствор-расплавная кристаллизация). Метод применяется для получения кристаллов железоиттриевых гранатов, слюды, полупроводниковых пленок.
Гидротермальное выращивание (рис. 2.14) применяется, когда растворимость вещества в водной среде при комнатной температуре и нормальном давлении мала, либо имеется несколько полиморфных модификаций. Сущность, как и в методе температурного перепада, заключается в непрерывном переносе растворенного вещества конвекционными потоками, которые образуются в растворе вследствие наличия градиента температуры. Пересыщение создается за счет высокого давления и перепада температур между верхней и нижней частями автоклава. В верхней части автоклава образуется кристалл. Скорость выращивания – от долей мм до нескольких мм в сутки. Кристаллы имеют высокое качество и кристаллографическую огранку, так как растут в условиях, близких к равновесным. Гидротермальный синтез – основной процесс производства монокристаллов кварца, рубина, кальцита, некоторых полупроводников.
Например, кристаллы сфалерита ZnS невозможно получить из расплава: при 1080 °С происходит полиморфное превращение в гексагональную модификацию – вюрцит. В гидротермальных условиях рост сфалерита происходит при более низкой (300–500 °С) температуре, т. е. в области устойчивой кубической модификации.
|
|
|

 Выращивание из раствора в расплаве. Метод спонтанной кристаллизации (рис. 2.15) заключается в обдуве холодным газом небольшого участка в центре дна тигля, где и возникает кристалл. Так как объем раствора велик (10–20 л), то растущий кристалл слабо меняет общее пересыщение раствора. Достоинство метода: кристаллизация проводится значительно ниже температуры плавления. Недостатки: необходимость точного регулирования температуры, дорогостоящие тигли. Способ позволил решить проблему синтеза алмаза для абразивных целей. Температура кристаллизации 1500 °С, давление в камере 50–60 тыс. атм. В качестве катализаторов-растворителей используются металлы переходной валентности: хром, марганец, кобальт, никель, палладий. Источник углерода – графит. При нагревании образуется раствор, в котором возникают кристаллы алмаза. Выращивают также крупные монокристаллы феррогранатов и ортоферритов.
Выращивание из раствора в расплаве. Метод спонтанной кристаллизации (рис. 2.15) заключается в обдуве холодным газом небольшого участка в центре дна тигля, где и возникает кристалл. Так как объем раствора велик (10–20 л), то растущий кристалл слабо меняет общее пересыщение раствора. Достоинство метода: кристаллизация проводится значительно ниже температуры плавления. Недостатки: необходимость точного регулирования температуры, дорогостоящие тигли. Способ позволил решить проблему синтеза алмаза для абразивных целей. Температура кристаллизации 1500 °С, давление в камере 50–60 тыс. атм. В качестве катализаторов-растворителей используются металлы переходной валентности: хром, марганец, кобальт, никель, палладий. Источник углерода – графит. При нагревании образуется раствор, в котором возникают кристаллы алмаза. Выращивают также крупные монокристаллы феррогранатов и ортоферритов.
Кристаллизация на затравку – затравочный кристалл находится в растворе и частично растворяется. Пересыщение раствора создается вблизи кристалла. Рост происходит при снижении температуры раствора. Равномерная подача вещества достигается вращением кристалла.
Зонная раствор-расплавная кристаллизация аналогична зонной плавке и заключается в том, что благодаря температурному градиенту происходит перемещение узкой зоны раствора вдоль образца.
|
|
|


