 |
Методология проведения анализа эффективности
|
|
|
|
Анализ эффективности является первым этапом проводимого фармакоэкономического исследования. Анализ эффективности ставит перед собой задачу поиска показателя эффективности, удовлетворяющего целям исследования, а также получения данных, характеризующих анализируемые технологии с позиций выбранного показателя эффективности.
В зависимости от дизайна фармакоэкономического исследования анализ эффективности может осуществляться двумя методами: организацией и проведением клинических исследований анализируемого Л С или же анализом уже существующих рандомизированных клинических исследований (РКИ). Проспективный дизайн исследования включает в себя проведение нового РКИ. В случае ретроспективного дизайна фармакоэкономического исследования, имеющего место в настоящей работе, данные о показателях эффективности анализируемых технологий получают методом информационного поиска. Информационный поиск осуществляется прежде всего в специализированных библиотеках и базах данных (БД). Наиболее информационно обеспеченными и часто используемыми БД по РКИ являются зарубежные электронные БД: РиЪтей, МеёИпк и СосЬгапе.
Важным этапом фармакоэкономических исследований является выбор специальных критериев (точек), с помощью которых оценивается эффективность медицинского вмещательства, что позволяет сделать вывод о целесообразности его применения в клинической практике. Поэтому в правильном выборе точек кли-
нической эффективности оказываются заинтересованными четыре стороны: 1) специалисты в области клинических испытаний; 2) специалисты в области фармакоэкономики; 3) практикующие врачи; 4) пациенты.
|
|
|
Адекватный выбор конечных точек подразумевает получение с их помощью объективной оценки эффективности медицинского вмещательства; так, например, отдаленные результаты могут не подтвердить заключения об эффективности лечения, сделанного на основании анализа прямых клинических эффектов исследуемого вмещательства. Лечение препаратом, снижающим АД, не всегда приводит к уменьщению риска инсульта и преждевременной смерти (что и было с верапамилом). Таким образом, при выборе точек клинической эффективности необходимо учитывать следующие факторы: специфику медицинского вмещательства; особенности и характер течения заболевания; значимость точки для пациента и т. д. В качестве критериев эффективности медицинского вмещательства при проведении комплексного клинико-эконо-мического анализа могут использоваться:
1. Прямые клинические эффекты (сдвиг физиологических и биохимических параметров, на изменение которых направлено действие лекарственного средства, — снижение АД, прирост гемоглобина и т. п.; устранение симптомов и синдромов заболевания; потеря или восстановление функций).
2. Опосредованные клинические эффекты (снижение частоты осложнений, сокращение числа повторных госпитализаций и т. п.).
3. Изменение показателей здоровья в группе, на которую направлено действие медицинского вмешательства (смертность, вьгживаемость, продолжительность жизни, инвалидизация, число сохраненных лет без инвалидности и т. п.).
4 Изменение КЖ, обусловленного здоровьем (ОАЬУ).
Таблица 4.1. Сравнительная характеристика точек клинической эффективности
| Вид точки | Предлагаемая суррогат- | Целевая клиниче- | Конечная | |
| ная точка | ская точка | точка | ||
| Расшиф- | Биомаркер или клини- | Клиническая точ- | Клиниче- | |
| ровка | ческая точка, предна- | ка, обладающая | ская точка. | |
| значенная для замены | высокой значимо- | непосредст- | ||
| конечной точки | стью для пациен- | венно отра- | ||
| Биомаркер | Клиниче- | та, но необяза- | жающая | |
| ская точка | тельно отражающая продолжительность и качество жизни | продолжительность и качество жизни | ||
| Примеры | Уровень | Боль в | инфаркт миокар- | Количество |
| лпнп | груди | да, сердечно-сосудистая смерть, абсолютная выживаемость | продленных лет качественной жизни | |
| Значи- | Неочевид- | Очевидны | ->• | Очевидны и |
| мость для | ны для па- | для паци- | значимы для | |
| пациента | циента | ента | пациента | |
| Направ- | Критерий, Ориентиро- | -> | Критерий, | |
| ленность | ванный на болезнь | ориентированный на пациента |
Предпочтительной считается оценка эффективности с использованием критериев 3-й и 4-й групп, которые могут быть отнесены к конечным точкам [8]. Однако использование таких критериев, как смертность, выживаемость, продолжительность жизни, требует длительного периода проведения исследования и сопряжено со значительными финансовыми затратами, поэтому при определенных условиях конечные точки могут быть заменены на суррогатные (1-я и 2-я группы). Суррогатные точки могут быть сравнительно легко измерены, поэтому их использование значительно ускоряет процесс исследования и снижает затраты на его проведение. Сравнительная характеристика видов точек клинической эффективности представлена в табл. 4.1 [8].
|
|
|
Биологический маркер (биомаркер) — измеряемый и поддающийся количественному определению объективный индикатор естественного и патологического
биологического процесса и/или фармакологического ответа на терапевтические вмешательства на разных уровнях организменной и популяционной интеграции п]. В качестве биомаркеров могут использоваться: характеристики патологического процесса (лабораторные, иммуноферментные, биохимические показатели и Др.); состояния морфологических структур (наиболее часто — медицинские изображения); распределение фенотипа специфических генов в популяции; присутствие в тканях биологических субстанций и т. п. [2]. Для биологических маркеров характерны следующие свойства: а) специфичность — предпочтительно, чтобы биомаркер являлся индивидуальной характеристикой конкретного патологического процесса и не был подвержен влиянию других процессов (протекающих как в организме, так и вне его); б) заменимость — мониторинг исследуемого процесса может осуществляться с помощью нескольких равнозначных биомаркеров (утренний пик экспираторного потока и объем форсированного вьщоха при обструктивных заболеваниях легких); в) практичность — наличие четкой однозначной методики измерения позволяет упростить использование биомаркеров и снизить вероятность возникновения погрешностей; г) валидность — является самой важной характеристикой для биомаркеров, используемых в клинических испытаниях. Валидными называются биомаркеры, имеющие доказательство объективного отражения исследуемого физиологического, патологического, токсикологического, клинического явления и измеренные в системе аналитического теста с качественными характеристиками. Также вьщеляют группу биомаркеров неустановленной валидности, доказательство которых построено на общем соглашении в медицинской и научной практике, и биомаркеров вероятной валидности, не подвергавшихся публичной оценке [3]. Однако любой биологический маркер является результатом измерений, а всякий метод измерений имеет погрешность. Погрешность может быть обусловлена методом измерений, либо связана непосред-
|
|
|
ственно с ошибками измерений в том числе из-за психофизиологических особенностей личности исследователя. Также следует учитывать, что биомаркер есть некая количественная мера явления, но не само явление.
Конечная точка — мера исхода, используемая в оценке эффективности медицинского (диагностического, лечебного, иного) вмешательства. Конечные точки обладают высокой значимостью для пациента, так как являются объективным отражением уровня здоровья человека, а также характеризуют состояние и исходы имеющегося у него патологического и естественного биологического процесса и связанного с ним функциональных и морфологических реакций и/или фармакологического ответа на врачебные вмешательства. Различают два уровня конечных точек: популя-ционный и индивидуальный [2]. Конечные точки по-пуляционного уровня отражают эффект медицинского вмешательства в масштабах популяции (например, заболеваемость, смертность, развитие осложнений и др.) Конечные точки индивидуального уровня используются для оценки эффективности медицинского вмешательства у конкретного пациента: КЖ, исход патологического процесса (разрешение, переход в по-дострое состояние, хронизация), класс функциональных нарушений вовлеченных в процесс органов и систем и др. Следует отметить, что результаты исследований с использованием конечных точек популяци-онного уровня носят статистический характер и не отражают индивидуальных реакций, поэтому в последние годы наблюдается тенденция в сторону совместного использования точек обоих уровней для обеспечения максимальной объективности и достоверности результатов исследований.
|
|
|
Суррогатная (замеш;аюшая) точка — мера исхода, используемая в оценке эффективности медицинского (диагностического, лечебного, иного) вмешательства у конкретного пациента, основанная на биологических маркерах [2]. Суррогатные точки являются результатами измерений структурных и функциональных при-
| /^Медицин (вмешател | гкоеХ — зСТВО /^ | - валида- ция - количест венное из- | |||||
| Патологический процесс (ИБО) | ^^ | Суррогатная точка (АД, уровень холестерина В крови) | мерение | Конечная точка (смертность, заболеваемость, КЖ) | ^ | Анализ - «затра— ты-эффек-тивность» | |
| \ Источник данных (мета-анализ контролируемых рандомизированных исследований) | |||||||
Рис. 4.1. Использование точек клинической эффективности в фарма- коэкономических исследованиях.
знаков биологических маркеров, используемыми как заместительные для клинически значимых точек. Использование суррогатных точек основывается на предположении о том, что изменения биологических маркеров, произошедшие в результате медицинского вмешательства, могут предопределить изменения конечных точек. Необходимым условием для этого является установление связи между суррогатными и конечными точками, для чего разрабатываются специальные руководства, подробнее о которых будет изложено далее. Основными критериями суррогатных точек являются [1]: простота выявления; частота событий выше, чем у конечных точек; наличие теоретической и эпидемиологической связи с патофизиологией заболевания; наличие связи с реальными конечными точками; параллелизм в обратном развитии с конечными точками. Однако нельзя забывать, что для получения достоверных результатов необходимо доказать связь как между самими суррогатной и конечной точками, так и между их изменением в результате медицинского вмешательства.
|
|
|
Схематично использование точек клинической эффективности в фармакоэкономических исследованиях может быть представлено следующим образом (рис. 4.1) [9].
В качестве источника информации для проведения

|
Рис. 4.2. Пример нерационального выбора суррогатной точки — суррогатная точка находится вне пути воздействия патологического процесса на конечную точку.
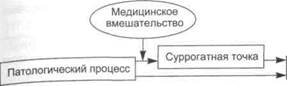
|
Конечная точка
Рис. 4.3. Пример нерационального выбора суррогатной точки — суррогатная точка отражает только один из нескольких механизмов патологического процесса.

|
| Медицинское вмешательство |
 фармакоэкономического анализа эффективности медицинского вмешательства чаще всего используется мета-анализ результатов контролируемых рандомизированных исследований. Если в исследованиях, выбранных для мета-анализа, в качестве критериев эффективности использовались суррогатные точки, то осуществляется валидация. Однако на практике медицинское вмещательство, вызывающее изменение суррогатной точки, может не оказывать эффекта на конечную точку, даже при условии установленной связи между этими точками. Наиболее характерные причины подобного несоответствия [5]:
фармакоэкономического анализа эффективности медицинского вмешательства чаще всего используется мета-анализ результатов контролируемых рандомизированных исследований. Если в исследованиях, выбранных для мета-анализа, в качестве критериев эффективности использовались суррогатные точки, то осуществляется валидация. Однако на практике медицинское вмещательство, вызывающее изменение суррогатной точки, может не оказывать эффекта на конечную точку, даже при условии установленной связи между этими точками. Наиболее характерные причины подобного несоответствия [5]:
1. Суррогатная точка основана на биомаркере, который изменяется так же, как и конечная точка, под действием патологического процесса, но лежит вне механизма действия патологического процесса на конечную точку: показатели уровней онкомаркеров ра-ково-эмбриональный антиген и простатоспецифиче-ский антиген колеблются аналогично изменению риска заболеваемости/смертности. Само по себе изменение уровня онкомаркеров не является звеном патологического процесса, в результате которого происходит изменение конечной точки (рис. 4.2).
2. Суррогатная точка отражает только один из нескольких путей развития патологического процесса, вызывающего изменение конечной точки, в результате чего влияние медицинского вмещательства на конечную точку может быть недо- или переоценено. Множественность факторов риска развития инфаркта миокарда при АГ обусловливает необходимость использования системы суррогатных точек для получе-
| ^, | - | |||
| Патологический процесс | Суррогатная точка | Конечная точка |
Рис. 4.4. Пример нерационального выбора суррогатной точки — суррогатная точка охватывает не все эффекты медицинского вмешательства.
ния наиболее достоверных результатов (АД, гипертрофия левого желудочка, функциональное состояние сосудов и др.) (рис. 4.3)
3. Медицинское вмещательство может обладать эффектами, независимыми от основного терапевтического эффекта, влияние которых на конечные точки зачастую не учитывается (исследование антиаритмических препаратов — флекаинида и энкаинида) [4]. Известно, что аритмия является основным фактором риска преждевременной сердечной смерти. В ходе исследования оба препарата эффективно устраняли аритмию, однако изменение конечной точки не совпало с прогнозом — абсолютная вьгживаемость снизилась. Позже было установлено, что противоположный эффект медицинского вмещательства на конечную точку обусловлен побочным действием препаратов, возможность которого влиять на результаты была ощибочно оценена исследователями как незначительная (рис. 4.4).
Достоверность результатов исследований, проводимых с заменой (трансформацией) конечных точек на
Таблица 4.2. Шкала оценки суррогатных точек по методике ОМЕКАСТ
| Блок | Расшифровка | Баллы |
| Цель исследо- | Истинная конечная точка, которая была за- | |
| вания | менена на суррогатную в ходе исследования | 0-5 |
| Дизайн иссле- | Достоверность доказательства связи между | |
| дования | конечной и суррогатной точками | 0-5 |
| Статистиче- | Выраженность связи между конечной и сур- | |
| ская обосно- | рогатной точками и ее статистическое зна- | |
| ванность | чение | 0-5 |
| Штрафы | Недостаток доказательств или наличие их опровержения (биологическое и эпидемио- | |
| логическое) | 1-3 |
суррогатные, во многом зависит от качества валида-ции, подробного доказательства взаимосвязи не только самих конечных и суррогатных точек, но и их изменения в результате медицинского вмешательства. Существуют различные подходы к осуществлению ва-лидации, один из которых описан далее. Подробная методика валидации суррогатных точек была разработана английской научной группой, входящей в международную исследовательскую организацию ОМЕКАСТ (Ои1соте Меазигез 1п Ш1еита1о1й АШтгШд СИшса! Тг1а18) [9]. Была создана схема, позволяющая классифицировать суррогатные точки по силе доказательства их связи с конечными точками. Данная система представляет собой методику определения степени «доказательности» суррогатных точек, которая заключается в оценке суррогатной точки по определенным критериям, объединенным в четыре блока, после чего ей присваивается один из пяти валидационных уровней в зависимости от количества набранных баллов. Кратко методика ОМЕКАСТ 8соппё представлена в табл. 4.2.
Итоговое количество набранных баллов, может колебаться от О до 15, используется для определения уровня доказательства связи между конечной и суррогатной точками (от самого сильного — уровень 1, до самого слабого — уровень 5). Авторы данной методи-
5да предлагают считать возможной замену конечных точек только на суррогатные точки уровней 1 и 2 (набравшие 10 баллов и более). Таким образом, использование оценочной шкалы ОМЕКАСТ, благодаря четким и однозначным критериям, позволяет формализовать подход к валидации суррогатных точек, повышая тем самым ее качество.
Рассмотрим пример выбора точек на примере изменения уровня холестерина.
Известно, что повышенный уровень ОХС, его фракций и триглицеридов в крови является одним из самых сильных факторов риска внезапной сердечной смерти, однако в научных кругах до сих пор не остывают споры о связи снижения уровня липидов в крови и уменьшения общей смертности. Некоторую ясность в этот вопрос внесли результаты мета-анализа, проведенного американским ученым Дж. Гордоном [6]. В мета-анализ были включены 50 рандомизированных контролируемых исследований различных медицинских вмешательств, направленных на снижение уровня холестерина, таких как диета, гормоны, фиб-раты, секвестранты желчных кислот, статины. Среднее снижение уровня холестерина, обусловленное эффектом медицинского вмешательства, составило 10%, тогда как смертность в результате сердечных событий снизилась на 9%. Но, несмотря на это, эффект данной группы медицинских вмешательств на общую смертность оказался противоположным, так как смертность, не связанная с сердечными событиями, выросла на 24%, в результате чего общая смертность увеличилась на 1%. Таким образом, отрицательное влияние медицинских вмешательств на общую смертность нивелировало их положительное действие на смертность в результате сердечных событий. Поэтому без использования общей смертности в качестве конечной точки эффективность таких групп препаратов, как гормоны и фибраты, оказывающих выраженное гиполипидемическое действие, была бы оценена неадекватно [7].
Таким образом, конечные точки являются более значимыми для пациента, поэтому их применение предпочтительно при проведении исследований. Суррогатные точки менее значимы для пациента, но более просты в измерении и позволяют ускорить исследовательский процесс, что сохраняет интерес к ним как к возможной альтернативе конечным точкам.
Глава 5
|
|
|


