 |
Механизм ретроингибирования антибиотиков
|
|
|
|
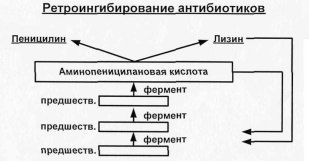
Когда аминоадипиновая кислота накапливается в достаточном количестве для клетки, она начинает реагировать с первым ферментом цепочки (ключевым ферментом), связывается с его аллостерическим центром, в результате чего изменяется структура активного центра фермента и синтез прекращается. Когда
концентрация аминоадипиновой кислоты снижается, синтез начинается снова. Если лизина в клетке много, он также может выключить процесс своего образования, а так как аминоадипиновая кислота – его предшественник и образуется с лизином в одном метаболическом пути, то ее образование также прекращается. Биотехнологу для достижения большого выхода целевого продукта следует работать со штаммами, где разрегулирована (нарушена) система ретроингибирования.
Механизмы развития резистентности у бактерий.
Плазмиды – носители генов информации (всего около 30 генов). Плазмиды автономно реплицируются (размножаются) независимо от деления клетки. Плазмиды могут содержать гены резистентности (устойчивости) к разным антибиотикам. Плазмиды с генами резистентности легко передаются из клетки в клетку при коньюгации микроорганизмов. При этом двойная нить плазмиды расходится на две отдельные нити и одна остается в клетке донора, а другая передается реципиенту. Особенно часто это явление наблюдается в больницах (внутрибольничная инфекция). Коньюгация м/о может быть не только внутривидовой, но и межвидовой и даже межродовой; возможна «вспышка» - вся микрофлора может стать резистентной к антибиотикам. Схема развития плазмидной резистентности.
Первоисточник генов резистентности находится в почве у почвенных микроорганизмов – продуцентов антибиотиков. Они могут передаваться через промежуточных хозяев патогенным микроорганизмам.
|
|
|
Борьба с резистентностью микроорганизмов.
1. β-лактамы инактивируются β-лактамазами, которые расщепляют их β- лактамное кольцо. Основной путь борьбы с β-лактамазами – создание молекул, которые не захватываются активным центром β- лактамаз.
Создают полусинтетический антибиотик (например, оксациллин или метициллин), которые не чувствительны к пенициллазам.
Механизм создания полусинтетических пенициллинов:
а) отщепление бензильного радикала (остается о-аминопенициллановая кислота – 6АПК).
б) введение других радикалов химическим путем.
Так же идет работа с цефалоспоринами: радикалы присоединяют к 7- аминоцефалоспориновой кислоте (7АЦК).
После того как новые антибиотики внедряются в практику, они становятся селективным фоном отбора для резистентности микроорганизмов, таким образом постепенно создаются резистентные штаммы.
2. Создание ингибиторов β-лактамаз, созданы комбинированные препараты, содержащие антибиотик и ингибитор β-лактамаз.
Уназин (ампициллин + сульбактам - ингибитор пенициллазы).
Амоксиклав (амоксициллин + клавулановая кислота – ингибитор
Пенициллазы).
Аугментин (амоксициллин + клавулановая кислота но в другом
Соотношении).
Резистентность может существовать также за счет генов клетки

У некоторых клеток есть гены, которые делают мембраны непроницаемыми для антибиотиков (сужаются поры или снижается их количество).
Способы борьбы с этой резистнтностью
1. Создан β-лактамный антибиотик Имипинем, который в растворе образует цвиттер-ион, меньший по размерам, чем пенициллин и легко проникает через узкие пориновые каналы.
2. Могут быть созданы структуры, которые проникают не через пориновые каналы, а другим способом, например, с помощью имитации структуры переносчика. Есть цефалоспорин, имитирующий переносчик железа и, попадая в клетку, он угнетает синтез пептидогликана, ингибируя транспептидазу).
|
|
|
-цефалоспорины Ш поколения не расщепляются β-лактамазами, но они являются индукторами выработки β-лактамаз,
- цефалоспорины 1У поколения (Цефепим) не являются индукторами β- лактамаз.
3. аминогликозидный антибиотик Амикацин имеет фрагмент гаммаоксимасляной кислоты в структуре канамицина защищающий этот антибиотик от инактивации со стороны изоферментов этого антибиотика, поэтому этот антибиотик отличается высоким терапевтическим эффектом.
Теория взаимозаменяемости антибиотиков.
В настоящее время есть 4 группы антибиотиков широкого спектра действия (β-лактамы, аминогликозиды, фторхинолоны тетрациклины). Еслипопробовать запретить применение одной группы (например, группы №1)антибиотиков, то резистентность к ним исчезает через 10 лет. Послевозобновления применения 1-ой группы, запрещают применение 2-ой группыи т.д.Но сейчас нельзя исключить ни одной группы антибиотиков из практикилечения, так как достаточно активных и безопасных антибиотиков еще не
хватает и требуется создавать новые и новые группы,.но, со временем, наверное, можно применить такую схему чередования разных групп антибиотиков для повышения терапевтического эффекта.
Известно, что в разных частях бактериальной клетки транспептидаза пептидогликана как белок неодинакова, с другой стороны, все многочисленные антибиотики имеют одинаковый механизм действия на патогенный микроорганизм, поэтому в рекомендациях по применению антибиотиков различного характера имеется информация по взаимодействию их с пенициллинсвязывающими белками (ПБС ). Эта
рекомендация связана с иммунитетом человека, принимающего антибиотики. Если есть информация в рекомендациях по применению, что новый антибиотик связывается с ПБС-2, то это означает, что клетка
микроорганизма будет активно лизироваться и освобождающиеся полисахариды в большом количестве будут поступать в кровь, что в свою очередь работает как пирогенный фактор и ведет к повышению
температуры больного на короткое время. Такие антибиотики могут быть рекомендованы больным с невысоким уровнем иммунитета (например, это больные СПИДом). Если же есть информация о ПБС-3, то это означает, что в результате действия такого антибиотика бактериальная клетка только временно перестает делиться, оставаясь живой и после отмены этого антибиотика, она начинает снова свое размножение с большой активностью и с опасностью возникновения новой инфекции. Для людей с низким иммунитетом применение таких антибиотиков опасно. Реализуя в продаже тот или иной антибиотик, вы должны предупреждать врачей о таком факте.
|
|
|
Биотехнология стероидных гормонов. Структура стероидных препаратов. Традиционные источники получения стероидных гормонов.. Проблемы трансформации стероидных структур. Приимущество биотрансформации перед химической трансормацией. Штаммы микроорганизмов., обладающие к способности к трансформации (биоконверсии) стероидов. Конкретные реакции биоконверсии стероидов. Подходы к решению селективности процессов биокнверсии..
Применение модля синтеза лс делят на 2 направления:
1. Полный биосинтез мо БАВ(антибиотиков, витаминов, ферментов, стеринов)
2. Микробиологическая трансформация- когда совмест использ химические и микробиологические стадии.
*+* -упрощается синтез лс
- продукты более чистые без примесей
-осуществляется рентабильный промыш синтез
-большинство процессов макробиол синтеза приводит к перестройке молекул субстратов
-это трансфор может осуш-ся одним или неск ферментами.
Принята микробиологическая трансформация, по типу возникновения или отщепления функ группы.
Основные принцыпы микробиол трансформации:
1. окисление2.Восстановление3.Гидролиз4. дегидрирование5. декарбоксилирование6. дезаминирование7. образование гикозидов8.метилирование9. ацетилирование
Структура стер препар:
Производные этого циклического ряда_ стерины, стеролы.
К ним относится стероиды, у которых в С3 имеется гидроксильная группа.
Предстовители:
-кортикосероиды(гидрокорт, преднизолон)
-Прогестерон(прогестерон, оксипрогестерон)
-андроген(тетстестерон,метилтестестер)
|
|
|
-эстроген(эстрон)
Все содержат в С3 кетогруппу. Кроме эстрогенов.
Андроген и эстроген содержит при С17 карбонильную или гидроксильную группу.
Из аналоги при С17 имеет алкильную или этинильную гр.
Прогестерон и кортикостерон принадлеж к замещенным прегнанам.
Источ получения:
Одним из наиболее изуч явл:
-холестерин(кл зоостерины)-обназ во всех органах и тканях, приним участие в разви растущ организмаю
Для получения стероидов примен:
- фитостерины (стерины растений) эргостерин отличается от халестерина в дополнит метильной гр при С24 и 2х допол двойных связей при С7 и С22, 23
-Эргостерин является провитамином витамина Д(строение установлено в 1934)
-Стигмастерин –содерж в соевом масле, сах таснике и отлич от холестен наличием этильной группы при С24.
B-ситостерин- наиболее экономичны, аналог сигмастерина получ из сахар тросника и хлоп масла, содержится во всех растениях и отходах древесины.
Для использов ситостерона в производстве стероидных гормонов осуществ направленное окисление боковой цепи стерина с образованием 17кетоандростона.
*стероиды трудно раствор в воде,. то и цеевой продукт трансформации практически на 99% выделяется в виде криссталов.
* культуральныю жидкость отфильтровывают и выделяют биомассу с целевым продуктом +ацетон, фильтруют отдел от биомассы целевой продукт 17кетоадростон., затем ацет р-р концентрир и выделяют ад для послед перекристаллизации.
|
|
|


